 是中学常用的氧化剂。实验室制备
是中学常用的氧化剂。实验室制备 并探究其性质:
并探究其性质:实验一:制备
 。①高温下,在熔融KOH中用
。①高温下,在熔融KOH中用 氧化
氧化 制备
制备 ;②水浸后冷却,调整溶液pH至弱碱性,
;②水浸后冷却,调整溶液pH至弱碱性, 歧化生成
歧化生成 和
和 ;③减压过滤,将滤液蒸发浓缩、冷却结晶,再减压过滤得
;③减压过滤,将滤液蒸发浓缩、冷却结晶,再减压过滤得 。
。(1)步骤①选择_______(填字母)。
| A.瓷坩埚 | B.铝坩埚 | C.铁坩埚 | D.石英坩埚 |
(3)利用如图所示装置过滤。减压过滤的优点是
 晶体的操作是
晶体的操作是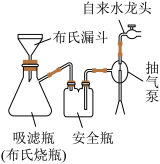
实验二:探究
 性质。在5.0mL 0.1
性质。在5.0mL 0.1
 溶液(含稀硫酸)中加入10.0mL 0.5
溶液(含稀硫酸)中加入10.0mL 0.5
 溶液,测得
溶液,测得 体积(V)与时间(t)关系如图所示。
体积(V)与时间(t)关系如图所示。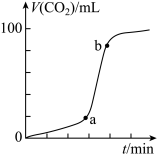
(4)关于ab段速率“突增”的原因(不考虑热效应),有同学猜想:可能是
 对反应起催化作用。为了证实其猜想,请完成下列实验方案。
对反应起催化作用。为了证实其猜想,请完成下列实验方案。| 实验 | 0.1  (aq)(含稀硫酸) (aq)(含稀硫酸) | 0.5  (aq) (aq) | 添加物质 | 记录溶液褪色时间/s |
| Ⅰ | 2.0mL | 2.0mL | 无 |  |
| Ⅱ | ①_______。 | 2.0mL | ②_______。 |  |
 ,上述猜想正确。①
,上述猜想正确。①实验三:测定
 样品纯度(杂质不参与反应)。准确称量m g高锰酸钾样品溶于水,加入稀硫酸酸化,加入
样品纯度(杂质不参与反应)。准确称量m g高锰酸钾样品溶于水,加入稀硫酸酸化,加入 mL
mL

 溶液(过量),充分反应后,用
溶液(过量),充分反应后,用
 标准
标准 溶液滴定至终点,消耗滴定液
溶液滴定至终点,消耗滴定液 mL。
mL。(5)滴定终点现象是
(6)该样品纯度为
 、
、 、
、 、
、 的式子表示)。若滴定
的式子表示)。若滴定 溶液前俯视读数,滴定后仰视读数,则测得结果
溶液前俯视读数,滴定后仰视读数,则测得结果
更新时间:2022-11-05 11:15:20
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】碳酸亚铁(FeCO3)可作为补血剂。利用某硫酸厂产生的烧渣(主要含Fe2O3、FeO,还有一定量的SiO2)制备FeCO3的流程如图:
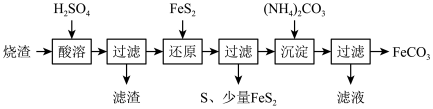
(1)“酸溶”步骤所得溶液中金属阳离子有___ (写离子符号),滤渣的成分是____ (写化学式)。
(2)“还原”步骤中FeS2(Fe元素为+2价)与H2SO4不反应;Fe3+通过两个反应被还原,其中一个反应如下:FeS2+14Fe3++8H2O=15Fe2++2SO +16H+,则另一个反应的离子方程式为
+16H+,则另一个反应的离子方程式为____ 。
(3)“沉淀”步骤需要控制温度在35℃以下,原因之一是为了防止____ 分解(写物质名称)。
(4)“沉淀”步骤中获得目标产品的化学方程式为____ 。
(5)FeCO3补血剂需密封包装的原因是____ 。
(6)FeCO3在空气中煅施生成Fe2O3时,也会生成FeO。现煅烧11.6kg的FeCO3,使其完全反应得到Fe2O3和FeO的混合物7.92kg,则Fe2O3的质量为____ kg。

(1)“酸溶”步骤所得溶液中金属阳离子有
(2)“还原”步骤中FeS2(Fe元素为+2价)与H2SO4不反应;Fe3+通过两个反应被还原,其中一个反应如下:FeS2+14Fe3++8H2O=15Fe2++2SO
 +16H+,则另一个反应的离子方程式为
+16H+,则另一个反应的离子方程式为(3)“沉淀”步骤需要控制温度在35℃以下,原因之一是为了防止
(4)“沉淀”步骤中获得目标产品的化学方程式为
(5)FeCO3补血剂需密封包装的原因是
(6)FeCO3在空气中煅施生成Fe2O3时,也会生成FeO。现煅烧11.6kg的FeCO3,使其完全反应得到Fe2O3和FeO的混合物7.92kg,则Fe2O3的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】随着新型冠状病毒感染的肺炎确诊病例越来越多,消毒已成了人们关注的话题。前不久李兰娟院士说过新冠病毒的几个弱点,比如含氯的消毒剂就可以有效的灭活病毒。某校化学兴趣小组为制备并收集氯气,设计下图装置,装置中的夹持装置和加热装置均已略去。
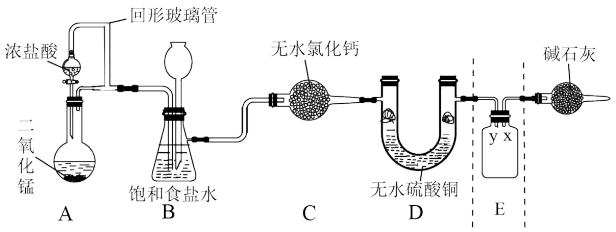
回答下列问题:
(1)写出盛放浓盐酸的仪器名称_______ ,回形玻璃管的作用是_______ 。
(2)写出装置A中发生反应的化学方程式_______ 。
(3)装置C的作用是_______ 。
(4)E装置中导管_______ (填“x”或“y”)应伸至靠近集气瓶底部。
(5)ClO2是目前国际上公认的新一代高效、广谱、安全的杀菌、保鲜剂,在水处理等方面具有广泛的应用。与Cl2相比,ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
①我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示:
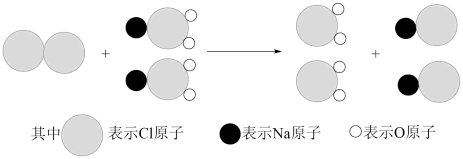
该反应的化学方程式_______ 。
②将ClO2通入酸性淀性粉碘化钾溶液,溶液变成蓝色,ClO2被还原为氯离子,该反应的离子方程式为:_______ 。

回答下列问题:
(1)写出盛放浓盐酸的仪器名称
(2)写出装置A中发生反应的化学方程式
(3)装置C的作用是
(4)E装置中导管
(5)ClO2是目前国际上公认的新一代高效、广谱、安全的杀菌、保鲜剂,在水处理等方面具有广泛的应用。与Cl2相比,ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
①我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示:

该反应的化学方程式
②将ClO2通入酸性淀性粉碘化钾溶液,溶液变成蓝色,ClO2被还原为氯离子,该反应的离子方程式为:
您最近一年使用:0次
【推荐3】K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。请回答下列问题:
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]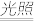 2FeC2O4+3K2C2O4+2CO2↑:显色反应的化学反应式为: FeC2O4+K3[Fe(CN)6] →Fe3[Fe(CN)6]2+
2FeC2O4+3K2C2O4+2CO2↑:显色反应的化学反应式为: FeC2O4+K3[Fe(CN)6] →Fe3[Fe(CN)6]2+______ ,配平并完成该显色反应的化学方程式。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。
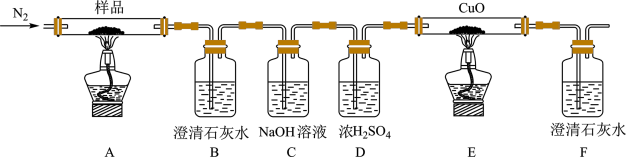
①通入氮气的目的是_________________ 。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有_______ ,____ 。
③样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:____ 。
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]
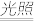 2FeC2O4+3K2C2O4+2CO2↑:显色反应的化学反应式为: FeC2O4+K3[Fe(CN)6] →Fe3[Fe(CN)6]2+
2FeC2O4+3K2C2O4+2CO2↑:显色反应的化学反应式为: FeC2O4+K3[Fe(CN)6] →Fe3[Fe(CN)6]2+(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。

①通入氮气的目的是
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有
③样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】我国科学家最近揭示氢化钡固氮加氢产生氨气的反应机理。某小组设计实验制备高纯度的BaH2并测定其纯度。
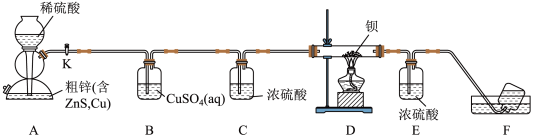
请回答下列问题:
(1)写出氢化钡的电子式_______ 。
(2)粗锌较纯锌相比,与稀硫酸反应产生H2速率较快,请解释原因_______ 。
(3)实验中B装置出现的现象是_______ 。
(4)先启动A中反应,F处检验氢气纯净后点燃D处酒精灯,这样操作的目的是_______ 。
(5)实验完毕,从A装置的混合物中提取ZnSO4·7H2O的一系列操作包括_______ 、过滤、洗涤、干燥。
(6)已知:氢化钡遇水剧烈反应。设计如图装置测定氢化钡纯度。室温下,向恒压分液漏斗中加入足量水,乙管实验前对应气体体积读数为V1mL,甲中完全反应后乙管气体体积读数为V2mL(V2>V1)。
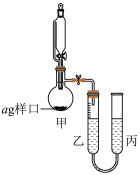
①D每次读数前要调整丙管高度,使其与乙管液面持平,其目的是_______ 。
②已知室温下,气体摩尔体积为VmL/mol,该产品纯度为_______ ,若实验结束时,未调平乙管和丙管的液面,且丙管的液面高于乙管,所测得产品纯度_______ (填“偏高”或“偏低”)。

请回答下列问题:
(1)写出氢化钡的电子式
(2)粗锌较纯锌相比,与稀硫酸反应产生H2速率较快,请解释原因
(3)实验中B装置出现的现象是
(4)先启动A中反应,F处检验氢气纯净后点燃D处酒精灯,这样操作的目的是
(5)实验完毕,从A装置的混合物中提取ZnSO4·7H2O的一系列操作包括
(6)已知:氢化钡遇水剧烈反应。设计如图装置测定氢化钡纯度。室温下,向恒压分液漏斗中加入足量水,乙管实验前对应气体体积读数为V1mL,甲中完全反应后乙管气体体积读数为V2mL(V2>V1)。

①D每次读数前要调整丙管高度,使其与乙管液面持平,其目的是
②已知室温下,气体摩尔体积为VmL/mol,该产品纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如图:已知 在低温下溶解度较小。
在低温下溶解度较小。
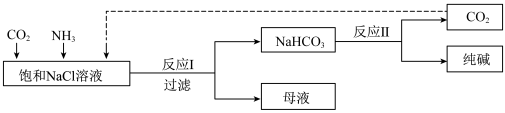
(1)一定温度下,往一定量饱和NaCl溶液中先通入___________ 达到饱和后,再不断通入另一种气体,一段时间后,出现沉淀,过滤得到 晶体。
晶体。
(2)得到的 晶体中可能含有少量NaCl、
晶体中可能含有少量NaCl、 等杂质,检验该晶体中是否含有氯离子杂质的操作方法是
等杂质,检验该晶体中是否含有氯离子杂质的操作方法是___________ 。
(3) 和
和 是两种常见的钠盐,
是两种常见的钠盐, 和
和 溶于水溶液均显
溶于水溶液均显___________ (填“酸性”、“中性”或“碱性”)。写出向饱和碳酸钠溶液中通入 的离子方程式
的离子方程式___________ 。
Ⅱ.工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中 的含量。
的含量。
(4)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧两侧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若___________ ,说明装置不漏气。
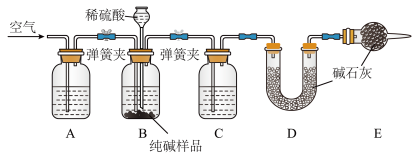
(5)装置A中的试剂为___________ ,装置C中的试剂为___________ 。
(6)实验前称取28.80g样品,实验后测得D装置增重8.80g,则样品中 的质量分数为
的质量分数为___________ (保留小数点后一位):若缺少E装置,会使测定结果___________ (填“偏高”或“偏低”)。
 在低温下溶解度较小。
在低温下溶解度较小。
(1)一定温度下,往一定量饱和NaCl溶液中先通入
 晶体。
晶体。(2)得到的
 晶体中可能含有少量NaCl、
晶体中可能含有少量NaCl、 等杂质,检验该晶体中是否含有氯离子杂质的操作方法是
等杂质,检验该晶体中是否含有氯离子杂质的操作方法是(3)
 和
和 是两种常见的钠盐,
是两种常见的钠盐, 和
和 溶于水溶液均显
溶于水溶液均显 的离子方程式
的离子方程式Ⅱ.工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中
 的含量。
的含量。(4)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧两侧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若

(5)装置A中的试剂为
(6)实验前称取28.80g样品,实验后测得D装置增重8.80g,则样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】废钼催化剂中钼、钴、镍等有价金属作为二次资源可加以回收利用。一种从废钼催化剂(主要成分为 、
、 ,含少量CoO、CoS、NiO、
,含少量CoO、CoS、NiO、 等)中回收有价金属的工艺流程如下:
等)中回收有价金属的工艺流程如下: ,
,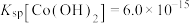 。
。
②当溶液中剩余金属离子的浓度 时,视为已沉淀完全。
时,视为已沉淀完全。
③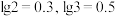 。
。
回答下列问题:
(1)基态Mo原子的价层电子排布式为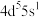 ,则Mo在元素周期表中的位置为
,则Mo在元素周期表中的位置为_______ 。
(2)“焙烧”时先将废钼催化剂磨成粉末,然后采取如图所示的“多层逆流焙烧”,其目的是_______ 。“焙烧”时生成的气体A的主要成分为_______ (写化学式)。 转化为
转化为 。“碱浸”时,
。“碱浸”时, 参与反应的离子方程式为
参与反应的离子方程式为_______ 。
(4)“除铁”时,若溶液中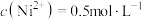 、
、 、
、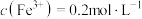 ,加入适量NaOH溶液调节pH(溶液体积变化忽略不计),可以使
,加入适量NaOH溶液调节pH(溶液体积变化忽略不计),可以使 沉淀完全,则调节pH的范围为
沉淀完全,则调节pH的范围为_______ 。
(5)若除铁后所得滤液中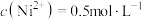 ,“沉镍”后所得滤液中
,“沉镍”后所得滤液中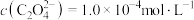 ,则沉镍率=
,则沉镍率=_______ [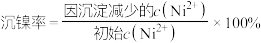 ,计算过程中不考虑溶液体积变化]。
,计算过程中不考虑溶液体积变化]。
(6)在空气中加热18.3g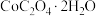 ,其热重曲线如图所示。a点对应固体的成分是
,其热重曲线如图所示。a点对应固体的成分是_______ (填化学式,下同);b、c点对应固体均为钴的氧化物,则b、c点对应固体的成分分别是_______ 、_______ 。
 、
、 ,含少量CoO、CoS、NiO、
,含少量CoO、CoS、NiO、 等)中回收有价金属的工艺流程如下:
等)中回收有价金属的工艺流程如下: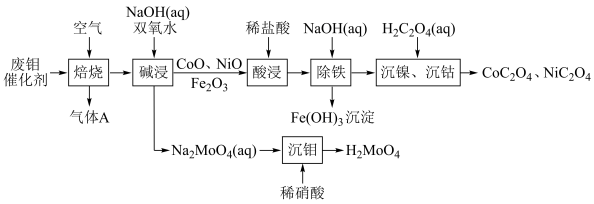
 ,
,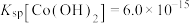 。
。②当溶液中剩余金属离子的浓度
 时,视为已沉淀完全。
时,视为已沉淀完全。③
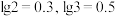 。
。回答下列问题:
(1)基态Mo原子的价层电子排布式为
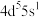 ,则Mo在元素周期表中的位置为
,则Mo在元素周期表中的位置为(2)“焙烧”时先将废钼催化剂磨成粉末,然后采取如图所示的“多层逆流焙烧”,其目的是
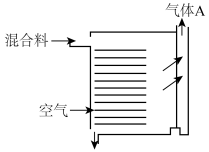
 转化为
转化为 。“碱浸”时,
。“碱浸”时, 参与反应的离子方程式为
参与反应的离子方程式为(4)“除铁”时,若溶液中
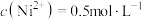 、
、 、
、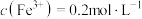 ,加入适量NaOH溶液调节pH(溶液体积变化忽略不计),可以使
,加入适量NaOH溶液调节pH(溶液体积变化忽略不计),可以使 沉淀完全,则调节pH的范围为
沉淀完全,则调节pH的范围为(5)若除铁后所得滤液中
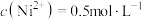 ,“沉镍”后所得滤液中
,“沉镍”后所得滤液中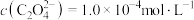 ,则沉镍率=
,则沉镍率=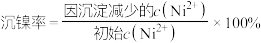 ,计算过程中不考虑溶液体积变化]。
,计算过程中不考虑溶液体积变化]。(6)在空气中加热18.3g
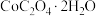 ,其热重曲线如图所示。a点对应固体的成分是
,其热重曲线如图所示。a点对应固体的成分是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某学习小组用如图所示装置测定铝镁合金中铝的质量分数和铝的相对原子质量。
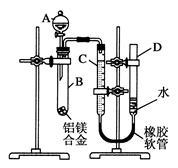
(1)A中的试剂为_________
(2)B中发生反应的化学方程式为_________________________________
(3)若实验用铝镁合金的质量为ag,测得 氢气体积为b mL(已换算为标准状况),B中剩余固体的质量为cg,则铝的质量分数为_______________ ,铝的相对原子质量为____________ 。
(4)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将________ (填“偏大”、“偏小”或“不受影响”)

(1)A中的试剂为
(2)B中发生反应的化学方程式为
(3)若实验用铝镁合金的质量为ag,测得 氢气体积为b mL(已换算为标准状况),B中剩余固体的质量为cg,则铝的质量分数为
(4)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】钠是很活泼的金属,在空气中燃烧的产物是Na2O2.Na2O的制取可以通过钠与硝酸钠共热反应完成:Na+NaNO3→Na2O+N2↑(未配平)。请回答下列问题:
(1)上述反应的氧化剂是_______ (写化学式)。制取Na2O时,若金属钠与NaNO3按质量比23∶17投料,充分反应后收集到的气体体积为1.12 m3(标准状况下),则制得的Na2O的质量为_______ kg。
(2)制取Na2O时由于设备密封性不好而进入了少量空气,导致制得的Na2O产品中含有Na2O2杂质。现有Na2O产品m g(假设只含有Na2O2杂质),请从下面选用合适的仪器和试剂,设计一种可选用的实验仪器组合,以完成样品中Na2O含量的测定。
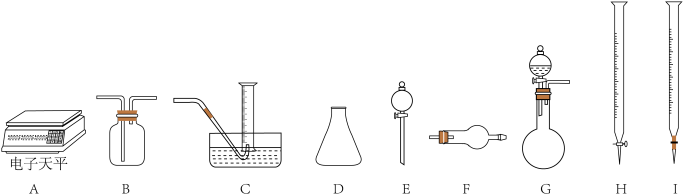
可选用的试剂:a.浓硫酸 b.水 c.盐酸标准溶液 d.NaOH标准溶液e.酚酞 f.碱石灰 g.稀盐酸
(3)某学生设计了以下实验方案来测定该试样中Na2O的质量分数,其操作流程和实验数据如下,该Na2O产品中Na2O的质量分数为_______ 。
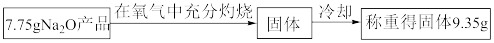
(1)上述反应的氧化剂是
(2)制取Na2O时由于设备密封性不好而进入了少量空气,导致制得的Na2O产品中含有Na2O2杂质。现有Na2O产品m g(假设只含有Na2O2杂质),请从下面选用合适的仪器和试剂,设计一种可选用的实验仪器组合,以完成样品中Na2O含量的测定。

可选用的试剂:a.浓硫酸 b.水 c.盐酸标准溶液 d.NaOH标准溶液e.酚酞 f.碱石灰 g.稀盐酸
| 实验过程中发生反应的化学方程式 | 实验所需仪器(用字母表示) | 实验所需试剂(用字母表示) | 实验需直接测定的有关物理量(用文字说明) |
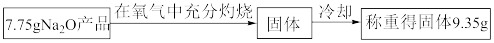
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】硫化锌(ZnS)是一种半导体材料,某小组在实验室制备硫化锌: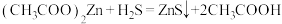 。回答下列问题:
。回答下列问题:
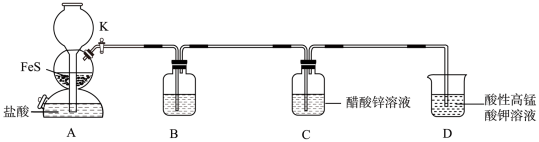
(1)装置A中发生反应的化学方程式为__________________ 。
(2)装置B中盛装的试剂可能是____________ (填标号)。
a.NaOH溶液 b.饱和NaHS溶液 c.新制氯水
(3)装置A能控制反应的发生和停止,装置C中完全反应后,停止装置A中反应的操作是____________ 。
(4)当装置D中0.01mol 完全反应时,转移0.08mol电子,则该反应中氧化产物与还原产物的物质的量之比为
完全反应时,转移0.08mol电子,则该反应中氧化产物与还原产物的物质的量之比为____________ 。
(5)实验完毕后,从装置C中得到较纯净的ZnS的操作是____________ (填标号)、洗涤、干燥。
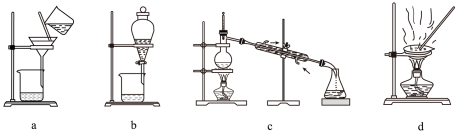
(6)测定ZnS产品纯度。
准确称取mg产品(杂质不含Zn元素)溶于足量盐酸,加热至不产生气泡,稀释成250mL溶液,准确量取25.00mL稀释后的溶液于锥形瓶中,调节pH在1.5~3,用二苯胺作指示剂,用 的亚铁氰化钾{
的亚铁氰化钾{ }标准溶液滴定至终点,消耗标准溶液VmL。
}标准溶液滴定至终点,消耗标准溶液VmL。
已知:滴定反应为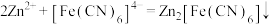 。
。
①加热的目的是____________ 。
②该产品中ZnS的质量分数为____________ (用含m、c、V的代数式表示)%。
③如果其他操作均正确,滴定前俯视读数,滴定终点时仰视读数,那么测得结果____________ (填“偏高”、“偏低”或“无影响”)。
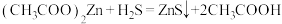 。回答下列问题:
。回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)装置B中盛装的试剂可能是
a.NaOH溶液 b.饱和NaHS溶液 c.新制氯水
(3)装置A能控制反应的发生和停止,装置C中完全反应后,停止装置A中反应的操作是
(4)当装置D中0.01mol
 完全反应时,转移0.08mol电子,则该反应中氧化产物与还原产物的物质的量之比为
完全反应时,转移0.08mol电子,则该反应中氧化产物与还原产物的物质的量之比为(5)实验完毕后,从装置C中得到较纯净的ZnS的操作是

(6)测定ZnS产品纯度。
准确称取mg产品(杂质不含Zn元素)溶于足量盐酸,加热至不产生气泡,稀释成250mL溶液,准确量取25.00mL稀释后的溶液于锥形瓶中,调节pH在1.5~3,用二苯胺作指示剂,用
 的亚铁氰化钾{
的亚铁氰化钾{ }标准溶液滴定至终点,消耗标准溶液VmL。
}标准溶液滴定至终点,消耗标准溶液VmL。已知:滴定反应为
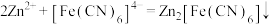 。
。①加热的目的是
②该产品中ZnS的质量分数为
③如果其他操作均正确,滴定前俯视读数,滴定终点时仰视读数,那么测得结果
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某同学设计如图装置,研究非金属元素性质变化规律。

(1)已知硅酸(H2SiO3)是一种难溶于水的弱酸,呈白色。在化学反应中,强酸一般能制取弱酸。现有硝酸溶液、碳酸钙、澄清石灰水、硅酸钠溶液,选择所给试剂,用如图装置来证明酸性:HNO3>H2CO3>H2SiO3。(不考虑硝酸的挥发性)
A、B、C中盛装的试剂分别为________ 、________ 、________ 。C中实验现象为_____________________________________________________ ;
写出C中发生反应的离子方程式:__________________________________ 。
(2)已知高锰酸钾在常温下与浓盐酸反应产生氯气,利用图中装置证明氯气氧化性强于碘单质的氧化性。A中盛装浓盐酸,B中装入高锰酸钾粉末,实验时C中溶液变成蓝色,则C中盛装的试剂为________ ;写出C中离子方程式____________________________________________________________________ 。
该实验该装置有明显不足,请指出改进方法:______________________________________________ 。
(3)如果C中盛装饱和氢硫酸(H2S饱和水溶液),A中装浓盐酸,B中装高锰酸钾溶液,反应开始后观察到现象是C中产生淡黄色沉淀。写出该反应的化学方程式:______________________________________ ;
如果将SO2气体通入饱和氢硫酸溶液中,也会产生淡黄色沉淀,该过程体现SO2________ (填字母)。
A.漂白性 B.氧化性
C.还原性 D.酸性

(1)已知硅酸(H2SiO3)是一种难溶于水的弱酸,呈白色。在化学反应中,强酸一般能制取弱酸。现有硝酸溶液、碳酸钙、澄清石灰水、硅酸钠溶液,选择所给试剂,用如图装置来证明酸性:HNO3>H2CO3>H2SiO3。(不考虑硝酸的挥发性)
A、B、C中盛装的试剂分别为
写出C中发生反应的离子方程式:
(2)已知高锰酸钾在常温下与浓盐酸反应产生氯气,利用图中装置证明氯气氧化性强于碘单质的氧化性。A中盛装浓盐酸,B中装入高锰酸钾粉末,实验时C中溶液变成蓝色,则C中盛装的试剂为
该实验该装置有明显不足,请指出改进方法:
(3)如果C中盛装饱和氢硫酸(H2S饱和水溶液),A中装浓盐酸,B中装高锰酸钾溶液,反应开始后观察到现象是C中产生淡黄色沉淀。写出该反应的化学方程式:
如果将SO2气体通入饱和氢硫酸溶液中,也会产生淡黄色沉淀,该过程体现SO2
A.漂白性 B.氧化性
C.还原性 D.酸性
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】草酸合铜(Ⅱ)酸钾是一种重要的化工原料,可用于无机合成、功能材料制备,其晶体组成可表示为 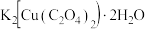 。
。
I.制备草酸合铜(Ⅱ)酸钾
向 溶液中滴加足量
溶液中滴加足量  溶液,产生浅蓝色沉淀,加热,沉淀转变成黑色,过滤,将
溶液,产生浅蓝色沉淀,加热,沉淀转变成黑色,过滤,将 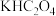 溶液加热至
溶液加热至 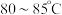 ,加入黑色沉淀
,加入黑色沉淀 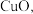 充分反应后,趁热过滤,得到草酸合铜 (Ⅱ)酸钾溶液。
充分反应后,趁热过滤,得到草酸合铜 (Ⅱ)酸钾溶液。
(1)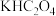 溶液最好采用
溶液最好采用___________ (填“酒精灯"或“水浴")加热;生成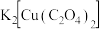 的化学方程式为
的化学方程式为___________ 。
(2)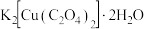 存在的化学键有
存在的化学键有___________ 。
A.氢键 B.范德华力 C.共价键 D.配位键 E.离子键
Ⅱ.产品的相关实验:
已知草酸合铜(Ⅱ)酸钾加热到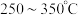 时会发生分解,生成
时会发生分解,生成 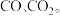 验证草酸合铜(Ⅱ)酸钾的分解产物中含有
验证草酸合铜(Ⅱ)酸钾的分解产物中含有 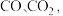 选用下列装置进行实验:
选用下列装置进行实验:
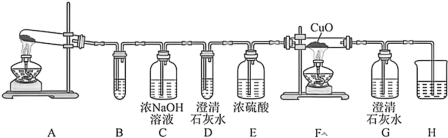
(3)装置B中盛放的试剂是___________ 。
(4)能说明产物中有 的实验现象是
的实验现象是___________
Ⅲ.草酸合铜 (Ⅱ)酸钾(摩尔质量为 )纯度的测定:
)纯度的测定:
准确称取草酸合铜(Ⅱ)酸钾晶体 溶于氨水,加水定容至
溶于氨水,加水定容至  ,取试样溶液
,取试样溶液  于锥形瓶中,水浴加热至
于锥形瓶中,水浴加热至 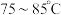 ,趁热用稀硫酸酸化的
,趁热用稀硫酸酸化的 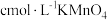 标准溶液滴定(滴定时发生反应:
标准溶液滴定(滴定时发生反应: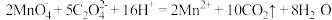 ),重复滴定三次,
),重复滴定三次, 标准溶液的平均用量为
标准溶液的平均用量为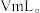
(5)盛装 标准溶液的仪器是
标准溶液的仪器是 ___________ (填“酸式”或“碱式”)滴定管;达到滴定终点的现象为___________ 。
(6)开始实验时盛有 的滴定管尖嘴部分有气泡,在滴定过程中气泡消失,会使测定结果
的滴定管尖嘴部分有气泡,在滴定过程中气泡消失,会使测定结果___________ 。(选填“偏高偏低”或“无影响”)
(7)产品的纯度为___________ %(用含c、V、m、M的式子表示)。
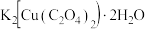 。
。I.制备草酸合铜(Ⅱ)酸钾
向
 溶液中滴加足量
溶液中滴加足量  溶液,产生浅蓝色沉淀,加热,沉淀转变成黑色,过滤,将
溶液,产生浅蓝色沉淀,加热,沉淀转变成黑色,过滤,将 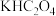 溶液加热至
溶液加热至 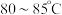 ,加入黑色沉淀
,加入黑色沉淀 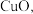 充分反应后,趁热过滤,得到草酸合铜 (Ⅱ)酸钾溶液。
充分反应后,趁热过滤,得到草酸合铜 (Ⅱ)酸钾溶液。(1)
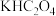 溶液最好采用
溶液最好采用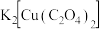 的化学方程式为
的化学方程式为(2)
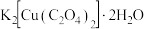 存在的化学键有
存在的化学键有A.氢键 B.范德华力 C.共价键 D.配位键 E.离子键
Ⅱ.产品的相关实验:
已知草酸合铜(Ⅱ)酸钾加热到
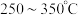 时会发生分解,生成
时会发生分解,生成 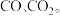 验证草酸合铜(Ⅱ)酸钾的分解产物中含有
验证草酸合铜(Ⅱ)酸钾的分解产物中含有 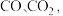 选用下列装置进行实验:
选用下列装置进行实验:
(3)装置B中盛放的试剂是
(4)能说明产物中有
 的实验现象是
的实验现象是Ⅲ.草酸合铜 (Ⅱ)酸钾(摩尔质量为
 )纯度的测定:
)纯度的测定:准确称取草酸合铜(Ⅱ)酸钾晶体
 溶于氨水,加水定容至
溶于氨水,加水定容至  ,取试样溶液
,取试样溶液  于锥形瓶中,水浴加热至
于锥形瓶中,水浴加热至 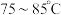 ,趁热用稀硫酸酸化的
,趁热用稀硫酸酸化的 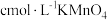 标准溶液滴定(滴定时发生反应:
标准溶液滴定(滴定时发生反应: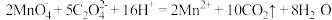 ),重复滴定三次,
),重复滴定三次, 标准溶液的平均用量为
标准溶液的平均用量为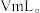
(5)盛装
 标准溶液的仪器是
标准溶液的仪器是 (6)开始实验时盛有
 的滴定管尖嘴部分有气泡,在滴定过程中气泡消失,会使测定结果
的滴定管尖嘴部分有气泡,在滴定过程中气泡消失,会使测定结果(7)产品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】四氧化锡可用作媒染剂。利用如图所示装置可以制备四氯化锡(部分夹持装置已略去);
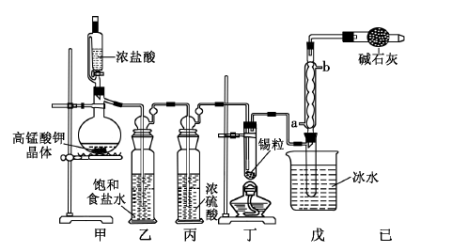
有关信息如下表:
回答下列问题:
(1)戊装置中冷凝管的进水口为___________ (填“a”或“b”)。
(2)用甲装置制氯气,MnO4-被还原为Mn2+,该反应的离子方程式为________________ 。
(3)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到___________ (填现象)后,开始加热丁装置,锡熔化后适当增大氯气流量,继续加热丁装置,此时继续加热丁装置的目的是:
①促进氯气与锡反应;
②_______________________________ 。
(4)如果缺少乙装置,可能产生的后果是___________________ ;己装置的作用是_________________ 。
(5)某同学认为丁装置中的反应可能产生SnCl2杂质,以下试剂中可用于检测是否产生SnCl2 的有_______________ (填标号)。
a.FeCl3溶液(滴有KSCN) b.H2O2溶液 C.溴水 d.AgNO3溶液
(6)反应中用去锡粒1.19g,反应后在戊装置的试管中收集到2.38gSnCl4,则SnCl4的产率为________ 。

有关信息如下表:
| 化学式 | SnCl2 | SnCl4 |
| 熔点/℃ | 246 | -33 |
| 沸点/℃ | 652 | 144 |
| 其他性质 | 无色晶体,易氧化 | 无色液体,易水解 |
(1)戊装置中冷凝管的进水口为
(2)用甲装置制氯气,MnO4-被还原为Mn2+,该反应的离子方程式为
(3)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到
①促进氯气与锡反应;
②
(4)如果缺少乙装置,可能产生的后果是
(5)某同学认为丁装置中的反应可能产生SnCl2杂质,以下试剂中可用于检测是否产生SnCl2 的有
a.FeCl3溶液(滴有KSCN) b.H2O2溶液 C.溴水 d.AgNO3溶液
(6)反应中用去锡粒1.19g,反应后在戊装置的试管中收集到2.38gSnCl4,则SnCl4的产率为
您最近一年使用:0次



