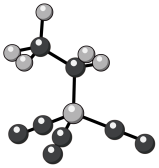
关于硅原子核外电子的描述错误的是
| A.有5种运动状态不同的电子 | B.有4种空间伸展方向 |
| C.有5种能量不同电子 | D.占据了8个轨道 |
更新时间:2022-10-22 20:58:54
|
相似题推荐
【推荐1】下列说法正确的是
| A.某价层电子排布为4d25s2的基态原子,该元素位于周期表中第五周期第ⅡA族 |
| B.在元素周期表中,s区、d区和ds区的元素都是金属元素 |
C.当碳原子的核外电子排布由 转变为 转变为 时,吸收能量,由激发态转化成基态 时,吸收能量,由激发态转化成基态 |
| D.非金属元素形成的共价化合物中,原子的最外层电子数不一定是2或8 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于能层与能级的说法中正确的是( )
| A.原子核外电子的每一个能层最多可容纳的电子数为2n2 |
| B.任一能层的能级总是从s能级开始,而且能级数少于该能层的能层序数 |
| C.同是s能级,在不同的能层中所能容纳的最多电子数是不相同的 |
| D.1个原子轨道里最多只能容纳2个电子,但自旋方向相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法不正确的是
① H2O2分子中既含极性键又含非极性键
②若R2—和M+的电子层结构相同,则原子序数:R>M
③ F2、Cl2、Br2、I2熔点随相对分子质量增大而升高
④ NCl3、PCl3、CO2、CS2分子中各原子均达到8e-稳定结构
⑤若X的质子数为a,中子数为b,则原子可表示为 X
X
⑥由于非金属性Cl>Br>I,所以酸性HCl>HBr>HI
⑦由于氨和水分子之间能形成氢键,NH3分子极易溶于水
⑧原子序数为34号的元素属于长周期的副族元素
① H2O2分子中既含极性键又含非极性键
②若R2—和M+的电子层结构相同,则原子序数:R>M
③ F2、Cl2、Br2、I2熔点随相对分子质量增大而升高
④ NCl3、PCl3、CO2、CS2分子中各原子均达到8e-稳定结构
⑤若X的质子数为a,中子数为b,则原子可表示为
 X
X⑥由于非金属性Cl>Br>I,所以酸性HCl>HBr>HI
⑦由于氨和水分子之间能形成氢键,NH3分子极易溶于水
⑧原子序数为34号的元素属于长周期的副族元素
| A.②⑤⑥⑧ | B.①③④⑤ | C.②④⑤⑦ | D.③⑤⑦⑧ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
| A.Fe3+的最外层电子排布式为3s23p63d5 |
| B.高温时CuO比Cu2O稳定 |
C.基态碳原子价电子的轨道表示式: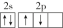 |
| D.元素周期表每一周期元素原子的最外层电子排布均是从ns1过渡到ns2np6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】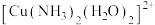 有两种配离子,其结构如图所示:
有两种配离子,其结构如图所示:
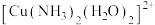 有两种配离子,其结构如图所示:
有两种配离子,其结构如图所示: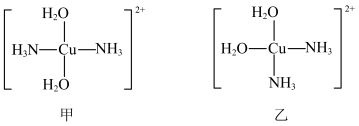
| A.甲、乙中Cu原子配位数均为4 |
| B.铜离子与两个氮原子、两个氧原子形成的空间结构为平面四边形 |
C.基态 的价层电子排布式是 的价层电子排布式是 |
D.中心离子 采用 采用 杂化 杂化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列化学用语的理解正确的是( )
| A.Cr的价电子排布式为3d44s2 |
B.氢氧根离子的电子式为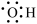 |
| C.1s22s22p3 和 1s22s22p4 能形成AB2型共价化合物 |
D.比例模型为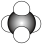 可以同时表示CH4和CCl4分子 可以同时表示CH4和CCl4分子 |
您最近一年使用:0次

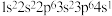
 :
: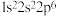
 :
: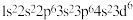
 :
: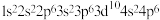
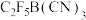 ]是可以用来合成稳定的全氟硼烷室温离子液体的阴离子(结构如图所示),具有良好的热稳定性及电化学稳定性。下列说法错误的是
]是可以用来合成稳定的全氟硼烷室温离子液体的阴离子(结构如图所示),具有良好的热稳定性及电化学稳定性。下列说法错误的是