某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
请回答:
(1)表中实验Ⅰ需加入蒸馏水V1=_______ 。验证浓度对反应速率影响的实验是_______ (填实验序号,下同)验证温度对反应速率影响的实验是_______ 。
(2)利用实验Ⅰ中数据计算,忽略混合前后溶液体积的微小变化,若用KMnO4的浓度变化表示的反应速率为:v(KMnO4)=_______ 。
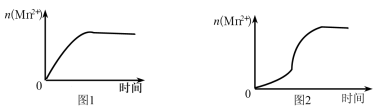
(3)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
①该小组同学提出的假设是_______ 。
②请你帮助该小组同学完成实验方案Ⅳ。
问题:该反应的催化剂选择MnCl2还是MnSO4_______ (填“MnCl2”或“MnSO4”)。
【实验原理】2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量/ mL | 试验温度/0C | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6mol·L-1H2C2O4溶液 | H2O | 3 mol·L-1稀硫酸 | 0.05mol·L-1KMnO4溶液 | |||
| Ⅰ | 3 | V1 | 2 | 3 | 25 | 1.5 |
| Ⅱ | 2 | 3 | 2 | 3 | 25 | 2.7 |
| Ⅲ | 2 | 3 | 2 | 3 | 40 | 1.3 |
(1)表中实验Ⅰ需加入蒸馏水V1=
(2)利用实验Ⅰ中数据计算,忽略混合前后溶液体积的微小变化,若用KMnO4的浓度变化表示的反应速率为:v(KMnO4)=
(3)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。

①该小组同学提出的假设是
②请你帮助该小组同学完成实验方案Ⅳ。
| 实验编号 | 室温下,试管中所加试剂及其用量 / mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间 / min | |||
| 0.6 mol·L-1H2C2O4溶液 | H2O | 3 mol·L-1稀硫酸 | 0.05mol·L-1KMnO4溶液 | |||
| Ⅳ | 3.0 | 2.0 | 2.0 | 3.0 | t | |
更新时间:2022-10-26 19:42:46
|
【知识点】 外因对化学反应速率影响的综合分析解读
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某同学欲探究硫代硫酸钠与酸反应速率的影响因素,设计了一系列如下实验,记录出现浑浊的时间:
(1)该反应的离子方程式为___ 。
(2)实验过程中为什么不用测量一定时间内放出SO2气体的量来表示该反应的化学反应速率大小___ 。
(3)若要探究温度对反应速率的影响,可以选择实验中的哪些组合来比较___ (填组号)。
(4)利用反应:I2+2Na2S2O3=Na2S4O6+2NaI可定量测定市售硫代硫酸钠的纯度,现称硫代硫酸钠固体样品配成溶液,取一定量溶液置于锥形瓶中,加入指示剂,用碘水滴定。回答下列各题:
①实验中滴定管应选择___ (填酸式或碱式)滴定管,滴定前可以选择___ 作为指示剂,滴定终点时的现象为___ 。
②下列操作测得硫代硫酸钠的含量偏大的是( )
A.滴定前滴定管内有气泡,滴定后气泡消失
B.读取碘水体积刻度时,滴定前平视,滴定后俯视
C.滴定过程中,锥形瓶振荡过于剧烈,有少量溶液溅出
D.滴定管用蒸馏水洗净后,直接加入碘水溶液
| 实验 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c(mol•L-1) | V/mL | c(mol•L-1) | V/mL | ||
| A | 10 | 5 | 0.1 | 5 | 0.1 | 5 |
| B | 10 | 5 | 0.1 | 5 | 0.1 | 10 |
| C | 30 | 5 | 0.1 | 5 | 0.1 | 5 |
| D | 30 | 5 | 0.2 | 5 | 0.2 | 10 |
(2)实验过程中为什么不用测量一定时间内放出SO2气体的量来表示该反应的化学反应速率大小
(3)若要探究温度对反应速率的影响,可以选择实验中的哪些组合来比较
(4)利用反应:I2+2Na2S2O3=Na2S4O6+2NaI可定量测定市售硫代硫酸钠的纯度,现称硫代硫酸钠固体样品配成溶液,取一定量溶液置于锥形瓶中,加入指示剂,用碘水滴定。回答下列各题:
①实验中滴定管应选择
②下列操作测得硫代硫酸钠的含量偏大的是
A.滴定前滴定管内有气泡,滴定后气泡消失
B.读取碘水体积刻度时,滴定前平视,滴定后俯视
C.滴定过程中,锥形瓶振荡过于剧烈,有少量溶液溅出
D.滴定管用蒸馏水洗净后,直接加入碘水溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某研究性学习小组为探究铁与稀盐酸反应,取同质量、体积的铁片、同浓度的盐酸做了下列平行实验:实验①:把纯铁片投入到盛有稀盐酸的试管中,发现放出氢气的速率变化如图所示:

实验②:把铁片投入到含FeCl3的同浓度稀盐酸中,发现放出氢气的量减少。
实验③:在稀盐酸中滴入几滴CuCl2溶液,用铁片做实验,发现生成氢气的速率加快。
试回答下列问题:
(1)分析实验①中t1~t2速率变化的主要原因是______ ,t2~t3速率变化的主要原因是______ 。
(2)实验②放出氢气的量减少的原因是______ (用离子方程式表示)。
(3)某同学认为实验③反应速率加快的主要原因是形成了原电池,你认为是否正确?______ (正确填“a”,不正确填“b”)。请回答下列相应的a或b问题。
a.若正确,则写出实验③中原电池的正、负极电极反应式______ 。b.若不正确,请说明原因。

实验②:把铁片投入到含FeCl3的同浓度稀盐酸中,发现放出氢气的量减少。
实验③:在稀盐酸中滴入几滴CuCl2溶液,用铁片做实验,发现生成氢气的速率加快。
试回答下列问题:
(1)分析实验①中t1~t2速率变化的主要原因是
(2)实验②放出氢气的量减少的原因是
(3)某同学认为实验③反应速率加快的主要原因是形成了原电池,你认为是否正确?
a.若正确,则写出实验③中原电池的正、负极电极反应式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】富硼渣中含有镁硼酸盐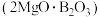 、镁硅酸盐
、镁硅酸盐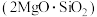 及少量
及少量 、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸
、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸 晶体的一种工艺流程如下:
晶体的一种工艺流程如下:
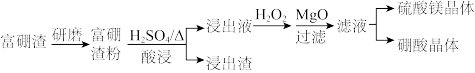
(1)在该工艺流程中为了加快化学反应速率的措施有___________ 种。
(2)写出酸浸过程镁硼酸盐发生反应的化学方程式:___________ 。
(3)浸出渣的主要成分是___________ (写化学式)。
(4)加入MgO后过滤的滤渣的主要成分是___________ 。
(5)为了获得硫酸镁晶体和硼酸 晶体,将滤液先浓缩至溶液接近饱和,然后将浓缩液放入高压签中,接下来的操作应该是
晶体,将滤液先浓缩至溶液接近饱和,然后将浓缩液放入高压签中,接下来的操作应该是___________ 。
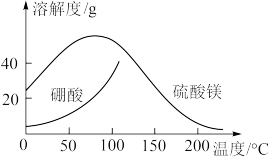
注:温度高时,硼酸会随水蒸气挥发
(6)单质硼可用于生成具有优良抗冲击性能的硼钢。以硼酸 和金属镁为原料可制备单质硼,用化学方程式表示制备过程:
和金属镁为原料可制备单质硼,用化学方程式表示制备过程:___________ 。
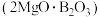 、镁硅酸盐
、镁硅酸盐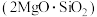 及少量
及少量 、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸
、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸 晶体的一种工艺流程如下:
晶体的一种工艺流程如下: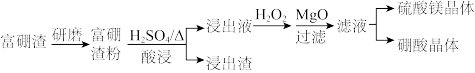
(1)在该工艺流程中为了加快化学反应速率的措施有
(2)写出酸浸过程镁硼酸盐发生反应的化学方程式:
(3)浸出渣的主要成分是
(4)加入MgO后过滤的滤渣的主要成分是
(5)为了获得硫酸镁晶体和硼酸
 晶体,将滤液先浓缩至溶液接近饱和,然后将浓缩液放入高压签中,接下来的操作应该是
晶体,将滤液先浓缩至溶液接近饱和,然后将浓缩液放入高压签中,接下来的操作应该是
注:温度高时,硼酸会随水蒸气挥发
(6)单质硼可用于生成具有优良抗冲击性能的硼钢。以硼酸
 和金属镁为原料可制备单质硼,用化学方程式表示制备过程:
和金属镁为原料可制备单质硼,用化学方程式表示制备过程:
您最近一年使用:0次



