汽车排气管装有三元催化剂装置,在催化剂表面通过发生吸附、解吸消除CO、NO等污染物。回答下列问题:
(1)消除CO、NO污染物的反应机理如下[Pt(s)表示催化剂,带“*”表示吸附状态]:
I.NO+Pt(s)=NO*;II.CO+Pt(s)=CO*;III.NO*=N*+O*;IV.CO*+O*=CO2+Pt(s);V.N*+N*=N2+Pt(s)
经测定汽车尾气中反应物浓度及生成物浓度随温度T变化关系如图一和图二所示。
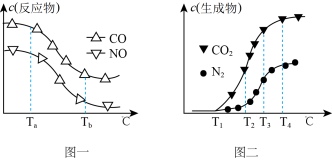
①图一中温度从Ta℃升至Tb℃的过程中,反应物浓度急剧减小的主要原因是_______ 。
②由图二知,T2℃时反应V的活化能_______ 反应IV的活化能(填“<”、“>”或“=”)。
(2)为模拟汽车的“催化转化器”,将2molNO(g)和2mol CO(g)充入1L密闭容器中,加入催化剂后发生反应2NO(g)+2CO(g)⇌N2(g)+2CO2(g),测得CO的平衡转化率α随温度T变化曲线如图三所示。
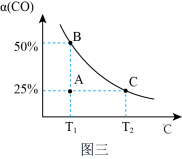
①图象中A点正反应速率_______ 逆反应速率(填“>”、“=”或“<”);
②T1℃,下列说法能表明该反应已达到平衡状态的是_______ (填序号)。
a.混合气体的密度不变b.体系的压强不变
c.混合气体中N2的体积分数不变d.2υ正(CO)=υ逆(N2)
(1)消除CO、NO污染物的反应机理如下[Pt(s)表示催化剂,带“*”表示吸附状态]:
I.NO+Pt(s)=NO*;II.CO+Pt(s)=CO*;III.NO*=N*+O*;IV.CO*+O*=CO2+Pt(s);V.N*+N*=N2+Pt(s)
经测定汽车尾气中反应物浓度及生成物浓度随温度T变化关系如图一和图二所示。

①图一中温度从Ta℃升至Tb℃的过程中,反应物浓度急剧减小的主要原因是
②由图二知,T2℃时反应V的活化能
(2)为模拟汽车的“催化转化器”,将2molNO(g)和2mol CO(g)充入1L密闭容器中,加入催化剂后发生反应2NO(g)+2CO(g)⇌N2(g)+2CO2(g),测得CO的平衡转化率α随温度T变化曲线如图三所示。

①图象中A点正反应速率
②T1℃,下列说法能表明该反应已达到平衡状态的是
a.混合气体的密度不变b.体系的压强不变
c.混合气体中N2的体积分数不变d.2υ正(CO)=υ逆(N2)
更新时间:2022-11-11 13:02:36
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:

(1)写出该反应的化学方程式_________________________ 。
(2)计算反应开始到10s,用X表示的反应速率是___________ 。
(3)下列叙述中能说明上述反应达到平衡状态的是_________ 。
a.当X与Y的反应速率之比为1:1
b.混合气体中X的浓度保持不变
c.X、Y、Z的浓度之比为1:1:2
(4)为使该反应的反应速率增大,可采取的措施是_______ 。
a.适当降低温度 b.扩大容器的体积 c.充入一定量Z

(1)写出该反应的化学方程式
(2)计算反应开始到10s,用X表示的反应速率是
(3)下列叙述中能说明上述反应达到平衡状态的是
a.当X与Y的反应速率之比为1:1
b.混合气体中X的浓度保持不变
c.X、Y、Z的浓度之比为1:1:2
(4)为使该反应的反应速率增大,可采取的措施是
a.适当降低温度 b.扩大容器的体积 c.充入一定量Z
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】茶温度下,在一个2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白:

(1)从开始至2min,X的平均反应速率为___________ 。
(2)该反应的化学方程式为___________ 。
(3)1min时,
___________ 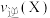 (填“>”、“<”或“=”下同),2min时,转化率
(填“>”、“<”或“=”下同),2min时,转化率
___________  。
。
(4)若2min时向容器中通入氩气(容器体积不变),X的化学反应速率将___________ (填“增大”、“减小”或“不变”。下同),5min时,压缩容器体积,反应速率会___________ 。
(5)若X、Y、Z均为气体(容器体积不变),下列能说明反应已达平衡的是___________ 。
a.X、Y、Z三种气体的浓度相等
b.混合气体的相对分子质量不随时间变化
c.混合气体的总压强不随时间变化
d.反应速率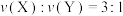
e.

(1)从开始至2min,X的平均反应速率为
(2)该反应的化学方程式为
(3)1min时,

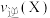 (填“>”、“<”或“=”下同),2min时,转化率
(填“>”、“<”或“=”下同),2min时,转化率
 。
。(4)若2min时向容器中通入氩气(容器体积不变),X的化学反应速率将
(5)若X、Y、Z均为气体(容器体积不变),下列能说明反应已达平衡的是
a.X、Y、Z三种气体的浓度相等
b.混合气体的相对分子质量不随时间变化
c.混合气体的总压强不随时间变化
d.反应速率
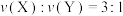
e.

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】一定条件下,将一定物质的量的A、B混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g),经5 min后测得:A的转化率达到了最大值,且A和B的转化率相等,C的平均反应速率为0.2 mol/(L·min),D的浓度为0.5 mol/L。
xC(g)+2D(g),经5 min后测得:A的转化率达到了最大值,且A和B的转化率相等,C的平均反应速率为0.2 mol/(L·min),D的浓度为0.5 mol/L。
(1)判断:此反应此时_______ (填“是”或“否”)达到了平衡状态。
(2)反应开始前容器中的A和B的物质的量之比为n(A):n(B)=_______ 。
(3)B的平均反应速率v(B)=________ mol/(L·min)。
(4)x的值为________ 。
 xC(g)+2D(g),经5 min后测得:A的转化率达到了最大值,且A和B的转化率相等,C的平均反应速率为0.2 mol/(L·min),D的浓度为0.5 mol/L。
xC(g)+2D(g),经5 min后测得:A的转化率达到了最大值,且A和B的转化率相等,C的平均反应速率为0.2 mol/(L·min),D的浓度为0.5 mol/L。(1)判断:此反应此时
(2)反应开始前容器中的A和B的物质的量之比为n(A):n(B)=
(3)B的平均反应速率v(B)=
(4)x的值为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】二甲醚(CH3OCH3)气体是一种可再生绿色新能源,被誉为“21 世纪的清洁燃料”。
(1)写出二甲醚一种同分异构体的结构简式:___________ 。
(2)已知:4.6g二甲醚气体完全燃烧生成液态水放出 145.5kJ 热量,写出其燃烧的热化学反应方程式___________ 。
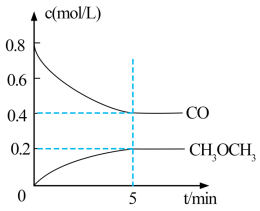
(3)工业上可用水煤气合成二甲醚:2CO(g) + 4H2(g)⇌CH3OCH3(g) + H2O(g)
①测得 CO 和 CH3OCH3(g)的浓度随时间变化如图所示,则反应开始至平衡时的 H2平均反应速率v(H2)=___________ mol/(L·min )。
②该反应在恒容密闭容器中进行,下列叙述中能表示该反应达到平衡状态的是___________ 。
A.单位时间内生成CO和H2的物质的量之比为1﹕2
B.CH3OCH3的浓度不再变化
C.容器内压强不再变化
D.CH3OCH3与H2O的物质的量相等
(4)二甲醚燃料电池工作原理如图所示
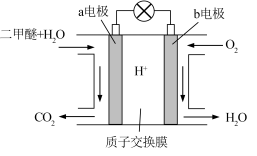
①该电池的负极是___________ (填“a 电极”或“b 电极”)
②H+通过质子交换膜时的移动方向是___________ 。(填选项字母)
A.从左向右 B.从右向左
③通入O2的电极反应式是___________ 。
(5)标况下每转移6mol电子需要氧气多少L______ ?(写出解题过程)
(1)写出二甲醚一种同分异构体的结构简式:
(2)已知:4.6g二甲醚气体完全燃烧生成液态水放出 145.5kJ 热量,写出其燃烧的热化学反应方程式
(3)工业上可用水煤气合成二甲醚:2CO(g) + 4H2(g)⇌CH3OCH3(g) + H2O(g)
①测得 CO 和 CH3OCH3(g)的浓度随时间变化如图所示,则反应开始至平衡时的 H2平均反应速率v(H2)=

②该反应在恒容密闭容器中进行,下列叙述中能表示该反应达到平衡状态的是
A.单位时间内生成CO和H2的物质的量之比为1﹕2
B.CH3OCH3的浓度不再变化
C.容器内压强不再变化
D.CH3OCH3与H2O的物质的量相等
(4)二甲醚燃料电池工作原理如图所示

①该电池的负极是
②H+通过质子交换膜时的移动方向是
A.从左向右 B.从右向左
③通入O2的电极反应式是
(5)标况下每转移6mol电子需要氧气多少L
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】I.在容积为2L的密闭容器中进行如下反应: ,开始时A为4mol,B为6mol;5min末时测得C为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。
,开始时A为4mol,B为6mol;5min末时测得C为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。
试回答下列问题:
(1)5min末A的物质的量浓度为___ 。
(2)前5min内用B表示的化学反应速率v(B)为___ 。
(3)化学方程式中n为___ 。
(4)此反应在四种不同情况下的反应速率如下:
①v(A)=5mol/(L·min)②v(B)=6mol/(L·min)③v(C)=4.5mol/(L·min)④v(D)=8mol/(L·min)
其中反应速率最快的是(填序号)___ 。
II.CO2可转化成有机物实现碳循环。在体积为1L的密闭容器中充入1molCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g) CH2OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH2OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(1)从3min到10min,v(H2)=___ mol/(L·min)。(到小数点后三位)
(2)能说明上述反应达到平衡状态的是___ 。
A.v(H2)=3v(H2O)
B.反应中CO2与CH3OH的物质的量浓度相等时(即图中3min时对应的点)
C.容器内压强不再发生变化
D.单位时间内每消耗3molH2,同时生成1molH2O
E.CO2的体积分数在混合气体中保持不变
F.混合气体的密度不再发生变化
 ,开始时A为4mol,B为6mol;5min末时测得C为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。
,开始时A为4mol,B为6mol;5min末时测得C为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。试回答下列问题:
(1)5min末A的物质的量浓度为
(2)前5min内用B表示的化学反应速率v(B)为
(3)化学方程式中n为
(4)此反应在四种不同情况下的反应速率如下:
①v(A)=5mol/(L·min)②v(B)=6mol/(L·min)③v(C)=4.5mol/(L·min)④v(D)=8mol/(L·min)
其中反应速率最快的是(填序号)
II.CO2可转化成有机物实现碳循环。在体积为1L的密闭容器中充入1molCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)
 CH2OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH2OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图所示。
(1)从3min到10min,v(H2)=
(2)能说明上述反应达到平衡状态的是
A.v(H2)=3v(H2O)
B.反应中CO2与CH3OH的物质的量浓度相等时(即图中3min时对应的点)
C.容器内压强不再发生变化
D.单位时间内每消耗3molH2,同时生成1molH2O
E.CO2的体积分数在混合气体中保持不变
F.混合气体的密度不再发生变化
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】向2L密闭容器中通入amol气体A和bmol气体B,在一定条件下发生反应:xA(g)+yB(g)  pC(g)+qD(g)已知:平均反应速率v(C)=
pC(g)+qD(g)已知:平均反应速率v(C)= v(A);反应2min时,A的浓度减少了
v(A);反应2min时,A的浓度减少了 ,B的物质的量减少了
,B的物质的量减少了 mol,有
mol,有 molD生成。回答下列问题:
molD生成。回答下列问题:
(1)反应2min内,v(A)=______________ ;v(B)=______________ ;
(2)下列叙述能说明该反应已达平衡状态的是:______ ;
A、 xV(A)正=qV(D)逆 B、气体总的质量保持不变 C、C的总质量保持不变 D、混合气体总的物质的量不再变化 E、混合气体总的密度不再变化 F、混合气体平均分子量不再变化
(3)反应平衡时,D为2amol,则B的转化率为________ ;
(4)其他条件不变,将容器的容积变为1L,进行同样的实验,则与上述反应比较,反应速率_____ (是“增大”“减小”或“不变”),
 pC(g)+qD(g)已知:平均反应速率v(C)=
pC(g)+qD(g)已知:平均反应速率v(C)= v(A);反应2min时,A的浓度减少了
v(A);反应2min时,A的浓度减少了 ,B的物质的量减少了
,B的物质的量减少了 mol,有
mol,有 molD生成。回答下列问题:
molD生成。回答下列问题:(1)反应2min内,v(A)=
(2)下列叙述能说明该反应已达平衡状态的是:
A、 xV(A)正=qV(D)逆 B、气体总的质量保持不变 C、C的总质量保持不变 D、混合气体总的物质的量不再变化 E、混合气体总的密度不再变化 F、混合气体平均分子量不再变化
(3)反应平衡时,D为2amol,则B的转化率为
(4)其他条件不变,将容器的容积变为1L,进行同样的实验,则与上述反应比较,反应速率
您最近一年使用:0次



