NF3是微电子工业中一种优良的等离子蚀刻气体,在1个标准大气压下,NF3的沸点为-129.0℃,能与空气中的水蒸气反应生成HF、NO和HNO3。NF3可通过如下方法制备:
(1)气-气反应:在常温下将OF2与干燥的空气混合即得NO2和NF3。
①原料OF2中氧元素的化合价为____ 。
②已知反应中每消耗1molN2转移7mol电子,配平反应:____ 。
____OF2+____N2+____O2=____NO2+____NF3
反应中氧化剂与还原剂的物质的量之比为____ 。
(2)气-固反应:由于气-气反应容易腐蚀设备,研究人员提出用气-固反应制备NF3。气-固反应包括如下两个步骤:
(NH4)3AlF6+6F2=2NF3+8HF+NH4AlF4
NH4AlF4+3F2=NF3+4HF+AlF3
①气-固反应的总化学方程式为____ ,若有0.5mol(NH4)3AlF6完全氧化,则可制得NF3____ L(标准状况下)。
②若要制备1.5molNF3,共有____ mol电子发生转移。
(3)NF3在空气中泄漏,还是易于发现的。判断发生了NF3泄漏的现象是____ 。一但NF3发生泄漏,可以用烧碱溶液喷淋的方法减少污染,其产物除NaNO2、NaF、H2O外还一定有____ (填化学式)。
(1)气-气反应:在常温下将OF2与干燥的空气混合即得NO2和NF3。
①原料OF2中氧元素的化合价为
②已知反应中每消耗1molN2转移7mol电子,配平反应:
____OF2+____N2+____O2=____NO2+____NF3
反应中氧化剂与还原剂的物质的量之比为
(2)气-固反应:由于气-气反应容易腐蚀设备,研究人员提出用气-固反应制备NF3。气-固反应包括如下两个步骤:
(NH4)3AlF6+6F2=2NF3+8HF+NH4AlF4
NH4AlF4+3F2=NF3+4HF+AlF3
①气-固反应的总化学方程式为
②若要制备1.5molNF3,共有
(3)NF3在空气中泄漏,还是易于发现的。判断发生了NF3泄漏的现象是
更新时间:2022-11-05 15:11:05
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)请配平下列方程式,并用双线桥法标出下列反应电子转移的方向和数目___________ 。
Al+NaNO3+NaOH=NaAlO2+N2↑+H2O
(2)某反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程H2O2→O2。
①该反应中的氧化剂是___________
②写出该反应的化学方程式___________
(3)①一种有效成分为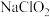 、
、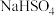 、
、 的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到
的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到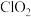 溶液。上述过程中,生成
溶液。上述过程中,生成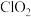 的反应属于歧化反应(氧化剂和还原剂为同一种物质的反应),每生成
的反应属于歧化反应(氧化剂和还原剂为同一种物质的反应),每生成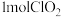 消耗
消耗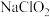 的量为
的量为___________ mol;产生“气泡”的化学方程式为___________ 。
②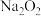 、
、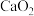 以及
以及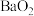 都可与酸反应生成过氧化氢,实验室通过上述某种过氧化物与适量稀硫酸反应,过滤后即可制得较纯净的
都可与酸反应生成过氧化氢,实验室通过上述某种过氧化物与适量稀硫酸反应,过滤后即可制得较纯净的 溶液,则最好选择的过氧化物是
溶液,则最好选择的过氧化物是___________ 。
(4)学生乙欲使用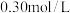 的HCl溶液950mL,现拟用36.5%(
的HCl溶液950mL,现拟用36.5%(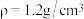 )的浓盐酸来配制,请回答下列问题:
)的浓盐酸来配制,请回答下列问题:
①应量取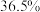 的盐酸的体积为
的盐酸的体积为___________  。
。
②该实验需要使用到的玻璃仪器有:烧杯、玻璃棒、胶头滴管、___________ 。
③下列操作会使所配溶液浓度小于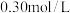 的是:
的是:___________ 。(填对应的序号)
a.容量瓶用蒸馏水洗净后没有烘干,瓶内有少量残留的蒸馏水;
b.在操作中没有用蒸馏水洗涤烧杯和玻璃棒;
c.定容时视线俯视刻度线;
d.定容时加蒸馏水超过了刻度线,倒出一些溶液,再重新加蒸馏水定容到刻度线;
e.将配制好的溶液转入试剂瓶的过程中不慎洒出了少许溶液;
f.用量筒量取浓盐酸时视线仰视刻度线。
(1)请配平下列方程式,并用双线桥法标出下列反应电子转移的方向和数目
Al+NaNO3+NaOH=NaAlO2+N2↑+H2O
(2)某反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程H2O2→O2。
①该反应中的氧化剂是
②写出该反应的化学方程式
(3)①一种有效成分为
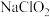 、
、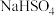 、
、 的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到
的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到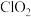 溶液。上述过程中,生成
溶液。上述过程中,生成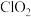 的反应属于歧化反应(氧化剂和还原剂为同一种物质的反应),每生成
的反应属于歧化反应(氧化剂和还原剂为同一种物质的反应),每生成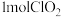 消耗
消耗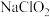 的量为
的量为②
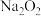 、
、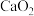 以及
以及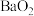 都可与酸反应生成过氧化氢,实验室通过上述某种过氧化物与适量稀硫酸反应,过滤后即可制得较纯净的
都可与酸反应生成过氧化氢,实验室通过上述某种过氧化物与适量稀硫酸反应,过滤后即可制得较纯净的 溶液,则最好选择的过氧化物是
溶液,则最好选择的过氧化物是(4)学生乙欲使用
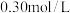 的HCl溶液950mL,现拟用36.5%(
的HCl溶液950mL,现拟用36.5%(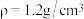 )的浓盐酸来配制,请回答下列问题:
)的浓盐酸来配制,请回答下列问题:①应量取
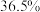 的盐酸的体积为
的盐酸的体积为 。
。②该实验需要使用到的玻璃仪器有:烧杯、玻璃棒、胶头滴管、
③下列操作会使所配溶液浓度小于
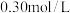 的是:
的是:a.容量瓶用蒸馏水洗净后没有烘干,瓶内有少量残留的蒸馏水;
b.在操作中没有用蒸馏水洗涤烧杯和玻璃棒;
c.定容时视线俯视刻度线;
d.定容时加蒸馏水超过了刻度线,倒出一些溶液,再重新加蒸馏水定容到刻度线;
e.将配制好的溶液转入试剂瓶的过程中不慎洒出了少许溶液;
f.用量筒量取浓盐酸时视线仰视刻度线。
您最近一年使用:0次
【推荐2】按要求回答以下问题
(1)金属加工后的废液中含有2%~5%的 ,它是一种环境污染物。人们用
,它是一种环境污染物。人们用 溶液来处理此废液,使亚硝酸钠转化为无毒物质。该反应分两步进行:
溶液来处理此废液,使亚硝酸钠转化为无毒物质。该反应分两步进行:
第一步:
第二步: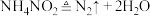
下列对上述反应的叙述中正确的是_______ (填字母)。
①两步均为氧化还原反应 ②第二步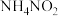 仅发生氧化反应③第二步
仅发生氧化反应③第二步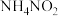 发生了分解反应④第二步中
发生了分解反应④第二步中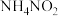 既被氧化又被还原 ⑤第一步为复分解反应
既被氧化又被还原 ⑤第一步为复分解反应
A.①③ B.①④ C.②③④ D.③④⑤
(2)实验室中,亚硝酸钠可用来处理过量的叠氮化钠 ,有关反应的化学方程式如下:
,有关反应的化学方程式如下:
a.
b.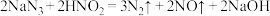
用双线桥法标出b反应中电子转移情况:_______ 。
(3)磷元素的含氧酸有 、
、 (亚磷酸)、
(亚磷酸)、 (次磷酸)等多种。其中已知
(次磷酸)等多种。其中已知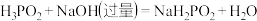 。
。 中磷元素的化合价是
中磷元素的化合价是_______ 。 属于
属于_______ (填“正盐”或“酸式盐”)。
(4) 可将溶液中的
可将溶液中的 转化为银,自身变为
转化为银,自身变为 ,可用于化学镀银。利用
,可用于化学镀银。利用 进行化学镀银的反应中,氧化剂与还原剂的个数比为
进行化学镀银的反应中,氧化剂与还原剂的个数比为_______ 。
(5)医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的含量,配平以下离子方程式:_______ 。
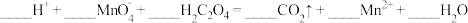
(1)金属加工后的废液中含有2%~5%的
 ,它是一种环境污染物。人们用
,它是一种环境污染物。人们用 溶液来处理此废液,使亚硝酸钠转化为无毒物质。该反应分两步进行:
溶液来处理此废液,使亚硝酸钠转化为无毒物质。该反应分两步进行:第一步:

第二步:
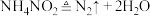
下列对上述反应的叙述中正确的是
①两步均为氧化还原反应 ②第二步
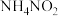 仅发生氧化反应③第二步
仅发生氧化反应③第二步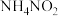 发生了分解反应④第二步中
发生了分解反应④第二步中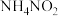 既被氧化又被还原 ⑤第一步为复分解反应
既被氧化又被还原 ⑤第一步为复分解反应A.①③ B.①④ C.②③④ D.③④⑤
(2)实验室中,亚硝酸钠可用来处理过量的叠氮化钠
 ,有关反应的化学方程式如下:
,有关反应的化学方程式如下:a.

b.
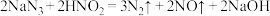
用双线桥法标出b反应中电子转移情况:
(3)磷元素的含氧酸有
 、
、 (亚磷酸)、
(亚磷酸)、 (次磷酸)等多种。其中已知
(次磷酸)等多种。其中已知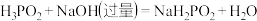 。
。 中磷元素的化合价是
中磷元素的化合价是 属于
属于(4)
 可将溶液中的
可将溶液中的 转化为银,自身变为
转化为银,自身变为 ,可用于化学镀银。利用
,可用于化学镀银。利用 进行化学镀银的反应中,氧化剂与还原剂的个数比为
进行化学镀银的反应中,氧化剂与还原剂的个数比为(5)医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的含量,配平以下离子方程式:
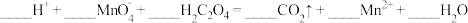
您最近一年使用:0次
【推荐1】在2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O反应中。
(1)_________ 元素被氧化,氧化产物是__________ ;还原产物是___________ ;氧化剂和还原剂的物质的量之比为__________ ;
(2)用双线桥法表示该反应的电子转移情况。___________
(1)
(2)用双线桥法表示该反应的电子转移情况。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)9.03×1023个H2O分子所含氢原子数的物质的量为_______ mol。
(2)28g氮气含有的电子数为_______ mol。
(3)在40g密度为dg/cm3的硫酸铁溶液中,含有2.24gFe3+离子,则此溶液中 的物质的量浓度为
的物质的量浓度为______ mol·L-1 。
(4)用4×10-3 mol的KZO4 恰好将60 mL 0.1 mol·L-1的Na2SO3溶液氧化为Na2SO4,则元素Z在还原产物中的化合价是____ (填写字母)
A.+6 B.+4 C.+3 D.+2
(5)实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓) =5Cl2↑+2MnCl2 +2KCl+8H2O
①用双线桥标出该反应的电子转移方向和数目___ 。
②浓盐酸在反应中显示出来的性质是(填写字母)___ 。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③标准状况下若产生4.48L Cl2,则反应过程中被氧化的HCl的物质的量是____ mol,则电子转移____ mol。
(2)28g氮气含有的电子数为
(3)在40g密度为dg/cm3的硫酸铁溶液中,含有2.24gFe3+离子,则此溶液中
 的物质的量浓度为
的物质的量浓度为(4)用4×10-3 mol的KZO4 恰好将60 mL 0.1 mol·L-1的Na2SO3溶液氧化为Na2SO4,则元素Z在还原产物中的化合价是
A.+6 B.+4 C.+3 D.+2
(5)实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓) =5Cl2↑+2MnCl2 +2KCl+8H2O
①用双线桥标出该反应的电子转移方向和数目
②浓盐酸在反应中显示出来的性质是(填写字母)
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③标准状况下若产生4.48L Cl2,则反应过程中被氧化的HCl的物质的量是
您最近一年使用:0次
【推荐3】医学上常用酸性高锰酸钾溶液和草酸溶液的反应来测定血钙的含量。回答下列问题:
( ) H++( ) MnO4-+( ) H2C2O4→( ) CO2↑+ ( ) Mn2++( ) ____
(1)配平以上离子方程式,并在横线中填上所需的微粒。
(2)该反应中的还原剂是_____________ (填化学式)。
(3)反应转移了0.4 mol电子,则消耗KMnO4的物质的量为_________ mol。
(4)测定血钙含量的方法是:取2.0mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①稀硫酸溶解CaC2O4沉淀的化学方程式是__________________________ 。
②溶解沉淀时______ (填“能”或“不能”)用稀盐酸,原因是________________ 。
③若消耗了1.0×10-4 mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙_____ g。
(5)草酸系统命名为乙二酸,请写出乙二酸的结构简式_____________________ 。
(6)已知:Ka1(H2C2O4)=5.9×10—2,Ka2(H2C2O4)=6.4×10—5;Ka(HF)=3.53×10—4,请写出足量草酸(H2C2O4)与NaF溶液反应的化学方程式:______ 。
(1)配平以上离子方程式,并在横线中填上所需的微粒。
(2)该反应中的还原剂是
(3)反应转移了0.4 mol电子,则消耗KMnO4的物质的量为
(4)测定血钙含量的方法是:取2.0mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①稀硫酸溶解CaC2O4沉淀的化学方程式是
②溶解沉淀时
③若消耗了1.0×10-4 mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙
(5)草酸系统命名为乙二酸,请写出乙二酸的结构简式
(6)已知:Ka1(H2C2O4)=5.9×10—2,Ka2(H2C2O4)=6.4×10—5;Ka(HF)=3.53×10—4,请写出足量草酸(H2C2O4)与NaF溶液反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】有下列三个在溶液中发生的氧化还原反应:
①
②
③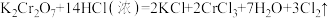
请根据上述反应分析推断后回答下列问题:
(1)对于反应①,氧化剂是___________ ,还原产物是___________ 。
(2)请用双线桥法标出反应③电子转移的方向及数目___________ ,反应中③被氧化和未被氧化的氯原子个数比为___________ 。
(3) 、
、 、
、 、
、 的氧化性由强到弱依次是
的氧化性由强到弱依次是___________ 。
(4) 、
、 在强酸性溶液中能否大量共存?
在强酸性溶液中能否大量共存?___________ (填“能”或“不能”),理由是___________ 。
(5)某同学发现可以用 溶液吸收污染气体
溶液吸收污染气体 。已知该反应体系中包含
。已知该反应体系中包含 、
、 、
、 、
、 、
、 、
、 六种物质,写出该反应的化学方程式
六种物质,写出该反应的化学方程式___________ 。
①

②

③
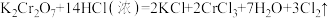
请根据上述反应分析推断后回答下列问题:
(1)对于反应①,氧化剂是
(2)请用双线桥法标出反应③电子转移的方向及数目
(3)
 、
、 、
、 、
、 的氧化性由强到弱依次是
的氧化性由强到弱依次是(4)
 、
、 在强酸性溶液中能否大量共存?
在强酸性溶液中能否大量共存?(5)某同学发现可以用
 溶液吸收污染气体
溶液吸收污染气体 。已知该反应体系中包含
。已知该反应体系中包含 、
、 、
、 、
、 、
、 、
、 六种物质,写出该反应的化学方程式
六种物质,写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)根据下列实验现象或要求写离子方程式(描述现象的,需要写出所有涉及的离子方程式。)
(2)某无色溶液,其中有可能存在的离子如下Na+、Ag+、Ba2+、Al3+、AlO 、S2-、CO
、S2-、CO 、SO
、SO 、SO
、SO ,现取该溶液进行有关实验,实验结果如图所示:
,现取该溶液进行有关实验,实验结果如图所示:

①沉淀甲是___________ ,生成沉淀的离子方程式___________ ;
②沉淀乙是___________ ,由溶液甲生成沉淀乙的离子方程式___________ ;
③沉淀丙是___________ ,设计实验证明___________ ;
④综合上述信息,可以肯定存在的离子有___________ 。
| 实验现象 | 离子方程式 |
| ①澄清石灰水中通入CO2出现白色沉淀,继续通,沉淀溶解。 | |
| ②湿法制备高铁酸钾(K2FeO4)的过程为,在氢氧化铁固体中加入KClO和KOH的混合液。写出该过程的离子方程式并配平。 |
(2)某无色溶液,其中有可能存在的离子如下Na+、Ag+、Ba2+、Al3+、AlO
 、S2-、CO
、S2-、CO 、SO
、SO 、SO
、SO ,现取该溶液进行有关实验,实验结果如图所示:
,现取该溶液进行有关实验,实验结果如图所示:
①沉淀甲是
②沉淀乙是
③沉淀丙是
④综合上述信息,可以肯定存在的离子有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按照要求写出下列相关方程式
(1)写出相应电解质在水中的电离方程式
①碳酸氢钠___________ 。
②硫酸氢钠___________ 。
(2)写出相应离子方程式
①钠与水的反应___________ 。
②过氧化钠与水的反应___________ 。
③已知氧化性: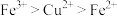 ,将足量Cu投入至FeCl3溶液中
,将足量Cu投入至FeCl3溶液中___________
④向Ba(OH)2溶液中滴加NaHSO4溶液至Ba2+沉淀完全___________ 。继续向上述溶液中滴加NaHSO4溶液至过量___________
⑤已知还原性: ,向FeBr2溶液中通入少量Cl2
,向FeBr2溶液中通入少量Cl2___________ ;向FeI2溶液中通入和Fe2+等数目的Cl2___________ 。
(3)写出相应化学方程式
①钠在空气中加热___________ 。
②制备氢氧化铁胶体的反应___________ 。
(4)用双线桥法表示下列反应的电子转移方向和数目___________ 。
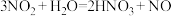
(5)用单线桥法表示下列反应的电子转移方向和数目___________ 。

(6)配平下列方程式
①超氧化钾(KO2)与水的反应:___________ 。
___________KO2+___________H2O→___________KOH+___________O2↑+___________H2O2
②___________ 。
___________ +___________ClO-→N2↑+Cl-+___________+___________
+___________ClO-→N2↑+Cl-+___________+___________
(1)写出相应电解质在水中的电离方程式
①碳酸氢钠
②硫酸氢钠
(2)写出相应离子方程式
①钠与水的反应
②过氧化钠与水的反应
③已知氧化性:
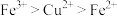 ,将足量Cu投入至FeCl3溶液中
,将足量Cu投入至FeCl3溶液中④向Ba(OH)2溶液中滴加NaHSO4溶液至Ba2+沉淀完全
⑤已知还原性:
 ,向FeBr2溶液中通入少量Cl2
,向FeBr2溶液中通入少量Cl2(3)写出相应化学方程式
①钠在空气中加热
②制备氢氧化铁胶体的反应
(4)用双线桥法表示下列反应的电子转移方向和数目
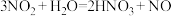
(5)用单线桥法表示下列反应的电子转移方向和数目

(6)配平下列方程式
①超氧化钾(KO2)与水的反应:
___________KO2+___________H2O→___________KOH+___________O2↑+___________H2O2
②
___________
 +___________ClO-→N2↑+Cl-+___________+___________
+___________ClO-→N2↑+Cl-+___________+___________
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化还原反应在生产、生活中具有广泛的用途。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是_____ (选填编号)。
a. 海水提溴 b. 工业制氯碱 c. 海水晒盐 d. 海带提碘
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关”可用下图表示。
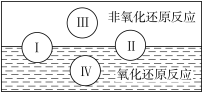
试写出有水参加且符合反应类型 IV 的一个化学方程式:___________________ 。
(3)工业上利用 NaIO3和 NaHSO3反应来制取单质 I2。
①配平下列化学方程式并标明电子转移的方向和数目:
_____ NaIO3+ NaHSO3→ I2+ Na2SO4+ H2SO4+ H2O
②该反应还原剂是_____ ,_____ 元素被还原,若生成 1mol 氧化产物则转移电子数目为_____ NA。
(4)已知:HSO3-、I2、I-、SO42-和一些未知物组成的一个氧化还原反应,其中SO42-是氧化产物,该反应中还原性HSO3-_____ I-(填“>”或“<”),完成该反应_____________________________________ 。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是
a. 海水提溴 b. 工业制氯碱 c. 海水晒盐 d. 海带提碘
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关”可用下图表示。

试写出有水参加且符合反应类型 IV 的一个化学方程式:
(3)工业上利用 NaIO3和 NaHSO3反应来制取单质 I2。
①配平下列化学方程式并标明电子转移的方向和数目:
②该反应还原剂是
(4)已知:HSO3-、I2、I-、SO42-和一些未知物组成的一个氧化还原反应,其中SO42-是氧化产物,该反应中还原性HSO3-
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:

(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有___ (填化学式)。
(2)将X与Y混合,可生成淡黄色固体,该反应中还原剂与氧化剂的物质的量之比为___ 。
(3)检验物质Y的方法是___ 。
(4)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为___ 。
(5)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是___ (填代号)。
a.Na2S+S b.SO2+Na2SO4 c.Na2SO3+S d.Na2SO3+Na2SO4 e.SO2+ Na2S2+Na2CO3
(6)已知Na2SO3能被K2Cr2O7氧化为Na2SO4则24mL0.05 mol·L-1的Na2SO3溶液与20mL0.02mol·L-1的K2Cr2O7溶液恰好完全反应时,Cr元素在还原产物中的化合价为___ 。

(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
(2)将X与Y混合,可生成淡黄色固体,该反应中还原剂与氧化剂的物质的量之比为
(3)检验物质Y的方法是
(4)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为
(5)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是
a.Na2S+S b.SO2+Na2SO4 c.Na2SO3+S d.Na2SO3+Na2SO4 e.SO2+ Na2S2+Na2CO3
(6)已知Na2SO3能被K2Cr2O7氧化为Na2SO4则24mL0.05 mol·L-1的Na2SO3溶液与20mL0.02mol·L-1的K2Cr2O7溶液恰好完全反应时,Cr元素在还原产物中的化合价为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮氧化物、二氧化硫能引发酸雨、雾霾等。回答下列问题:
(1)NO2产生硝酸型酸雨的化学方程式为____________________ 。
(2)汽车尾气催化转化器可将尾气中的CO、NO均转化为无害气体,该反应的还原产物为______ 。
(3)目前工业上烟气脱硫脱硝的工艺流程如下:
①“催化氧化”的目的是____________________ 。
②图中产品中含硫成分为______ (填化学式)。
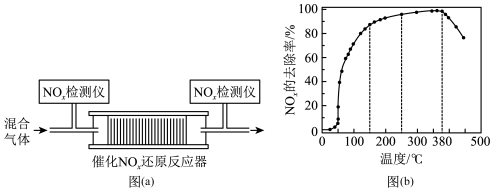
(4)为探究某种催化剂在有氧条件下用NH3还原NOx的最佳温度,将一定比例的O2、NH3和NOx混合,以一定的流速通过催化NOx还原反应器[如图(a)],反应相同时间后测得NOx的去除率随反应温度的变化曲线如图(b)所示。______________ 。
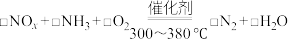
②当反应温度高于380℃时,NOx的去除率迅速下降的原因可能是____________________ 。
(1)NO2产生硝酸型酸雨的化学方程式为
(2)汽车尾气催化转化器可将尾气中的CO、NO均转化为无害气体,该反应的还原产物为
(3)目前工业上烟气脱硫脱硝的工艺流程如下:

①“催化氧化”的目的是
②图中产品中含硫成分为
(4)为探究某种催化剂在有氧条件下用NH3还原NOx的最佳温度,将一定比例的O2、NH3和NOx混合,以一定的流速通过催化NOx还原反应器[如图(a)],反应相同时间后测得NOx的去除率随反应温度的变化曲线如图(b)所示。
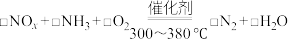
②当反应温度高于380℃时,NOx的去除率迅速下降的原因可能是
您最近一年使用:0次

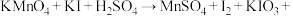 ___________
___________ 。
。 和
和 的化学计量数都是5。补全下面的化学方程式并用单线桥法标出电子转移的方向和数目
的化学计量数都是5。补全下面的化学方程式并用单线桥法标出电子转移的方向和数目 ___________
___________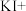 ___________
___________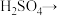 ___________
___________ ___________
___________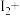 ___________
___________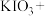 ___________
___________ ___________
___________

