是重要化工原料,由
是重要化工原料,由 制备
制备 一种工艺流程如下:
一种工艺流程如下:I.研磨
 ,加水配成浊液。
,加水配成浊液。II.
 浊液经还原、纯化、制备等过程,最终获得
浊液经还原、纯化、制备等过程,最终获得 固体。
固体。
资料:
①
 不溶于水。该工艺条件下,
不溶于水。该工艺条件下, 与
与 不反应。
不反应。②难溶电解质的溶度积:
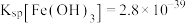 ,
,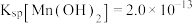
(1)研磨
 的目的是
的目的是(2)
 氧化
氧化 为
为 的离子方程式为
的离子方程式为①根据上述反应,还原
 所需的
所需的 与
与 的物质的量比值应为2。而实际上加入的酸要少一些,请结合含铁产物解释原因
的物质的量比值应为2。而实际上加入的酸要少一些,请结合含铁产物解释原因②取少量母液,滴加
 。
。(3)纯化
向母液中滴加氨水调pH,除去残留的
 。若母液中
。若母液中 ,使
,使 恰好沉淀完全即溶液中
恰好沉淀完全即溶液中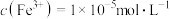 ,溶液中
,溶液中 至少为
至少为 ,则溶液中
,则溶液中 ,沉淀生成。(已知
,沉淀生成。(已知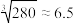 )。
)。(4)制备
将
 纯化液与稍过量的
纯化液与稍过量的 ,溶液混合,得到含
,溶液混合,得到含 的浊液。将浊液过滤,洗涤沉淀,干燥后得到
的浊液。将浊液过滤,洗涤沉淀,干燥后得到 固体。
固体。①通过检验
 来判断沉淀是否洗涤干净。检验
来判断沉淀是否洗涤干净。检验 的操作是取最后一次洗涤液,
的操作是取最后一次洗涤液,②生成
 的离子方程式是
的离子方程式是
更新时间:2022-11-24 23:06:02
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。
某化学研究小组采用下图装置(实验前已除尽装置内的空气)制取Na2S2O5,装置II中有Na2S2O5晶体析出,发生的反应为:Na2SO3+SO2=Na2S2O5
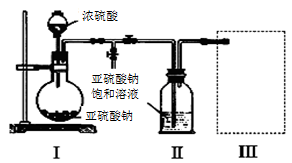
(1)装置I中产生气体的化学方程式为____________________________ 。
(2)要从装置II中获得已析出的晶体,需要用到的玻璃仪器有_______________ 。
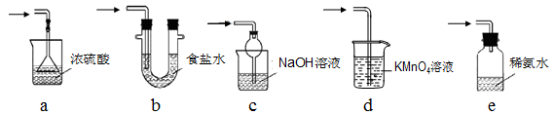
装置III用于处理尾气,可选用的合理装置(夹持仪器已略去)为_____________ (填序号)。
现将0.5mol Na2S2O5溶解于水配成1L溶液,该溶液pH=4.5。溶液中部分微粒浓度随溶液酸碱性变化如图。
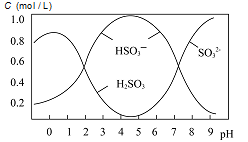
(3)写出Na2S2O5溶解于水的化学方程式________________________ ;当溶液pH小于1后,溶液中H2SO3的浓度减小,其原因可能是_____________________ 。
(4)葡萄酒常用Na2S2O5做抗氧化剂。1.90g Na2S2O5最多能还原________ mLO2(标准状况)。
(5)检验Na2S2O5晶体在空气中已被氧化的实验方案是_____________________ 。
某化学研究小组采用下图装置(实验前已除尽装置内的空气)制取Na2S2O5,装置II中有Na2S2O5晶体析出,发生的反应为:Na2SO3+SO2=Na2S2O5

(1)装置I中产生气体的化学方程式为
(2)要从装置II中获得已析出的晶体,需要用到的玻璃仪器有
装置III用于处理尾气,可选用的合理装置(夹持仪器已略去)为

现将0.5mol Na2S2O5溶解于水配成1L溶液,该溶液pH=4.5。溶液中部分微粒浓度随溶液酸碱性变化如图。

(3)写出Na2S2O5溶解于水的化学方程式
(4)葡萄酒常用Na2S2O5做抗氧化剂。1.90g Na2S2O5最多能还原
(5)检验Na2S2O5晶体在空气中已被氧化的实验方案是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】亚氯酸钠NaClO2是一种高效氧化剂和优质漂白剂。一种以氯酸钠NaClO3为原料制备NaClO2粗品的工艺流程如图所示:

(1)NaClO2中氯元素的化合价为_______ 。
(2)试剂A可以选择_______ (填字母)。
a. SO2 b. 浓硝酸 c. 酸性高锰酸钾溶液
(3)反应Ⅱ的离子方程式为_______ ,该反应的氧化剂为_______ ,被氧化的元素为_______ ,还原产物为_______ 。
(4)与传统消毒剂Cl2,相比NaClO2的消毒能力是Cl2的_______ 倍。(提示:以单位质量得电子数表示,还原产物为Cl-,计算结果保留一位小数)
(5)中间产物二氧化氯(ClO2)是一种高效、低毒的消毒剂,某同学在实验室中探究ClO2与Na2S的反应。

将适量稀释后的ClO2通入如图装置中充分反应,得到无色澄清溶液。取少量I中溶液于试管中,加入盐酸酸化的BaCl2溶液,振荡,出现白色沉淀,证明有_______ 离子生成。请设计实验验证I中溶液有Cl-生成_______ 。

(1)NaClO2中氯元素的化合价为
(2)试剂A可以选择
a. SO2 b. 浓硝酸 c. 酸性高锰酸钾溶液
(3)反应Ⅱ的离子方程式为
(4)与传统消毒剂Cl2,相比NaClO2的消毒能力是Cl2的
(5)中间产物二氧化氯(ClO2)是一种高效、低毒的消毒剂,某同学在实验室中探究ClO2与Na2S的反应。

将适量稀释后的ClO2通入如图装置中充分反应,得到无色澄清溶液。取少量I中溶液于试管中,加入盐酸酸化的BaCl2溶液,振荡,出现白色沉淀,证明有
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
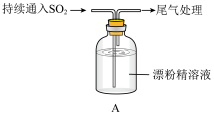
【推荐3】某学生对 与漂粉精的反应进行实验探究:
与漂粉精的反应进行实验探究:
(1)pH试纸颜色的变化说明漂粉精溶液具有的性质是______ 。
(2)向水中持续通入 ,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:
,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用硝酸酸化的 溶液检验白雾,产生白色沉淀。
溶液检验白雾,产生白色沉淀。
①实验a目的是______ 。
②由实验a、b不能判断白雾中含有HCl,理由是______ 。
(3)现象ⅱ中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和 发生反应。通过进一步实验确认了这种可能性,其实验方案是
发生反应。通过进一步实验确认了这种可能性,其实验方案是______ 。
(4)将A瓶中混合物过滤、洗涤,得到沉淀X。
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入 溶液,产生白色沉淀。则沉淀X中含有的物质是
溶液,产生白色沉淀。则沉淀X中含有的物质是______ 。
②用离子方程式解释现象ⅲ中黄绿色褪去的原因:______ 。
 与漂粉精的反应进行实验探究:
与漂粉精的反应进行实验探究:操作 | 现象 |
| 取4g漂粉精固体,加入100mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
| ⅰ.液面上方出现白雾; ⅱ.稍后,出现浑浊,溶液变为黄绿色; ⅲ.稍后,产生大量白色沉淀,黄绿色褪去 |
(2)向水中持续通入
 ,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:
,未观察到白雾。推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用硝酸酸化的
 溶液检验白雾,产生白色沉淀。
溶液检验白雾,产生白色沉淀。①实验a目的是
②由实验a、b不能判断白雾中含有HCl,理由是
(3)现象ⅱ中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和
 发生反应。通过进一步实验确认了这种可能性,其实验方案是
发生反应。通过进一步实验确认了这种可能性,其实验方案是(4)将A瓶中混合物过滤、洗涤,得到沉淀X。
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入
 溶液,产生白色沉淀。则沉淀X中含有的物质是
溶液,产生白色沉淀。则沉淀X中含有的物质是②用离子方程式解释现象ⅲ中黄绿色褪去的原因:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】以下是25 ℃时几种难溶电解质的溶度积:
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些杂质离子。例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可。
请回答下列问题:
(1)上述三个除杂方案都能够达到很好效果,Fe3+、Fe2+都被转化为_____________ (填化学式)而除去。
(2)①中加入的试剂应该选择___________ 为宜,其原因是_____________________ 。
(3)②中除去Fe3+所发生的总反应的离子方程式为________ 。
(4)下列与③相关的叙述中,正确的是________ (填字母)。
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质,不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜
D.在pH>4的溶液中Fe3+一定不能大量存在
| 难溶电解质 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶度积 | 1.8×10-11 | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可。
请回答下列问题:
(1)上述三个除杂方案都能够达到很好效果,Fe3+、Fe2+都被转化为
(2)①中加入的试剂应该选择
(3)②中除去Fe3+所发生的总反应的离子方程式为
(4)下列与③相关的叙述中,正确的是
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质,不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜
D.在pH>4的溶液中Fe3+一定不能大量存在
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】碳酸钴(CoCO3)是一种红色粉末,主要用作催化剂、选矿剂和陶瓷釉。以含钴废料 (主要成分为CoO、Co2O3还含少量Al2O3、Zn等杂质)为原料制备CoCO3的一种工艺如下:
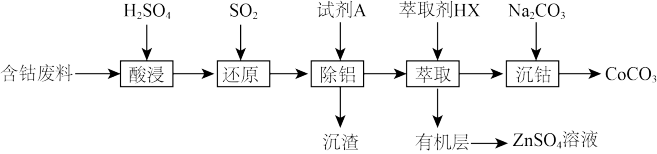
回答下列问题:
(1)“酸浸”前常将含钴废料粉碎,其主要目的是_______ 。
(2)“还原”过程中还原8.3kgCo2O3理论上需消耗SO2的体积为_______ L(标准状况)。
(3)已知“萃取” 的原理为
的原理为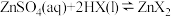 (有机层)
(有机层)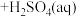 ,从有机层中获得
,从有机层中获得 溶液的操作是加入
溶液的操作是加入__ (填试剂名称),其作用是___ (从平衡移动原理角度分析)。

回答下列问题:
(1)“酸浸”前常将含钴废料粉碎,其主要目的是
(2)“还原”过程中还原8.3kgCo2O3理论上需消耗SO2的体积为
(3)已知“萃取”
 的原理为
的原理为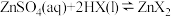 (有机层)
(有机层)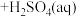 ,从有机层中获得
,从有机层中获得 溶液的操作是加入
溶液的操作是加入
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】碳酸锂广泛应用于陶瓷和医药等领域。以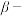 锂辉石(主要成分为
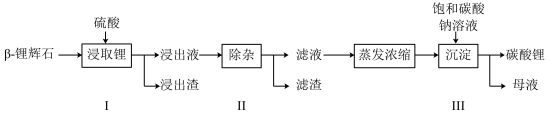
锂辉石(主要成分为 )为原材料制备Li2CO3的工艺流程如下:
)为原材料制备Li2CO3的工艺流程如下:
已知:Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH如下表。
(1)步骤Ⅰ前,β-锂辉石要粉碎成细颗粒的目的是______ 。步骤Ⅰ中,酸浸后得到的酸性浊液中含有Li+、 ,另含有Al3+、Fe3+、Fe2+、Mg2+、Ca2+、Na+等杂质,需在搅拌下加入石灰石调节溶液的pH到6沉淀部分杂质离子,然后分离得到浸出液。浸出渣的主要成分是
,另含有Al3+、Fe3+、Fe2+、Mg2+、Ca2+、Na+等杂质,需在搅拌下加入石灰石调节溶液的pH到6沉淀部分杂质离子,然后分离得到浸出液。浸出渣的主要成分是______ (填写化学式)。
(2)①步骤Ⅱ中,将适量的H2O2溶液、石灰乳和Na2CO3溶液依次加入浸出液中,可除去的杂质金属离子有______ 。
②下列说法正确的是______ 。
A.步骤Ⅰ的浸出液需冷却后再加入H2O2溶液
B.考虑工业生产成本,步骤Ⅱ中石灰乳更换成烧碱更佳
C.步骤Ⅲ母液中只有Na2SO4和NaOH
D.可通过离子交换膜法电解母液回收利用NaOH
(3)在实验室模拟工业生产中的蒸发浓缩操作,需要用到的硅酸盐仪器有______ 。
(4)步骤Ⅲ中得到的Li2CO3固体需要清洗,简述检验Li2CO3已被清洗干净的操作______ 。
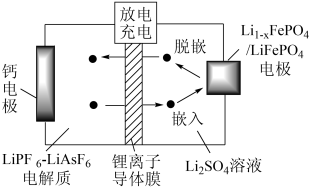
(5)工业上FePO4与Li2CO3在高温条件下与H2C2O4煅烧可得LiFePO4,其常用作锂离子电池电极材料,如图为Ca-LiFePO4可充电电池的工作原理示意图,锂离子导体膜只允许Li+通过。充电时,钙电极为______ (“阳极”或“阴极”),放电时,电极上发生Li+的嵌入的电极反应是______ 。
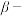 锂辉石(主要成分为
锂辉石(主要成分为 )为原材料制备Li2CO3的工艺流程如下:
)为原材料制备Li2CO3的工艺流程如下:
已知:Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH如下表。
| 沉淀物 |  |  |  |  |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
 ,另含有Al3+、Fe3+、Fe2+、Mg2+、Ca2+、Na+等杂质,需在搅拌下加入石灰石调节溶液的pH到6沉淀部分杂质离子,然后分离得到浸出液。浸出渣的主要成分是
,另含有Al3+、Fe3+、Fe2+、Mg2+、Ca2+、Na+等杂质,需在搅拌下加入石灰石调节溶液的pH到6沉淀部分杂质离子,然后分离得到浸出液。浸出渣的主要成分是(2)①步骤Ⅱ中,将适量的H2O2溶液、石灰乳和Na2CO3溶液依次加入浸出液中,可除去的杂质金属离子有
②下列说法正确的是
A.步骤Ⅰ的浸出液需冷却后再加入H2O2溶液
B.考虑工业生产成本,步骤Ⅱ中石灰乳更换成烧碱更佳
C.步骤Ⅲ母液中只有Na2SO4和NaOH
D.可通过离子交换膜法电解母液回收利用NaOH
(3)在实验室模拟工业生产中的蒸发浓缩操作,需要用到的硅酸盐仪器有
(4)步骤Ⅲ中得到的Li2CO3固体需要清洗,简述检验Li2CO3已被清洗干净的操作
(5)工业上FePO4与Li2CO3在高温条件下与H2C2O4煅烧可得LiFePO4,其常用作锂离子电池电极材料,如图为Ca-LiFePO4可充电电池的工作原理示意图,锂离子导体膜只允许Li+通过。充电时,钙电极为

您最近半年使用:0次