请运用所学知识判断,向1 mL0.1 mol/LAgNO3溶液中依次滴加1 mL0.1 mol/L的NaCl、NaBr、KI溶液时,会发生什么变化________ 。
更新时间:2022-11-26 17:22:16
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】利用所学化学反应原理,解决以下问题:
(1)KAl (SO4)2·12H2O可做净水剂,其原理是
(SO4)2·12H2O可做净水剂,其原理是____________________________________ (用离子方程式表示)
(2)碳酸氢钠溶液蒸干并灼烧得到的固体物质是__________ (填化学式)
(3)向FeCl3溶液中滴加NaHCO3溶液,有沉淀和气体生成的离子方程式_____________
(4)将AgCl分别放入①5mLH2O ②10mL0.2mol·L-1MgCl2溶液 ③20mL0.5mol·L-1NaCl溶液④40mL0.1mol·L-1HCl溶液中溶解至饱和,各溶液中Ag+的浓度由大到小的顺序是________________________ (用序号填空)
(5)常温下amol/L CH3COOH稀溶液和bmol/LKOH稀溶液等体积混合:若c(K+)<c(CH3COO-),则a
CH3COOH稀溶液和bmol/LKOH稀溶液等体积混合:若c(K+)<c(CH3COO-),则a_____________ b(填>、<、=),室温下,1mol/L相同体积的下列四种溶液:①KCl②FeCl3③HF④Na2CO3中,所含阳离子数由少到多的顺序是_________________________ (用序号填空)
(1)KAl
 (SO4)2·12H2O可做净水剂,其原理是
(SO4)2·12H2O可做净水剂,其原理是(2)碳酸氢钠溶液蒸干并灼烧得到的固体物质是
(3)向FeCl3溶液中滴加NaHCO3溶液,有沉淀和气体生成的离子方程式
(4)将AgCl分别放入①5mLH2O ②10mL0.2mol·L-1MgCl2溶液 ③20mL0.5mol·L-1NaCl溶液④40mL0.1mol·L-1HCl溶液中溶解至饱和,各溶液中Ag+的浓度由大到小的顺序是
(5)常温下amol/L
 CH3COOH稀溶液和bmol/LKOH稀溶液等体积混合:若c(K+)<c(CH3COO-),则a
CH3COOH稀溶液和bmol/LKOH稀溶液等体积混合:若c(K+)<c(CH3COO-),则a
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。
(1)在25℃时,将c mol·L-1的醋酸溶液与0.02 mol·L-1 NaOH溶液等体积混合后溶液刚好呈中性,用含c的代数式表示CH3COOH的电离常数Ka=________ 。
(2)25℃时,H2SO3 HSO3-+H+的电离常数Ka=1×10-2 mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kb=
HSO3-+H+的电离常数Ka=1×10-2 mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kb=________ mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中 将
将________ (填“增大”、“减小”或“不变”)。
(3)已知H2A在水中存在以下平衡:H2A=H++HA-,HA- H++A2-。常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s)
H++A2-。常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s) Ca2+(aq)+A2-(aq) △H>0。若要使该溶液中Ca2+浓度变小,可采取的措施有
Ca2+(aq)+A2-(aq) △H>0。若要使该溶液中Ca2+浓度变小,可采取的措施有________ 。
A.升高温度 B.降低温度 C.加入NH4Cl晶体 D.加入Na2A固体
(1)在25℃时,将c mol·L-1的醋酸溶液与0.02 mol·L-1 NaOH溶液等体积混合后溶液刚好呈中性,用含c的代数式表示CH3COOH的电离常数Ka=
(2)25℃时,H2SO3
 HSO3-+H+的电离常数Ka=1×10-2 mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kb=
HSO3-+H+的电离常数Ka=1×10-2 mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kb= 将
将(3)已知H2A在水中存在以下平衡:H2A=H++HA-,HA-
 H++A2-。常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s)
H++A2-。常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s) Ca2+(aq)+A2-(aq) △H>0。若要使该溶液中Ca2+浓度变小,可采取的措施有
Ca2+(aq)+A2-(aq) △H>0。若要使该溶液中Ca2+浓度变小,可采取的措施有A.升高温度 B.降低温度 C.加入NH4Cl晶体 D.加入Na2A固体
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I .(1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈___________ (填“酸性”,“中性”或“碱性”),溶液中c(Na+)___________ c(CH3COO-)(填“>”或“=”或“<”)。
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈___________ (填“酸性”,“中性”或“碱性”),溶液中c(Na+)___________ c(CH3COO-)(填“>”或“=”或“<”)。
(3)盐类水解的本质是___________ 水的电离,(填促进,抑制)。升高温度___________ 盐类的水解。(填促进,抑制)
(4)弱电解质的电离常数只受___________ 影响,升温电离常数___________ (填增大,减小或不变)
II.已知H2A在水中存在以下平衡: ,
, 
(1)常温下, 溶液的pH
溶液的pH___________ (填字母序号),原因是___________ (填离子方程式)。
A.大于7 B.小于7 C.等于7 D.无法确定
(2)常温下,若向0.1mol·L-1的H2A溶液中逐滴滴加0.1mol·L-1 NaOH溶液至溶液呈中性。此时该混合溶液中的下列关系一定正确的是___________ (填字母序号)。
A.c(H+ ). c(OH-)= 1.0×10-14 B.
C.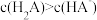 D.
D.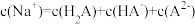
(3)常温下, 的饱和溶液中存在以下平衡:
的饱和溶液中存在以下平衡: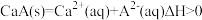 ,若要使该溶液中
,若要使该溶液中 浓度增大,可采取的措施有
浓度增大,可采取的措施有___________ (填字母序号)。
A.升高温度 B.降低温度 C.加入少量蒸馏水 D.加入 固体
固体
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈
(3)盐类水解的本质是
(4)弱电解质的电离常数只受
II.已知H2A在水中存在以下平衡:
 ,
, 
(1)常温下,
 溶液的pH
溶液的pHA.大于7 B.小于7 C.等于7 D.无法确定
(2)常温下,若向0.1mol·L-1的H2A溶液中逐滴滴加0.1mol·L-1 NaOH溶液至溶液呈中性。此时该混合溶液中的下列关系一定正确的是
A.c(H+ ). c(OH-)= 1.0×10-14 B.

C.
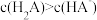 D.
D.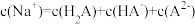
(3)常温下,
 的饱和溶液中存在以下平衡:
的饱和溶液中存在以下平衡: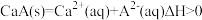 ,若要使该溶液中
,若要使该溶液中 浓度增大,可采取的措施有
浓度增大,可采取的措施有A.升高温度 B.降低温度 C.加入少量蒸馏水 D.加入
 固体
固体
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】铁及其化合物是生活中常见的物质。
(1)铁件表面镀铜可有效防止铁被腐蚀,电镀时,以CuSO4溶液为电解液,铜作_______ (填 “阳”或“阴”)极,铜离子向_______ 极移动,阴极的电极反应式为_______ 。
(2)下图中,为了减缓海水对铁闸门A的腐蚀,材料B可以选择_______ (填字母序号)。
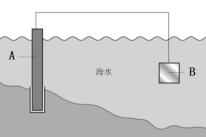
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因:_______ 。
(3)将FeCl3溶液滴加到Mg(OH)2悬浊液中,有红褐色沉淀产生。该变化的离子方程式为_______ 。
(1)铁件表面镀铜可有效防止铁被腐蚀,电镀时,以CuSO4溶液为电解液,铜作
(2)下图中,为了减缓海水对铁闸门A的腐蚀,材料B可以选择

a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因:
(3)将FeCl3溶液滴加到Mg(OH)2悬浊液中,有红褐色沉淀产生。该变化的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】钼酸钠晶体(Na2MoO4·2H2O)是一种金属腐蚀抑制剂。如图是利用钼精矿(主要成分是MoS2,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。
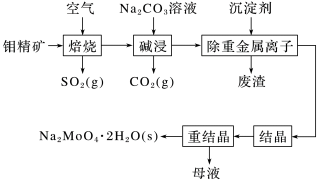
“结晶”前需向滤液中加入Ba(OH)2固体以除去 。若滤液中c(MoO
。若滤液中c(MoO )=0.40mol·L-1,c(
)=0.40mol·L-1,c( )=0.10mol/L,当BaMoO4开始沉淀时,
)=0.10mol/L,当BaMoO4开始沉淀时, 的去除率是
的去除率是___________ %[已知:Ksp(BaCO3)=1.0×10-9,Ksp(BaMoO4)=4.0×10-8,溶液体积变化忽略不计]。

“结晶”前需向滤液中加入Ba(OH)2固体以除去
 。若滤液中c(MoO
。若滤液中c(MoO )=0.40mol·L-1,c(
)=0.40mol·L-1,c( )=0.10mol/L,当BaMoO4开始沉淀时,
)=0.10mol/L,当BaMoO4开始沉淀时, 的去除率是
的去除率是
您最近一年使用:0次
【推荐3】已知难溶电解质在水溶液中存在溶解平衡MmAn(s) mMn+(aq)+nAm-(aq),Ksp=cm(Mn+)·cn(Am-)称为溶度积。
mMn+(aq)+nAm-(aq),Ksp=cm(Mn+)·cn(Am-)称为溶度积。
某学习小组欲探究CaSO4沉淀转化为CaCO3沉淀的可能性,查得如下资料(25℃):
他们的实验步骤如下:
①往100mL0.1mol·L-1的CaCl2溶液中加入0.1mol·L-1的Na2SO4溶液100mL立即有白色沉淀生成。
②向上述悬浊液中加入固体Na2CO33g,搅拌,静置后弃去上层清液。
③再加入蒸馏水搅拌,静置后再弃去上层清液。
④___________________________。
(1)由题中信息知Ksp越大,表示电解质的溶解度越__ (填“大”或“小”)。
(2)写出第②步发生反应的化学方程式__ 。
(3)设计第③步的目的是什么__ 。
(4)请补充第④步操作及发生的现象__ 。
(5)请写出该转化在实际生活、生产中的一个应用__ 。
 mMn+(aq)+nAm-(aq),Ksp=cm(Mn+)·cn(Am-)称为溶度积。
mMn+(aq)+nAm-(aq),Ksp=cm(Mn+)·cn(Am-)称为溶度积。某学习小组欲探究CaSO4沉淀转化为CaCO3沉淀的可能性,查得如下资料(25℃):
| 难浴电解质 | CaCO3 | CaSO4 | MgCO3 | Mg(OH)2 |
| Ksp | 2.8×10-9 | 9.1×10-6 | 6.8×10-6 | 1.8×10-11 |
他们的实验步骤如下:
①往100mL0.1mol·L-1的CaCl2溶液中加入0.1mol·L-1的Na2SO4溶液100mL立即有白色沉淀生成。
②向上述悬浊液中加入固体Na2CO33g,搅拌,静置后弃去上层清液。
③再加入蒸馏水搅拌,静置后再弃去上层清液。
④___________________________。
(1)由题中信息知Ksp越大,表示电解质的溶解度越
(2)写出第②步发生反应的化学方程式
(3)设计第③步的目的是什么
(4)请补充第④步操作及发生的现象
(5)请写出该转化在实际生活、生产中的一个应用
您最近一年使用:0次



