工业上采用电解的方法来制备活泼金属铝。纯净的氧化铝熔点很高(约为2045℃),在实际生产中,通过加入助熔剂冰晶石( )在1000℃左右就可得到熔融体。
)在1000℃左右就可得到熔融体。

主要的电极反应为:
阴极: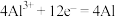
阳极:
总反应为:
在阳极生成的氧气全部与石墨电极反应生成一氧化碳气体和二氧化碳气体,因此在电解过程中,需要不断补充石墨电极,则:
(1)生产1t金属铝,转移电子的物质的量是___________ 。
(2)工业生产中,生产1t铝阳极损失0.6t石墨。石墨被氧化的产物是____ ,质量为______ 。
 )在1000℃左右就可得到熔融体。
)在1000℃左右就可得到熔融体。
主要的电极反应为:
阴极:
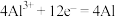
阳极:

总反应为:

在阳极生成的氧气全部与石墨电极反应生成一氧化碳气体和二氧化碳气体,因此在电解过程中,需要不断补充石墨电极,则:
(1)生产1t金属铝,转移电子的物质的量是
(2)工业生产中,生产1t铝阳极损失0.6t石墨。石墨被氧化的产物是
更新时间:2022-11-26 16:55:45
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】已知As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O。
(1)请用双线桥法标出电子转移的方向和数目______ 。
(2)Zn在上述反应中显示出来的性质是______ (填序号)。
A.氧化性 B.还原性 C.酸性 D.碱性
(3)该反应的氧化产物和还原产物的物质的量之比为______ 。
(4)若消耗0.3molAs2O3,则转移的电子数为______ 。
(5)写出该反应的离子方程式:______ 。
(1)请用双线桥法标出电子转移的方向和数目
(2)Zn在上述反应中显示出来的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
(3)该反应的氧化产物和还原产物的物质的量之比为
(4)若消耗0.3molAs2O3,则转移的电子数为
(5)写出该反应的离子方程式:
您最近一年使用:0次
【推荐2】按要求完成下列填空:
(1)某种粒子有1个原子核,核内有17个质子,20个中子,核外有 18个电子,写出该粒子的化学符号________ ,结构示意图____________ 。
(2)将NaHSO₄溶于水,破坏了 NaHSO₄中的_________ ,写出其电离方程式:_______________ 。
(3)19g某二价金属的氯化物 ACl₂中含有0.4molCl⁻,金属A的相对原子质量是________ 。
(4)根据反应 ,可知当有
,可知当有  参加反应时,被氧化的硫元素的物质的量为
参加反应时,被氧化的硫元素的物质的量为_______ mol,转移电子的物质的量为______ mol。
(1)某种粒子有1个原子核,核内有17个质子,20个中子,核外有 18个电子,写出该粒子的化学符号
(2)将NaHSO₄溶于水,破坏了 NaHSO₄中的
(3)19g某二价金属的氯化物 ACl₂中含有0.4molCl⁻,金属A的相对原子质量是
(4)根据反应
 ,可知当有
,可知当有  参加反应时,被氧化的硫元素的物质的量为
参加反应时,被氧化的硫元素的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】按要求填空。
(1)3.01 ×1023个 CH4分子的物质的量是_______ ,在标准状况下的体积为_______ 。
(2)某物质X的质量为6.4g,含有6.02 ×1022个分子,则X的摩尔质量为_______
(3)配平方程式:_______Cu+_______HNO3=_______Cu(NO3)2+_______NO↑+_______H2O
______
(4)书写钠与水反应的离子方程式:_______
(5)在一定条件下, RO 和Cl2可发生如下反应: RO
和Cl2可发生如下反应: RO +Cl2+2OH-=RO
+Cl2+2OH-=RO +2Cl-+H2O, 由以上反应可知在上述过程中RO
+2Cl-+H2O, 由以上反应可知在上述过程中RO 被
被_______ (填“氧化”或“还原”) RO 中元素R的化合价是
中元素R的化合价是_______ 。
(1)3.01 ×1023个 CH4分子的物质的量是
(2)某物质X的质量为6.4g,含有6.02 ×1022个分子,则X的摩尔质量为
(3)配平方程式:_______Cu+_______HNO3=_______Cu(NO3)2+_______NO↑+_______H2O
(4)书写钠与水反应的离子方程式:
(5)在一定条件下, RO
 和Cl2可发生如下反应: RO
和Cl2可发生如下反应: RO +Cl2+2OH-=RO
+Cl2+2OH-=RO +2Cl-+H2O, 由以上反应可知在上述过程中RO
+2Cl-+H2O, 由以上反应可知在上述过程中RO 被
被 中元素R的化合价是
中元素R的化合价是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】铜和铁是常见金属。但生铁易生锈,请讨论电化学实验中有关铁的性质

(1)①已知甲总反应为Fe+2HCl=FeCl2+H2↑,右电极产生H2则甲池中右电极材料为_____ ,左电极材料为_____ 。(填“Fe”或“C”)
②乙中的电解质为硫酸酸化的CuSO4溶液,现用来电解精炼铜,则左电极材料为_____ 。(填“粗铜”或“纯铜”)
③装置丙中,易生锈的是_____ (填“a”或“b”)点,发生_____ (填“析氢”或“吸氧”)腐蚀,其正极反应式为_____ 。
(2)下图为保护钢闸门的两种方法,根据所学知识完成下列填空:

①利用原电池原理保护钢闸门的是_____ (填“丁”或“戊”),在此过程中_____ (填“Fe”“Zn”或“辅助阳极”)失电子。
②戊装置中通电后,电子流向_____ (填“钢闸门”或“辅助阳极”)

(1)①已知甲总反应为Fe+2HCl=FeCl2+H2↑,右电极产生H2则甲池中右电极材料为
②乙中的电解质为硫酸酸化的CuSO4溶液,现用来电解精炼铜,则左电极材料为
③装置丙中,易生锈的是
(2)下图为保护钢闸门的两种方法,根据所学知识完成下列填空:

①利用原电池原理保护钢闸门的是
②戊装置中通电后,电子流向
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
氯气是制备系列含氯化合物的主要原料,可采用如图(a)所示的装置来制取。装置中的离子膜只允许___________ 离子通过,氯气的逸出口是___________ (填标号)。

氯气是制备系列含氯化合物的主要原料,可采用如图(a)所示的装置来制取。装置中的离子膜只允许

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】电化学方法是化工生产中常用的一种方法。利用该装置可以得到不同的产物:
(1)b电极的电极反应式:___________
(2)该电解池的总方程式:___________
(3)若有产生0.4mol电子,产生气体的总体积是___________ (标准状况下)
Ⅱ.二氧化氯(ClO2)是一种高效、广谱、快速、安全的杀菌消毒剂。用石墨作电极,在一定条件下电解饱和食盐水制取ClO2工艺。
(4)a电极附近pH___________ (填“增大”“减小”或“不变”)。电极反应式为___________ 。
(5)b电极作电解池的___________ 极,电极反应式为___________ 。
(6)该工艺应使用___________ (填“阴”或“阳”)离子交换膜。

(1)b电极的电极反应式:
(2)该电解池的总方程式:
(3)若有产生0.4mol电子,产生气体的总体积是
Ⅱ.二氧化氯(ClO2)是一种高效、广谱、快速、安全的杀菌消毒剂。用石墨作电极,在一定条件下电解饱和食盐水制取ClO2工艺。
(4)a电极附近pH
(5)b电极作电解池的
(6)该工艺应使用
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】电化学原理在工业生产、物质制备、污染物理处理等方面应用广泛,请按要求回答下列问题。
Ⅰ.如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。
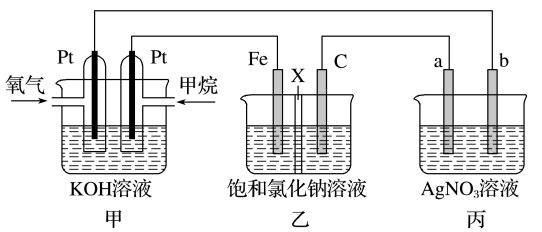
请按要求回答相关问题:
(1)甲烷燃料电池负极电极反应式是___________ 。
(2)乙中X是___________ 交换膜,向乙中加入几滴酚酞溶液,工作一段时间后___________ 电极(填“铁”或“碳”)附近溶液变红,该电极的电极反应式为___________ 。
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成气体的物质的量为___________ 。
(4)欲用丙装置给铜镀银,b应是___________ (填化学式)。
(5)将0.2molAgNO3、0.4molCu(NO3)2、0.6molKCl溶于水,配成100mL溶液,用惰性电极电解一段时间后,某一电极上析出了0.3molCu,此时在另一电极上产生的气体体积(标准状况)为___________ L
Ⅱ.微生物燃料电池(MFC)是一种现代化氨氮去除技术,如图为MFC碳氮联合同时去除的氮转化系统原理示意图。
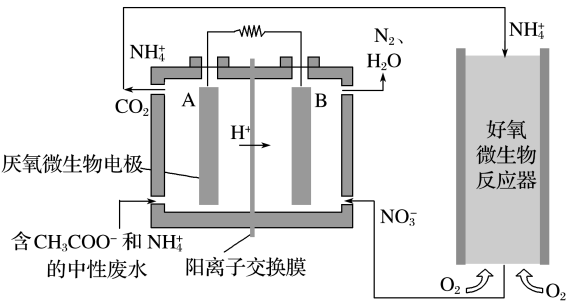
(6)A极的电极反应式为___________ ,A、B两极生成CO2和N2的物质的量之比为___________ 。
Ⅰ.如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。

请按要求回答相关问题:
(1)甲烷燃料电池负极电极反应式是
(2)乙中X是
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成气体的物质的量为
(4)欲用丙装置给铜镀银,b应是
(5)将0.2molAgNO3、0.4molCu(NO3)2、0.6molKCl溶于水,配成100mL溶液,用惰性电极电解一段时间后,某一电极上析出了0.3molCu,此时在另一电极上产生的气体体积(标准状况)为
Ⅱ.微生物燃料电池(MFC)是一种现代化氨氮去除技术,如图为MFC碳氮联合同时去除的氮转化系统原理示意图。

(6)A极的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】I.应用电化学原理,回答下列问题。
(1)下图中电流计指针偏移时,盐桥(装含琼脂的饱和 溶液)中离子移动的方向:
溶液)中离子移动的方向:___________ 离子移向硫酸锌溶液。
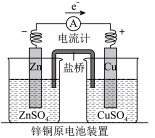
(2)下图中正极反应式为___________ ;若将 换成
换成 ,则负极反应式为
,则负极反应式为___________ 。
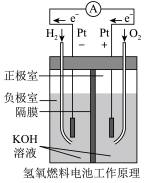
(3)下图中铅蓄电池放电时负极的质量___________ (填“增大”或“减小”),正极反应式为___________
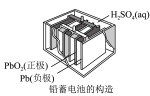
Ⅱ.现有如图所示装置,所有电极均为Pt,请按要求回答下列问题:
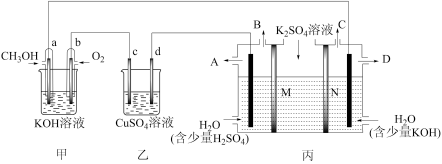
(4)甲装置是___________ (填“原电池”或“电解池”),乙池中c极的电极反应___________
(5)当b极消耗标准状况下的 112mL时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的pH=
112mL时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的pH=___________ 。若 (aq)足够,电解一段时间后,要恢复到原来的状态,则可加入
(aq)足够,电解一段时间后,要恢复到原来的状态,则可加入___________ 。
(6)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许某些离子通过,则A出口导出的溶液溶质为___________ (写化学式),N为___________ 离子交换膜(填“阴”或“阳”)。
(1)下图中电流计指针偏移时,盐桥(装含琼脂的饱和
 溶液)中离子移动的方向:
溶液)中离子移动的方向:
(2)下图中正极反应式为
 换成
换成 ,则负极反应式为
,则负极反应式为
(3)下图中铅蓄电池放电时负极的质量

Ⅱ.现有如图所示装置,所有电极均为Pt,请按要求回答下列问题:

(4)甲装置是
(5)当b极消耗标准状况下的
 112mL时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的pH=
112mL时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的pH= (aq)足够,电解一段时间后,要恢复到原来的状态,则可加入
(aq)足够,电解一段时间后,要恢复到原来的状态,则可加入(6)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许某些离子通过,则A出口导出的溶液溶质为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】近年来,加“碘”食盐较多地使用了碘酸钾 ,磺酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以
,磺酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以 溶液为电解液,在一定条件下电解,反应的化学方程式为
溶液为电解液,在一定条件下电解,反应的化学方程式为 。回答下列问题:
。回答下列问题:
(1)电解时,石墨作___________ 极,不锈钢作___________ 极。
(2)电解时的阳极反应式为___________ 。
(3)电解过程中电解质溶液的
___________ (填“变:大”、“变小”或“不变”)。
(4)当电解转移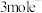 时,理论上可得到
时,理论上可得到___________  。
。
 ,磺酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以
,磺酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以 溶液为电解液,在一定条件下电解,反应的化学方程式为
溶液为电解液,在一定条件下电解,反应的化学方程式为 。回答下列问题:
。回答下列问题:(1)电解时,石墨作
(2)电解时的阳极反应式为
(3)电解过程中电解质溶液的

(4)当电解转移
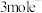 时,理论上可得到
时,理论上可得到 。
。
您最近一年使用:0次



