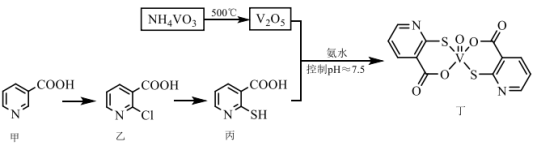
钒的化合物能有效调节血糖,化合物丁有望成为抗糖尿病的新型药物,其制备流程如下:
(1)金属V晶体的晶胞形状为立方体,结构如图所示。

①钒在元素周期表中的位置为_________ 。
②基态V的价层电子排布图为_________ 。
③设阿伏加德罗常数为 ,距离最近的两个钒原子间距为
,距离最近的两个钒原子间距为 (
( ),则金属钒的晶体密度为
),则金属钒的晶体密度为_________  (列出计算式)。
(列出计算式)。
(2) 转化为
转化为 的化学方程式是
的化学方程式是_________ 。
(3)下列说法正确的是_________(填字母)。
(4)分析丙的分子结构与性质。
①比较丙中 键角和
键角和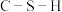 键角的大小并解释原因:
键角的大小并解释原因:_________ 。
②判断丙中能否形成分子内氢键。若能,画出其分子结构并表示出该氢键;若不能,说明原因:_________ 。
③1mol丙能与2mol一水合氨反应,反应的离子方程式是_________ 。
(5)丁是一种配合物。
①丁中存在配位键的原因是_________ 。
②含有化合物丁的样品中,含钒量的测定方法是:先把样品中的钒元素经处理转化为 溶液,再用硫酸酸化的
溶液,再用硫酸酸化的 标准溶液进行滴定,生成
标准溶液进行滴定,生成 。取样品10.2g,用上述方法测定其中钒的含量,消耗
。取样品10.2g,用上述方法测定其中钒的含量,消耗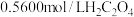 标准溶液25.00mL,则样品中钒元素的质量分数为
标准溶液25.00mL,则样品中钒元素的质量分数为_________ (写出计算结果)。

(1)金属V晶体的晶胞形状为立方体,结构如图所示。

①钒在元素周期表中的位置为
②基态V的价层电子排布图为
③设阿伏加德罗常数为
 ,距离最近的两个钒原子间距为
,距离最近的两个钒原子间距为 (
( ),则金属钒的晶体密度为
),则金属钒的晶体密度为 (列出计算式)。
(列出计算式)。(2)
 转化为
转化为 的化学方程式是
的化学方程式是(3)下列说法正确的是_________(填字母)。
A.元素的第一电离能: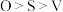 |
B.共价键的极性:丙中 乙中 乙中 |
C.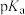 :乙>甲 :乙>甲 |
| D.甲分子中所有原子可能在同一平面内 |
①比较丙中
 键角和
键角和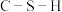 键角的大小并解释原因:
键角的大小并解释原因:②判断丙中能否形成分子内氢键。若能,画出其分子结构并表示出该氢键;若不能,说明原因:
③1mol丙能与2mol一水合氨反应,反应的离子方程式是
(5)丁是一种配合物。
①丁中存在配位键的原因是
②含有化合物丁的样品中,含钒量的测定方法是:先把样品中的钒元素经处理转化为
 溶液,再用硫酸酸化的
溶液,再用硫酸酸化的 标准溶液进行滴定,生成
标准溶液进行滴定,生成 。取样品10.2g,用上述方法测定其中钒的含量,消耗
。取样品10.2g,用上述方法测定其中钒的含量,消耗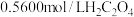 标准溶液25.00mL,则样品中钒元素的质量分数为
标准溶液25.00mL,则样品中钒元素的质量分数为
更新时间:2022-12-05 18:10:38
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】滴定法是化学常用来定量测定物质浓度的一种重要的实验方法。在食品工业、药品制造、化妆品行业等等都被广泛应用。
(I)中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25 g·L-1。某兴趣小组用如图装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。
(1)仪器A的名称是________ ,水通入A的进口为________ 。B中加入300.00 mL葡萄酒和适量盐酸,加热B使SO2全部逸出并与C中H2O2完全反应。
(2)除去C中过量的H2O2,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定,若滴定终点时溶液的pH=8.8,则选择的指示剂为________ 。滴定终点现象为______________________________________ 。
(3)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为:________ g·L-1。
(4)该测定结果往往比实际值偏高,最可能的原因是__________________________________ ,在不改变装置的情况下,如何改进:__________________________________________________________ 。
(II)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子(ClO )。饮用水中的ClO2、ClO
)。饮用水中的ClO2、ClO 含量可用连续碘量法进行测定。ClO2被I-还原为ClO
含量可用连续碘量法进行测定。ClO2被I-还原为ClO 、Cl-的转化率与溶液pH的关系如图所示。当pH≤2.0时,ClO
、Cl-的转化率与溶液pH的关系如图所示。当pH≤2.0时,ClO 也能被I-完全还原为Cl-。反应生成的I-用标准Na2S2O3溶液滴定:2Na2S2O3+I2=Na2S4O6+2NaI。
也能被I-完全还原为Cl-。反应生成的I-用标准Na2S2O3溶液滴定:2Na2S2O3+I2=Na2S4O6+2NaI。
(1)请写出pH≤2.0时ClO 与I-反应的离子方程式:
与I-反应的离子方程式:___________________________________ 。
(2)请完成相应的实验步骤:
步骤1:准确量取V mL水样加入到锥形瓶中;
步骤2:调节水样的pH为7.0~8.0;
步骤3:加入足量的KI晶体;
步骤4:加入少量淀粉溶液,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V1 mL;
步骤5:______________ ;
步骤6:再用c mol·L-1Na2S2O3溶液滴定至终点,又消耗Na2S2O3溶液V2 mL。
(3)根据上述分析数据,测得该饮用水中ClO 的浓度为
的浓度为________ mol·L-1(用含字母的代数式表示)。
(I)中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25 g·L-1。某兴趣小组用如图装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。

(1)仪器A的名称是
(2)除去C中过量的H2O2,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定,若滴定终点时溶液的pH=8.8,则选择的指示剂为
(3)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为:
(4)该测定结果往往比实际值偏高,最可能的原因是
(II)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子(ClO
 )。饮用水中的ClO2、ClO
)。饮用水中的ClO2、ClO 含量可用连续碘量法进行测定。ClO2被I-还原为ClO
含量可用连续碘量法进行测定。ClO2被I-还原为ClO 、Cl-的转化率与溶液pH的关系如图所示。当pH≤2.0时,ClO
、Cl-的转化率与溶液pH的关系如图所示。当pH≤2.0时,ClO 也能被I-完全还原为Cl-。反应生成的I-用标准Na2S2O3溶液滴定:2Na2S2O3+I2=Na2S4O6+2NaI。
也能被I-完全还原为Cl-。反应生成的I-用标准Na2S2O3溶液滴定:2Na2S2O3+I2=Na2S4O6+2NaI。
(1)请写出pH≤2.0时ClO
 与I-反应的离子方程式:
与I-反应的离子方程式:(2)请完成相应的实验步骤:
步骤1:准确量取V mL水样加入到锥形瓶中;
步骤2:调节水样的pH为7.0~8.0;
步骤3:加入足量的KI晶体;
步骤4:加入少量淀粉溶液,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V1 mL;
步骤5:
步骤6:再用c mol·L-1Na2S2O3溶液滴定至终点,又消耗Na2S2O3溶液V2 mL。
(3)根据上述分析数据,测得该饮用水中ClO
 的浓度为
的浓度为
您最近一年使用:0次
【推荐2】某种电镀污泥主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),可以用于制取Na2Cr2O7溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下:
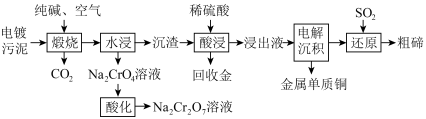
已知:煅烧时,Cu2Te发生的反应为Cu2Te+2O2 2CuO+TeO2。
2CuO+TeO2。
(1)煅烧时,Cr2O3发生反应的化学方程式为______ 。
(2)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有____ (填化学式)。
(3)工业上用重铬酸钠(Na2Cr2O7)母液生产重铬酸钾(K2Cr2O7)的工艺流程如图所示:

通过冷却结晶能析出大量K2Cr2O7的原因是_________ 。
(4)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.50 g配成250 mL溶液,用移液管取出25.00 mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000 mol·L-1硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定,重复进行二次实验。(已知Cr2O 被还原为Cr3+)
被还原为Cr3+)
①氧化还原滴定过程中的离子方程式为________ 。
②若三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00 mL,则所得产品中K2Cr2O7的纯度为_____ %。[已知M(K2Cr2O7)=294 g·mol-1,计算结果保留三位有效数字]。
(5)上述流程中K2Cr2O7发生氧化还原反应后所得溶液中除含有Cr3+外,还含有一定浓度的Fe3+杂质,可通过加碱调pH的方法使两者转化为沉淀。已知c(Cr3+)=3×10-5 mol·L-1,则当溶液中开始析出Cr(OH)3沉淀时Fe3+是否沉淀完全?____ (填“是”或“否”)。{已知:Ksp[Fe(OH)3]=4.0×10-38, Ksp[Cr(OH)3]=6.0×10-31}

已知:煅烧时,Cu2Te发生的反应为Cu2Te+2O2
 2CuO+TeO2。
2CuO+TeO2。(1)煅烧时,Cr2O3发生反应的化学方程式为
(2)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有
(3)工业上用重铬酸钠(Na2Cr2O7)母液生产重铬酸钾(K2Cr2O7)的工艺流程如图所示:

通过冷却结晶能析出大量K2Cr2O7的原因是
(4)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.50 g配成250 mL溶液,用移液管取出25.00 mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000 mol·L-1硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定,重复进行二次实验。(已知Cr2O
 被还原为Cr3+)
被还原为Cr3+)①氧化还原滴定过程中的离子方程式为
②若三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00 mL,则所得产品中K2Cr2O7的纯度为
(5)上述流程中K2Cr2O7发生氧化还原反应后所得溶液中除含有Cr3+外,还含有一定浓度的Fe3+杂质,可通过加碱调pH的方法使两者转化为沉淀。已知c(Cr3+)=3×10-5 mol·L-1,则当溶液中开始析出Cr(OH)3沉淀时Fe3+是否沉淀完全?
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】某校课外探究小组欲在实验室条件下制取少量纯净的无水氯化铝。查阅到以下资料:无水氯化铝是白色晶体,易吸收水分,常压下在177.8 ℃升华,遇潮湿空气即产生大量白雾。用于有机合成和石油工业的催化剂,以及用于处理润滑油等。他们设计了以下装置,请结合题意回答问题:
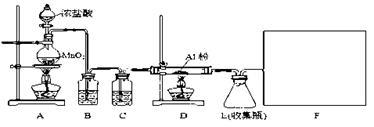
(1)A装置中发生反应的化学方程式为:_________________________
(2)装置B的作用是__________________________
(3)请给标记为F的实线方框选择合适的装置_______
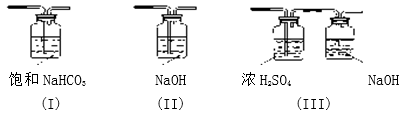
(4)AlCl3遇潮湿空气即产生大量白雾的原因是_________________ (结合化学方程式说明)。
(5)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,该小组同学提出酸碱中和滴定法测定方案。方案如下:首先准确量取残余清液稀释一定的倍数后作为试样,平行做了4次滴定。实验中所用NaOH溶液浓度为0.2000 mol·L-1,以下是实验记录与数据处理(不考虑NaOH与残液中其他成分的反应)。
①若本实验需要NaOH标准溶液80mL,则配制该标准溶液需要用到玻璃仪器有玻璃棒,烧杯_______
②经计算,该次滴定测的试样中盐酸浓度为_______________ mol·L-1。
③在本实验的滴定过程中,下列操作会使实验结果偏小的是___________ (填写序号)。
e.滴定前锥形瓶用待测盐酸润洗
f.观察读数时,滴定前仰视,滴定后俯视

(1)A装置中发生反应的化学方程式为:
(2)装置B的作用是
(3)请给标记为F的实线方框选择合适的装置

(4)AlCl3遇潮湿空气即产生大量白雾的原因是
(5)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,该小组同学提出酸碱中和滴定法测定方案。方案如下:首先准确量取残余清液稀释一定的倍数后作为试样,平行做了4次滴定。实验中所用NaOH溶液浓度为0.2000 mol·L-1,以下是实验记录与数据处理(不考虑NaOH与残液中其他成分的反应)。

①若本实验需要NaOH标准溶液80mL,则配制该标准溶液需要用到玻璃仪器有玻璃棒,烧杯
②经计算,该次滴定测的试样中盐酸浓度为
③在本实验的滴定过程中,下列操作会使实验结果偏小的是
| A.开始滴定时滴定管尖嘴处留有气泡,滴定结束气泡消失 |
| B.未用标准NaOH溶液润洗滴定管 |
| C.锥形瓶中加入待测盐酸后,再加少量水 |
| D.锥形瓶在滴定时剧烈摇动,有少量液体溅出 |
f.观察读数时,滴定前仰视,滴定后俯视
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
【推荐1】。某研究小组以甲苯为起始原料,按下列路线合成有机光电材料中间体 。
。
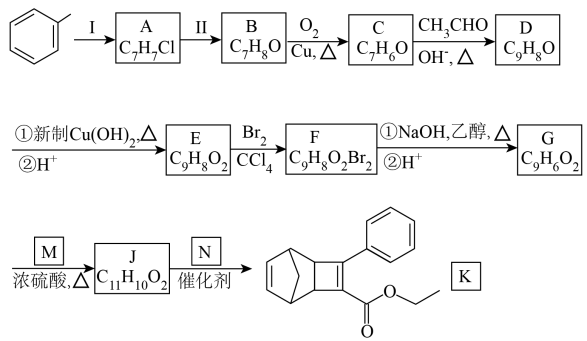
已知:①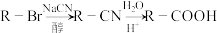 ;
;
②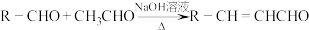 。
。
请回答:
(1)反应Ⅰ所需试剂和反应条件分别是___________ 、___________ 。C的化学名称为___________ 。化合物 的结构简式是
的结构简式是___________ 。
(2)下列说法不正确的是___________。
(3)反应 第①步反应的化学方程式是
第①步反应的化学方程式是___________ 。
(4)写出同时符合下列条件的化合物 的同分异构体的结构简式
的同分异构体的结构简式___________ 。
①分子中含有苯环;遇氯化铁溶液显紫色;
②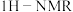 谱表明分子中有5种化学环境不同的氢原子;
谱表明分子中有5种化学环境不同的氢原子; 谱显示存在碳氧双键、碳碳双键。
谱显示存在碳氧双键、碳碳双键。
(5)设计以 、
、 为原料合成的合成
为原料合成的合成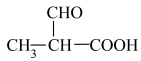 路线
路线___________ (用流程图表示,其它无机试剂任选)。
 。
。
已知:①
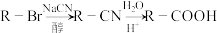 ;
;②
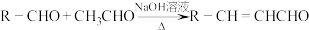 。
。请回答:
(1)反应Ⅰ所需试剂和反应条件分别是
 的结构简式是
的结构简式是(2)下列说法不正确的是___________。
| A.化合物D分子中所有原子可能共平面 |
B.化合物 与苯甲酸互为同系物 与苯甲酸互为同系物 |
C. 、 、 的反应类型分别为加成反应、取代反应 的反应类型分别为加成反应、取代反应 |
D.化合物 可由环戊二烯与乙烯经加成反应制得 可由环戊二烯与乙烯经加成反应制得 |
 第①步反应的化学方程式是
第①步反应的化学方程式是(4)写出同时符合下列条件的化合物
 的同分异构体的结构简式
的同分异构体的结构简式①分子中含有苯环;遇氯化铁溶液显紫色;
②
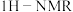 谱表明分子中有5种化学环境不同的氢原子;
谱表明分子中有5种化学环境不同的氢原子; 谱显示存在碳氧双键、碳碳双键。
谱显示存在碳氧双键、碳碳双键。(5)设计以
 、
、 为原料合成的合成
为原料合成的合成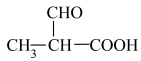 路线
路线
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
【推荐2】质子泵抑制剂奥美拉唑的中间体1可通过如下路线合成:

已知:
①
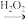
 ,
, 与苯环性质相似
与苯环性质相似
②
③
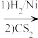
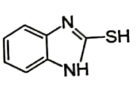
(1)化合物B的结构简式是___________ ;化合物G的含氮官能团的名称___________ 。
(2)下列说法正确的是___________。
(3)写出反应H+E→I的化学方程式___________ 。
(4)在制备H的过程中还可能生成一种分子式为C16H14N4O2S的化合物。用键线式表示其中一种结构___________ 。
(5)写出3种满足下列条件的化合物G的同分异构体的结构简式__________ 。
①1H-NMR谱显示只有6种不同环境的氢原子
②含有苯环且只有一个取代基,另含有一个五元环
③不含—O—O—、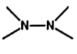 、
、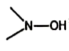 等结构片段
等结构片段
(6)根据题给信息,用不超过三步的反应设计D→ 的合成路线。
的合成路线。

已知:
①

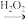
 ,
, 与苯环性质相似
与苯环性质相似②

③

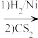

(1)化合物B的结构简式是
(2)下列说法正确的是___________。
| A.化合物C的分子式为C8H9N2O3 |
| B.H可能存在两种结构 |
| C.化合物A分子中所有的碳原子共平面 |
| D.化合物I可发生取代、加成、缩聚等反应 |
(4)在制备H的过程中还可能生成一种分子式为C16H14N4O2S的化合物。用键线式表示其中一种结构
(5)写出3种满足下列条件的化合物G的同分异构体的结构简式
①1H-NMR谱显示只有6种不同环境的氢原子
②含有苯环且只有一个取代基,另含有一个五元环
③不含—O—O—、
 、
、 等结构片段
等结构片段(6)根据题给信息,用不超过三步的反应设计D→
 的合成路线。
的合成路线。
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
【推荐3】靛蓝是最古老的蓝色染料,具有三千多年的历史。1870年,德国化学家拜耳(Baeyer)首次合成了靛蓝F(Indigo)。其合成路线如图所示:

已知:RCHO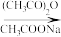 RCH=CHCOOH,回答相关问题。
RCH=CHCOOH,回答相关问题。
(1)A的化学名称为_________ ,C的结构简式为_________ 。
(2)写出D生成E第一步的化学方程式:________ 。
(3)E分子中最多有________ 个原子在同一条直线上。
(4)从反应类型的角度判断最后一步中葡萄糖的作用为________ 。
(5)1882年,拜耳利用邻硝基苯甲醛和丙酮在NaOH溶液中一步合成了靛蓝,已知产物中含有醋酸钠,写出化学方程式:________ 。
(6)1883年,拜耳确定了靛蓝的结构并因此获得了1905年诺贝尔化学奖。但是他当时所给出的结构是错误的,实际上给出的是靛蓝的顺反异构体G(异靛蓝),解释并说明靛蓝F和异靛蓝G哪个沸点更高:________ 。
(7)满足下列条件的B的同分异构体有______ 种(不考虑立体异构)。
a.属于酯类 b.分子中含有碳碳双键 c.属于芳香族化合物

已知:RCHO
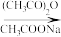 RCH=CHCOOH,回答相关问题。
RCH=CHCOOH,回答相关问题。(1)A的化学名称为
(2)写出D生成E第一步的化学方程式:
(3)E分子中最多有
(4)从反应类型的角度判断最后一步中葡萄糖的作用为
(5)1882年,拜耳利用邻硝基苯甲醛和丙酮在NaOH溶液中一步合成了靛蓝,已知产物中含有醋酸钠,写出化学方程式:
(6)1883年,拜耳确定了靛蓝的结构并因此获得了1905年诺贝尔化学奖。但是他当时所给出的结构是错误的,实际上给出的是靛蓝的顺反异构体G(异靛蓝),解释并说明靛蓝F和异靛蓝G哪个沸点更高:
(7)满足下列条件的B的同分异构体有
a.属于酯类 b.分子中含有碳碳双键 c.属于芳香族化合物
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】我国科学家在铁基超导研究方面取得了一系列的重大突破,标志着我国在凝聚态物理领域已经成为一个强国。LiZnAs 是研究铁基超导材料的重要前体。
(1)LiZnAs 中三种元素的电负性从小到大的顺序为_____ 。
(2)AsF3分子的空间构型为_____ ,As 原子的杂化轨道类型为_____ 。
(3)CO 分子内因配位键的存在,使 C 原子上的电子云密度较高而易与血红蛋白结合, 导致 CO 有剧毒。1mol[Zn(CN)4]2-离子内含有的共价键的数目为_____ ,配原子为_____ 。
(4)镍的氧化物常用作电极材料的基质。纯粹的 NiO 晶体的结构与 NaCl 的晶体结构相同,为获得更好的导电能力,将纯粹的 NiO 晶体在空气中加热,使部分 Ni2+被氧化成 Ni3+后, 每个晶胞内 O2-的数目和位置均未发生变化,镍离子的位置虽然没变,但其数目减少,造成晶体内产生阳离子空位(如图所示)。化学式为 NiO 的某镍氧化物晶体,阳离子的平均配位数为__________ ,阴离子的平均配位数与纯粹的 NiO 晶体相比____________ (填“增大”“减小”或“不变””,写出能体现镍元素化合价的该晶体的化学式________ 示例:Fe3O4写作 Fe2+Fe23+O4)。
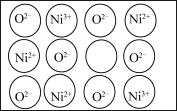
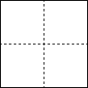
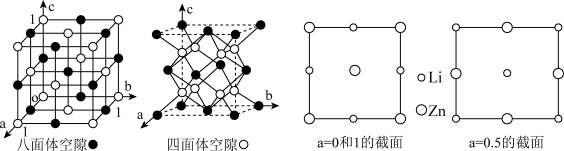
(5)所有的晶体均可看作由某些微粒按一定的方式堆积,另外的某些微粒填充在上述堆 积所形成的空隙中。在面心立方紧密堆积的晶胞中存在两种类型的空隙:八面体空隙和四面体空隙(如下左图所示)。在 LiZnAs 立方晶胞中,Zn 以面心立方形式堆积,Li 和 As 分别填充在 Zn 原子围成的八面体空隙和四面体空隙中,在 a=0,0.5 和 1 三个截面上 Zn 和 Li 按下图所示分布:请在下图 As 原子所在的截面上用“Δ”补画出 As 原子的位置,______________ 并说明 a=__________ 。
(1)LiZnAs 中三种元素的电负性从小到大的顺序为
(2)AsF3分子的空间构型为
(3)CO 分子内因配位键的存在,使 C 原子上的电子云密度较高而易与血红蛋白结合, 导致 CO 有剧毒。1mol[Zn(CN)4]2-离子内含有的共价键的数目为
(4)镍的氧化物常用作电极材料的基质。纯粹的 NiO 晶体的结构与 NaCl 的晶体结构相同,为获得更好的导电能力,将纯粹的 NiO 晶体在空气中加热,使部分 Ni2+被氧化成 Ni3+后, 每个晶胞内 O2-的数目和位置均未发生变化,镍离子的位置虽然没变,但其数目减少,造成晶体内产生阳离子空位(如图所示)。化学式为 NiO 的某镍氧化物晶体,阳离子的平均配位数为

(5)所有的晶体均可看作由某些微粒按一定的方式堆积,另外的某些微粒填充在上述堆 积所形成的空隙中。在面心立方紧密堆积的晶胞中存在两种类型的空隙:八面体空隙和四面体空隙(如下左图所示)。在 LiZnAs 立方晶胞中,Zn 以面心立方形式堆积,Li 和 As 分别填充在 Zn 原子围成的八面体空隙和四面体空隙中,在 a=0,0.5 和 1 三个截面上 Zn 和 Li 按下图所示分布:请在下图 As 原子所在的截面上用“Δ”补画出 As 原子的位置,


您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】金属铜、铁、铝等在人类文明史上先后被广泛使用。回答下列问题:
(1)铜、银、金三种金属在元素周期表同族且依次相邻,因此价电子层结构相似。银原子价层电子排布式为________ ;金元素在周期表的位置是________ 。
(2)观察如下循环图可以获知FeO的晶格能为________ kJ·mol-1。

(3)氯化铝熔点194℃,会升华,熔融态不易导电。实验测得气态氯化铝分子组成式为Al2Cl6,其结构式为________ ;气态氯化铝中存在________ (填选项标号)
A.离子键 B.配位键 C.氢键 D.范德华力 E.金属键 F.非极性共价键
(4)石墨微观结构如下图。其中碳原子杂化类型为________ 。金刚石晶体中碳碳键键长为0.155nm。金刚石的熔点略低于石墨,而远高于C60的原因是________ 。

(5)设阿伏加 德罗常数值为NA,则石墨的密度为________ 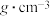 (列出计算表达式)
(列出计算表达式)
(1)铜、银、金三种金属在元素周期表同族且依次相邻,因此价电子层结构相似。银原子价层电子排布式为
(2)观察如下循环图可以获知FeO的晶格能为

(3)氯化铝熔点194℃,会升华,熔融态不易导电。实验测得气态氯化铝分子组成式为Al2Cl6,其结构式为
A.离子键 B.配位键 C.氢键 D.范德华力 E.金属键 F.非极性共价键
(4)石墨微观结构如下图。其中碳原子杂化类型为

(5)设阿伏加 德罗常数值为NA,则石墨的密度为
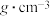 (列出计算表达式)
(列出计算表达式)
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】氮及其化合物广泛存在于自然界中,回答下列问题:
(1)基态氮原子核外有________ 种不同运动状态的电子,其价层电子排布图为_______________
(2)NH4NO3中元素的第一电离能大小关系:N_______ O,NO3-的空间构型为___________ ,NH4+中氮原子的杂化类型为_________
(3)HCN分子中含______ 个σ和________ 个π键。与CN-互为等电子体的分子和离子分别为______ 和______ (各举一例,填化学式)
(4)NH3极易溶于水,其主要原因是__________________________________________________________________
(5)立方氮化硼的结构与金刚石相似,其晶胞如图所示,B原子周围最近的N原子所构成的立体图形为_________ ,一个晶胞中N原子数目为__________

(1)基态氮原子核外有
(2)NH4NO3中元素的第一电离能大小关系:N
(3)HCN分子中含
(4)NH3极易溶于水,其主要原因是
(5)立方氮化硼的结构与金刚石相似,其晶胞如图所示,B原子周围最近的N原子所构成的立体图形为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】元素周期表中,第四周期元素单质及其化合物在化工生产和研究中有重要的应用。
(1)Ti能形成化合物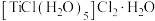 ,该化合物中
,该化合物中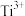 的配位数为
的配位数为______ ,在该化合物中不含______ (填标号)。
A. 键 B.
键 B. 键 C.配位键 D.离子键 E.极性键 F.非极性键
键 C.配位键 D.离子键 E.极性键 F.非极性键
(2)在ZnO催化作用下,呋喃( )可与氨反应,转化为吡咯(
)可与氨反应,转化为吡咯( ),吡咯分子中所有原子共平面,已知大π键可以用
),吡咯分子中所有原子共平面,已知大π键可以用 表示,其中m表示参与形成大
表示,其中m表示参与形成大 键的原子数,n代表大
键的原子数,n代表大 键中的电子数,则吡咯中大
键中的电子数,则吡咯中大 键可以表示为
键可以表示为______ 。呋喃的熔、沸点______ 吡咯(填“高于”或“低于”),原因是______ 。
(3)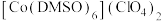 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为 。
。 中
中 键角
键角______  中
中 键角(填“大于”“小于”或“等于”)。
键角(填“大于”“小于”或“等于”)。
(4)硒氧化铋是一类:全新二维半导体芯片材料,为四方晶系晶胞结构(如图所示),可以看成带正电的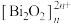 层与带负电的
层与带负电的 层交替堆叠。据此推断硒氧化铋的化学式为
层交替堆叠。据此推断硒氧化铋的化学式为______ 。晶胞棱边夹角均为90°,则晶体密度的计算式为______  (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)Ti能形成化合物
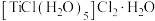 ,该化合物中
,该化合物中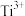 的配位数为
的配位数为A.
 键 B.
键 B. 键 C.配位键 D.离子键 E.极性键 F.非极性键
键 C.配位键 D.离子键 E.极性键 F.非极性键(2)在ZnO催化作用下,呋喃(
 )可与氨反应,转化为吡咯(
)可与氨反应,转化为吡咯( ),吡咯分子中所有原子共平面,已知大π键可以用
),吡咯分子中所有原子共平面,已知大π键可以用 表示,其中m表示参与形成大
表示,其中m表示参与形成大 键的原子数,n代表大
键的原子数,n代表大 键中的电子数,则吡咯中大
键中的电子数,则吡咯中大 键可以表示为
键可以表示为(3)
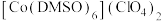 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为 。
。 中
中 键角
键角 中
中 键角(填“大于”“小于”或“等于”)。
键角(填“大于”“小于”或“等于”)。(4)硒氧化铋是一类:全新二维半导体芯片材料,为四方晶系晶胞结构(如图所示),可以看成带正电的
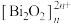 层与带负电的
层与带负电的 层交替堆叠。据此推断硒氧化铋的化学式为
层交替堆叠。据此推断硒氧化铋的化学式为 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】表中A、B、C、D、E、F为短周期主族元素,它们的原子序数依次增大。
(1)C基态原子的价电子轨道表达式为_____ ,CA3分子空间构型为_____ 。B,C,D三种元素的第一电离能由大到小的顺序_____ (填元素符号)。
(2)F的简单氢化物的VSEPR模型名称为_____ ,其属于_____ (填“极性”或“非极性”)分子,其沸点比水低的原因是_____ 。
(3)火箭推动剂由C2A4和A2D2组成,加热反应时有C元素的单质生成,写出该化学反应方程式:_____ 。
(4)下列关于C2A4和B2A4的说法中正确的是_____(填序号)。
(5)由E和G元素组成的化合物是共价化合物,该化合物气态时以共价的二聚分子(E2G6)形式存在,分子中所有原子都达到8e-稳定结构,请画出该二聚分子的结构式_____ 。
| A.元素周期表中原子半径最小的元素 | B.原子最外层电子数是内层电子数的2倍 |
| C.元素原子的核外p电子总数比s电子总数少1 | D.基态原子的价电子排布式为nsnnp2n |
| E.同周期中简单离子的半径最小 | F.与D同主族,且原子序数为D的2倍 |
| G.元素的主族序数与周期数的差为4 |
(2)F的简单氢化物的VSEPR模型名称为
(3)火箭推动剂由C2A4和A2D2组成,加热反应时有C元素的单质生成,写出该化学反应方程式:
(4)下列关于C2A4和B2A4的说法中正确的是_____(填序号)。
| A.分子中都含σ键和π键 |
| B.C2A4比B2A4的沸点高 |
| C.都是含极性键和非极性键的非极性分子 |
| D.B2A4分子发生加成反应时σ键断裂 |
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】NH3与甲醛CH2O反应可以制备乌洛托品(六亚甲基四胺,分子结构为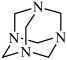 ),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:
),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:
(1)基态氮原子的价电子轨道表达式为___________ ,第三电离能I3(C)___________ I3(N)(填“>”或“<)。
(2)NH3的空间构型为___________ ,CH2O中C采取的杂化类型为___________ 。CH2O中碳氢键与NH3中氮氢键相比,键长较长的是___________ 。
(3)乌洛托品为___________ (填“极性”或“非极性”)分子,分子中的所有N原子呈正四面体分布,所有C原子呈___________ 几何体分布,该分子可与H+形成配位键,电子对给予体为___________ 原子。
(4)在乌洛托品晶体中,分子采取体心立方堆积,其分子配位数为___________ 。乌洛托品比金刚烷(C10H16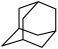 )水溶性更高,理由是
)水溶性更高,理由是___________ 。
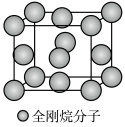
(5)金刚烷晶体采取分子密堆积、晶胞结构如图所示,若晶胞体积为Vnm3,阿伏加德罗常数为L×1023mol-1,则晶体的密度为___________ g/cm3。
 ),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:
),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:(1)基态氮原子的价电子轨道表达式为
(2)NH3的空间构型为
(3)乌洛托品为
(4)在乌洛托品晶体中,分子采取体心立方堆积,其分子配位数为
 )水溶性更高,理由是
)水溶性更高,理由是(5)金刚烷晶体采取分子密堆积、晶胞结构如图所示,若晶胞体积为Vnm3,阿伏加德罗常数为L×1023mol-1,则晶体的密度为

您最近一年使用:0次



