向三个体积均为 的恒容绝热容器中,按不同方式投入反应物,
的恒容绝热容器中,按不同方式投入反应物,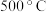 条件下开始发生如下反应:
条件下开始发生如下反应: ,测得达平衡时有关数据如下:
,测得达平衡时有关数据如下:
下列说法不正确的是 
 的恒容绝热容器中,按不同方式投入反应物,
的恒容绝热容器中,按不同方式投入反应物,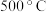 条件下开始发生如下反应:
条件下开始发生如下反应: ,测得达平衡时有关数据如下:
,测得达平衡时有关数据如下:| 容器 | Ⅰ | Ⅱ | Ⅲ |
| 反应物投入量 |  、 、 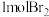 | 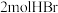 |  、 、 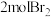 |
| 平衡时正反应速率 |  |  |  |
| 平衡常数 |  |  |  |
平衡时  的物质的量 的物质的量 |  |  |  |
| 反应物的转化率 |  |  |  |

A. | B.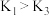 | C.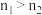 | D.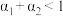 |
更新时间:2022-11-30 13:58:48
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】恒温、恒压下,反应N2 (g)+3H2 (g)  2NH3 (g)从两条途径分别建立平衡:
2NH3 (g)从两条途径分别建立平衡:
Ⅰ.N2、H2的起始浓度分别为1 mol / L和3 mol / L;
Ⅱ.NH3的起始浓度为4 mol / L。下列有关叙述不正确的是:
 2NH3 (g)从两条途径分别建立平衡:
2NH3 (g)从两条途径分别建立平衡:Ⅰ.N2、H2的起始浓度分别为1 mol / L和3 mol / L;
Ⅱ.NH3的起始浓度为4 mol / L。下列有关叙述不正确的是:
| A.途径Ⅰ与途径Ⅱ所得混合气体的百分组成相同 |
| B.途径Ⅰ的平衡速率v (N2)与途径Ⅱ的平衡速率v (NH3)的比值为1∶2 |
| C.途径Ⅰ所得NH3的浓度与途径Ⅱ所得NH3的浓度之比为1∶2 |
| D.途径Ⅰ与途径Ⅱ所得平衡混合气体的物质的量之比为1∶2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,发生反应PCl5(g) PCl3(g)+Cl2(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
PCl3(g)+Cl2(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
 PCl3(g)+Cl2(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是
PCl3(g)+Cl2(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是| t / s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3) / mol | 0 | 0. 16 | 0. 19 | 0. 20 | 0. 20 |
| A.反应在前50 s 的平均速率ν(Cl2)= 0. 0032 mol·L-1·s-1 |
| B.保持其他条件不变,升高温度,平衡时c(PCl3)= 0. 13 mol·L-1,则反应的ΔH<0 |
| C.相同温度下,起始时向容器中充入1. 0 mol PCl5、0. 20 mol PCl3 和0. 20 mol Cl2 ,反应达到平衡前ν(正)<ν(逆) |
| D.相同温度下,起始时向容器中充入2. 0 mol PCl3 和2. 0 mol Cl2 ,达到平衡时,PCl3 的转化率大于80% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】工业上主要采用甲醇与CO的羰基化反应来制备乙酸,发生反应如下:CH3OH(g)+CO(g)⇌CH3COOH(l)。在恒压密闭容器中通入0.20 mol CH3OH(g)和0.22 molCO,测得甲醇的转化率随温度的变化如图所示。已知在T2温度下,达到平衡时容器的体积为2 L。下列说法正确的是


| A.该反应的△H>0 |
| B.缩小容器体积,正反应反应速率加快,逆反应反应速率减慢 |
| C.温度为T1时,该反应的正反应速率B点大于A点 |
| D.温度为T2时,向上述已达平衡的恒压容器中,再通入0.12 mol CH3OH(g)和0.06 molCO的混合气体,则平衡不移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应: 。实验测得起始、平衡时的有关数据如下表,下列叙述正确的是
。实验测得起始、平衡时的有关数据如下表,下列叙述正确的是
 。实验测得起始、平衡时的有关数据如下表,下列叙述正确的是
。实验测得起始、平衡时的有关数据如下表,下列叙述正确的是| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
 |  |  | ||
| ① | 2 | 1 | 0 | 放出热量akJ |
| ② | 1 | 0.5 | 1 | 放出热量bkJ |
| ③ | 4 | 2 | 0 | 放出热量ckJ |
A. 的转化率:②>①>③ 的转化率:②>①>③ |
| B.三个容器内反应的平衡常数:③>①>② |
C.达平衡时 的体积分数:③>① 的体积分数:③>① |
D.放出热量关系: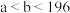 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度时,向容积为 2 L 的密闭容器中充入一定量的 SO2(g)和 O2(g),发生反应:2SO2(g)+ O2(g) 2SO3(g) △H = - 196 kJ/mol。一段时间后反应达到平衡状态,反应过程中测定的部分数据如表所示。
2SO3(g) △H = - 196 kJ/mol。一段时间后反应达到平衡状态,反应过程中测定的部分数据如表所示。
下列说法不正确的是
 2SO3(g) △H = - 196 kJ/mol。一段时间后反应达到平衡状态,反应过程中测定的部分数据如表所示。
2SO3(g) △H = - 196 kJ/mol。一段时间后反应达到平衡状态,反应过程中测定的部分数据如表所示。| 反应时间/min | n(SO2)/mol | n(O2)/mol |
| 0 | 2 | 1 |
| 5 | 1.2 | |
| 10 | 0.4 | |
| 15 | 0.8 |
| A.前 5 min 的平均反应速率为v(SO2) = 0.08 mol/(L·min) |
| B.保持温度不变,向平衡后的容器中再充入 0.2 mol SO2(g)和 0.2 mol SO3(g)时, v正 > v逆 |
| C.保持其他条件不变,若起始时向容器中充入 2 mol SO3(g),达到平衡状态时吸收 78.4 kJ的热量 |
| D.相同条件下,起始时向容器中充入 1.5 mol SO3(g),达到平衡状态时 SO3 的转化率为 40% |
您最近一年使用:0次
【推荐3】某温度下,反应CO2(g)+H2(g)⇌CO(g)+H2O(g)的平衡常数K=2.25,该温度下,在体积均为10L的三个密闭容器中分别加入反应物,起始加入量如表所示,下列判断不正确的是
| 起始量 | 甲 | 乙 | 丙 |
| H2(mol) | 1 | 2 | 2 |
| CO2(mol) | 1 | 1 | 2 |
| A.反应开始时,甲中的反应速率最慢,丙中的反应速率最快 |
| B.平衡时,甲和丙中CO2的转化率相等,均是60% |
| C.平衡时,乙中H2的转化率大于60% |
| D.平衡时,丙中c(H2)是0.08mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在1 L密闭容器中充入2 mol SO2和1 mol O2进行2SO2+O2 2SO3 ΔH<0,达到平衡时SO2转化率为a%,在1 L绝热容器中投料相同的情况下进行该反应,达到平衡时SO2转化率为b%,则下列关系正确的是
2SO3 ΔH<0,达到平衡时SO2转化率为a%,在1 L绝热容器中投料相同的情况下进行该反应,达到平衡时SO2转化率为b%,则下列关系正确的是
 2SO3 ΔH<0,达到平衡时SO2转化率为a%,在1 L绝热容器中投料相同的情况下进行该反应,达到平衡时SO2转化率为b%,则下列关系正确的是
2SO3 ΔH<0,达到平衡时SO2转化率为a%,在1 L绝热容器中投料相同的情况下进行该反应,达到平衡时SO2转化率为b%,则下列关系正确的是| A.a%﹥b% | B.a%﹤b% | C.a%=b% | D.a% 和b%的关系不确定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在温度体积不变时,1mol NO2高温分解,生成NO和O2,达到平衡时容器内总压强为反应前的1.2倍,这时NO2的转化率为
| A.10% | B.20% | C.40% | D.50% |
您最近一年使用:0次

 时,向容积为
时,向容积为 的密闭容器中充入一定量的
的密闭容器中充入一定量的 和
和 ,发生反应:
,发生反应: ,部分数据见下表
,部分数据见下表
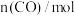
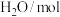


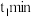 内的平均速率为
内的平均速率为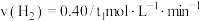
 氦气,压强增大,此反应速率加快
氦气,压强增大,此反应速率加快 时,
时,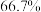
 ,则正反应速率加快,逆反应速率减慢
,则正反应速率加快,逆反应速率减慢

