在平衡体系Ca(OH)2(s) Ca2+(aq)+2OH-(aq) △H<0中,能使c(Ca2+)减小,而使c(OH-)增大的是
Ca2+(aq)+2OH-(aq) △H<0中,能使c(Ca2+)减小,而使c(OH-)增大的是
 Ca2+(aq)+2OH-(aq) △H<0中,能使c(Ca2+)减小,而使c(OH-)增大的是
Ca2+(aq)+2OH-(aq) △H<0中,能使c(Ca2+)减小,而使c(OH-)增大的是| A.加入少量CuCl2固体 | B.加入少量NaCl固体 |
| C.加入少量K2CO3固体 | D.升高体系温度 |
更新时间:2022-12-06 12:52:52
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】有关AgCl沉淀的溶解平衡的说法中,不正确的是( )
| A.AgCl沉淀生成和沉淀溶解不断进行,但速率相等 |
| B.AgCl难溶于水,溶液中没有Ag+和Cl- |
| C.升高温度,AgCl沉淀的溶解度增大 |
| D.向AgCl沉淀中加入NaCl固体,AgCl沉淀的溶解度降低 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列方程式书写正确的是
| A.NaHSO4在水溶液中的电离方程式:NaHSO4=Na++HSO4- |
B.H2SO3的电离方程式:H2SO3 2H++SO32- 2H++SO32- |
C.CO32-的水解方程式:CO32-+H2O HCO3-+OH- HCO3-+OH- |
| D.CaCO3沉淀溶解平衡方程式:CaCO3(s)=Ca2+(aq)+CO32-(aq) |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】下列有关说法正确的是
| A.Hg(l) + H2SO4(aq) = HgSO4(aq) + H2(g)常温下不能自发进行,说明△H<0 |
| B.用惰性电极电解1L1mol/L的CuSO4溶液,当阴极析出3.2 g铜时,加入0.05 molCu(OH)2固体可将溶液恢复至原浓度 |
| C.已知25℃时,Ksp(AgCl)=1.8×10-10、Ksp(Ag2CrO4)=2.0×10-12,所以AgCl的溶解度大于Ag2CrO4的溶解度 |
| D.25℃时,向0.1 mol/L CH3COOH溶液中加入少量CH3COONa固体,该溶液中水的电离程度将增大,且Kw不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】20℃时,PbCl2(s)在不同浓度盐酸中的最大溶解量(单位:g·L-1)如图所示。下列叙述正确的是( )
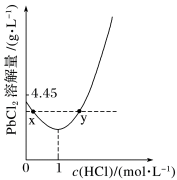

| A.盐酸浓度越小,Ksp(PbCl2)越小 |
| B.当盐酸浓度大于1mol·L-1时,PbCl2(s)与盐酸因发生化学反应而溶解 |
| C.x、y两点对应的溶液中c(Pb2+)相等 |
| D.当盐酸浓度为1 mol·L-1时,溶液中c(Pb2+)一定最小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】有关AgCl沉淀的溶解平衡说法正确的是( )
| A.AgCl沉淀生成和沉淀溶解不断进行,但速率相等 |
| B.AgCl难溶于水,溶液中没有Ag+和Cl- |
| C.升高温度,AgCl沉淀的溶解度不变 |
| D.向AgCl沉淀中加入NaCl固体,AgCl的沉淀溶解平衡不移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如下图所示。下列说法错误的是
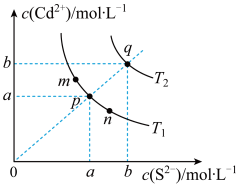

A.图中p和q分别为 、 、 温度下CdS达到沉淀溶解平衡 温度下CdS达到沉淀溶解平衡 |
B.图中各点对应的 的关系为: 的关系为: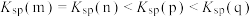 |
C.向m点的溶液中加入少量 固体,溶液中 固体,溶液中 浓度降低 浓度降低 |
| D.温度降低时,q点饱和溶液的组成由q沿qp线向p方向移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】25℃时,向1L0.2mol•L﹣1氢氟酸溶液中加入1L0.002mol•L﹣1CaCl2溶液,已知该温度下Ka(HF)=3.6×10﹣4,Ksp(CaF2)=1.46×10﹣10,下列说法正确的是
| A.氢氟酸溶液中不存在HF分子 |
| B.Ksp(CaF2)随温度和浓度的变化而变化 |
| C.25℃时,0.2mol•L﹣1氢氟酸溶液的pH=1 |
| D.两溶液混合后有沉淀生成 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】室温下,已知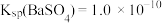 ,
,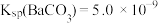 。下列说法中不正确的是
。下列说法中不正确的是
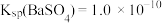 ,
,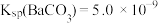 。下列说法中不正确的是
。下列说法中不正确的是A.在含有 固体的溶液中,不一定有 固体的溶液中,不一定有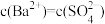 |
B.向只含有 的悬浊液中加入少量水,溶液中 的悬浊液中加入少量水,溶液中 增大 增大 |
C.向某 溶液中滴加 溶液中滴加 溶液,欲使 溶液,欲使 沉淀完全 沉淀完全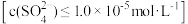 应保持溶液中 应保持溶液中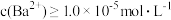 |
D.往相同浓度的 和 和 的混合溶液中加入 的混合溶液中加入 溶液,当生成 溶液,当生成 沉淀时, 沉淀时, |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如下图所示。下列说法错误的是


A.图中p和q分别为 、 、 温度下CdS达到沉淀溶解平衡 温度下CdS达到沉淀溶解平衡 |
B.图中各点对应的 的关系为: 的关系为: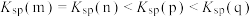 |
C.向m点的溶液中加入少量 固体,溶液中 固体,溶液中 浓度降低 浓度降低 |
| D.温度降低时,q点饱和溶液的组成由q沿qp线向p方向移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】下列有关电解质溶液的说法不正确的是
A.向0.1 的氨水中加入少量水,溶液中 的氨水中加入少量水,溶液中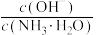 增大 增大 |
B.将 溶液从20℃升温至30℃,溶液中 溶液从20℃升温至30℃,溶液中 增大 增大 |
C.向氢氧化钠溶液中加入醋酸溶液至中性,溶液中 |
D.向 的饱和溶液中加入 的饱和溶液中加入 固体,溶液中的 固体,溶液中的 |
您最近一年使用:0次



