利用“价类二维图”可以系统地研究含氯物质的性质及其转化关系,氯元素的价类二维图如图所示:

回答下列问题:
(1)a物质的化学式为____ 。
(2)写出b物质在光照条件下反应的化学方程式为____ 。
(3)实验室利用反应MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O和如图所示装置制取并收集纯净干燥的Cl2。
MnCl2+Cl2↑+2H2O和如图所示装置制取并收集纯净干燥的Cl2。
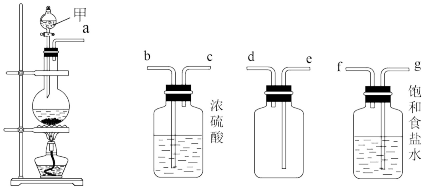
回答下列问题:
①仪器甲的名称为____ ;圆底烧瓶内发生反应的离子方程式为____ 。
②反应中产生标准状况下4.48LCl2时,需消耗MnO2的质量为____ 。
③为完成上述实验,仪器口的连接顺序为____ 。该实验装置还存在的缺陷是____ 。

回答下列问题:
(1)a物质的化学式为
(2)写出b物质在光照条件下反应的化学方程式为
(3)实验室利用反应MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O和如图所示装置制取并收集纯净干燥的Cl2。
MnCl2+Cl2↑+2H2O和如图所示装置制取并收集纯净干燥的Cl2。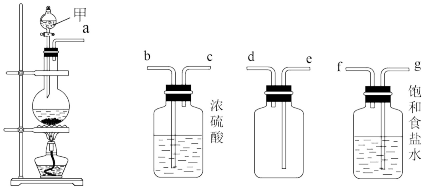
回答下列问题:
①仪器甲的名称为
②反应中产生标准状况下4.48LCl2时,需消耗MnO2的质量为
③为完成上述实验,仪器口的连接顺序为
更新时间:2022/12/13 21:17:06
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】某学习兴趣小组为探究离子反应发生的条件,选取了MgSO4和Ba(OH)2为实验对象,过程如下:
实验1:向烧杯中依次加入下列试剂,记录灯泡变化。
①MgSO4粉末:灯泡不亮
②加入蒸馏水:灯泡变亮
③逐滴滴加0.1 mol/L Ba(OH)2灯泡变化如下:
实验3:用M溶液替代MgSO4溶液,重复实验进行对照,结果与实验1的灯泡现象相同。
(1)实验1中加蒸馏水灯泡变亮的原因是___________ ,用离子方程式解释过程1中灯泡变暗的原因___________ 。
(2)实验2中选取氢氧化钠溶液的浓度为___________ ,加入氢氧化钠溶液过程中灯泡不熄灭,原因是___________ 。
(3)实验3中,M溶液为___________ ,该溶液属于___________ (填“强电解质”“弱电解质”“非电解质”或“以上都不是”)。
(4)已知:常温下,Mg(OH)2悬浊液中,c2(OH-)·c(Mg2+)= A(A是一个常数)。比较实验1中c(OH-)大小,溶液1___________ (填“>”“<”或“=”)溶液2。
实验1:向烧杯中依次加入下列试剂,记录灯泡变化。
①MgSO4粉末:灯泡不亮
②加入蒸馏水:灯泡变亮
③逐滴滴加0.1 mol/L Ba(OH)2灯泡变化如下:
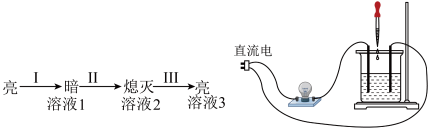
实验3:用M溶液替代MgSO4溶液,重复实验进行对照,结果与实验1的灯泡现象相同。
(1)实验1中加蒸馏水灯泡变亮的原因是
(2)实验2中选取氢氧化钠溶液的浓度为
(3)实验3中,M溶液为
(4)已知:常温下,Mg(OH)2悬浊液中,c2(OH-)·c(Mg2+)= A(A是一个常数)。比较实验1中c(OH-)大小,溶液1
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)下面是同学们熟悉的物质:① ;②金刚石;③
;②金刚石;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ ;⑧
;⑧ ;⑨
;⑨ ;⑩
;⑩ 。
。
这些物质中,只含有离子键的是___________ (填序号,下同);不存在化学键的是___________ ;属于共价化合物的是___________ 。
(2)将 溶于水,破坏了
溶于水,破坏了 中的
中的___________ ,写出其电离方程式:___________ 。
(3)已知氢碘酸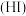 是一种具有强还原性的强酸,向
是一种具有强还原性的强酸,向 胶体中逐滴加入
胶体中逐滴加入 稀溶液,会出现如下一系列变化:先出现红褐色沉淀,随后沉淀溶解,溶液呈黄色,最后溶液颜色加深。
稀溶液,会出现如下一系列变化:先出现红褐色沉淀,随后沉淀溶解,溶液呈黄色,最后溶液颜色加深。
①红褐色沉淀溶解的离子方程式是___________ ;
②最后溶液颜色加深的离子方程式是___________ 。
(4)若实验室用密度为 ,质量分数为98%的浓硫酸配置
,质量分数为98%的浓硫酸配置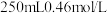 的稀硫酸。
的稀硫酸。
①配置时用量筒量取浓硫酸的体积为___________  ;
;
②实验所用到的玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外,还有___________ ;
③若某同学实际配制得到的浓度为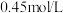 ,可能的原因是
,可能的原因是___________ (填序号)。
A.浓硫酸稀释后未经冷却直接转移 B.容量瓶洗净后未经干燥处理
C.没有将洗涤液转入容量瓶 D.定容时仰视刻度
(1)下面是同学们熟悉的物质:①
 ;②金刚石;③
;②金刚石;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ ;⑧
;⑧ ;⑨
;⑨ ;⑩
;⑩ 。
。这些物质中,只含有离子键的是
(2)将
 溶于水,破坏了
溶于水,破坏了 中的
中的(3)已知氢碘酸
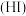 是一种具有强还原性的强酸,向
是一种具有强还原性的强酸,向 胶体中逐滴加入
胶体中逐滴加入 稀溶液,会出现如下一系列变化:先出现红褐色沉淀,随后沉淀溶解,溶液呈黄色,最后溶液颜色加深。
稀溶液,会出现如下一系列变化:先出现红褐色沉淀,随后沉淀溶解,溶液呈黄色,最后溶液颜色加深。①红褐色沉淀溶解的离子方程式是
②最后溶液颜色加深的离子方程式是
(4)若实验室用密度为
 ,质量分数为98%的浓硫酸配置
,质量分数为98%的浓硫酸配置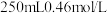 的稀硫酸。
的稀硫酸。①配置时用量筒量取浓硫酸的体积为
 ;
;②实验所用到的玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外,还有
③若某同学实际配制得到的浓度为
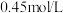 ,可能的原因是
,可能的原因是A.浓硫酸稀释后未经冷却直接转移 B.容量瓶洗净后未经干燥处理
C.没有将洗涤液转入容量瓶 D.定容时仰视刻度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
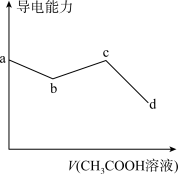
【推荐3】通过测定溶液导电性的变化可以探究离子反应的过程,向一定浓度的NH3·H2O和NaOH混合溶液中滴加稀CH3COOH,溶液导电性随加入的CH3COOH溶液的体积变化如图所示:_______ (填序号),bc段发生反应的离子方程式是_______ (填序号)。
A.H++OH-=H2O
B.CH3COOH+OH-=H2O+CH3COO-
C.CH3COOH+NH3·H2O=H2O+CH3COO-+NH
D.H++NH3·H2O=H2O+NH
(2)cd段溶液导电性下降的原因是_______ 。
A.H++OH-=H2O
B.CH3COOH+OH-=H2O+CH3COO-
C.CH3COOH+NH3·H2O=H2O+CH3COO-+NH

D.H++NH3·H2O=H2O+NH

(2)cd段溶液导电性下降的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】从价类二维的角度认识化学物质是一种高效的学习方法,铜元素的价类二维图如图,根据要求回答有关问题:
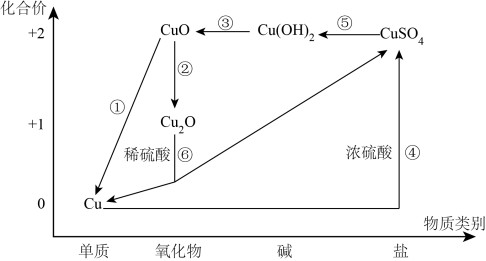
(1) 是铜绿的主要成分,其属于
是铜绿的主要成分,其属于 ______ (填序号)。
a.碱 b.正盐 c.碱式盐 d.酸式盐 e.碳酸盐
(2)转化②中铜元素的化合价_______ (填“升高”或“降低”)。
(3)转化④_____ (填“是”或“不是”)氧化还原反应。
(4)转化⑤的反应类型为_______ (填基本反应类型), 为
为 _______ (填“是”或“非”)电解质。
(5)已知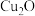 为砖红色不溶于水的固体,转化⑥可生成
为砖红色不溶于水的固体,转化⑥可生成 、
、 溶液和另一种物质,则转化⑥的方程式为
溶液和另一种物质,则转化⑥的方程式为 _______ 。
(6)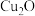 与稀
与稀 可以发生氧化还原反应,完成并配平下列方程式:
可以发生氧化还原反应,完成并配平下列方程式:_____
_______ 6
6 2
2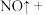 _______
_______

(1)
 是铜绿的主要成分,其属于
是铜绿的主要成分,其属于 a.碱 b.正盐 c.碱式盐 d.酸式盐 e.碳酸盐
(2)转化②中铜元素的化合价
(3)转化④
(4)转化⑤的反应类型为
 为
为 (5)已知
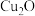 为砖红色不溶于水的固体,转化⑥可生成
为砖红色不溶于水的固体,转化⑥可生成 、
、 溶液和另一种物质,则转化⑥的方程式为
溶液和另一种物质,则转化⑥的方程式为 (6)
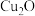 与稀
与稀 可以发生氧化还原反应,完成并配平下列方程式:
可以发生氧化还原反应,完成并配平下列方程式:_______
 6
6 2
2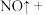 _______
_______
您最近一年使用:0次
【推荐2】某化学兴趣小组欲利用下列试剂:铁粉、锌粉、 溶液、KSCN溶液、新制氯水,探究
溶液、KSCN溶液、新制氯水,探究 的还原性,请回答下列问题:
的还原性,请回答下列问题:
(1)用所给试剂写出体现 具有还原性的离子反应方程式:
具有还原性的离子反应方程式:_______ ,由此得出,在配制 溶液时,
溶液时, 容易被氧化,欲检验
容易被氧化,欲检验 溶液是否变质,应加入的试剂是
溶液是否变质,应加入的试剂是_______ ;
(2)该小组同学用 溶液和NaOH溶液混合制备
溶液和NaOH溶液混合制备 ,观察到沉淀最终变成红褐色,原因是
,观察到沉淀最终变成红褐色,原因是_______ (用化学方程式解释);
(3)酸性条件下,某反应中反应物与生成物有 、
、 、
、 、
、 、
、 和一种未知离子X。
和一种未知离子X。
已知:反应中1mol 得5mol电子。
得5mol电子。
① 中Mn元素的化合价为
中Mn元素的化合价为_______ ,X离子是_______ 。
②该反应的离子方程式是_______ 。
 溶液、KSCN溶液、新制氯水,探究
溶液、KSCN溶液、新制氯水,探究 的还原性,请回答下列问题:
的还原性,请回答下列问题:(1)用所给试剂写出体现
 具有还原性的离子反应方程式:
具有还原性的离子反应方程式: 溶液时,
溶液时, 容易被氧化,欲检验
容易被氧化,欲检验 溶液是否变质,应加入的试剂是
溶液是否变质,应加入的试剂是(2)该小组同学用
 溶液和NaOH溶液混合制备
溶液和NaOH溶液混合制备 ,观察到沉淀最终变成红褐色,原因是
,观察到沉淀最终变成红褐色,原因是(3)酸性条件下,某反应中反应物与生成物有
 、
、 、
、 、
、 、
、 和一种未知离子X。
和一种未知离子X。已知:反应中1mol
 得5mol电子。
得5mol电子。①
 中Mn元素的化合价为
中Mn元素的化合价为②该反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)N原子的摩尔质量是__________ ,1mol HNO3约含有___________ 个氧原子(用NA表示)。
(2)实验室中以下述反应制取氯气:4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O 在该反应中浓盐酸的作用为
MnCl2+Cl2↑+2H2O 在该反应中浓盐酸的作用为_________________ , 若在标准状况下制得11.2L氯气则转移的电子总数为_______ 摩尔。
(2)实验室中以下述反应制取氯气:4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O 在该反应中浓盐酸的作用为
MnCl2+Cl2↑+2H2O 在该反应中浓盐酸的作用为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题
(1)下列10种物质:
①水②空气③铁④二氧化碳⑤硫酸⑥熟石灰[Ca(OH)2]⑦胆矾(CuSO4·5H2O)⑧酒精⑨硫酸氢钠溶液⑩熔融状态氯化钠
a.属于电解质的是___________ ;(填序号,下同)
b.属于非电解质的是___________ ;
c.属于弱电解质的是___________ ;
d.能导电的是___________ 。
(2)已知: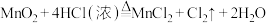 一定质量的二氧化锰溶解在
一定质量的二氧化锰溶解在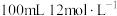 的浓盐酸中,当反应生成2.24L氯气(标况)时。请计算:
的浓盐酸中,当反应生成2.24L氯气(标况)时。请计算:
a.反应耗用 的质量
的质量___________ ;
b.反应结束时理论上最后能生成氯气的体积___________ (标准状况下)。
(1)下列10种物质:
①水②空气③铁④二氧化碳⑤硫酸⑥熟石灰[Ca(OH)2]⑦胆矾(CuSO4·5H2O)⑧酒精⑨硫酸氢钠溶液⑩熔融状态氯化钠
a.属于电解质的是
b.属于非电解质的是
c.属于弱电解质的是
d.能导电的是
(2)已知:
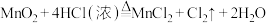 一定质量的二氧化锰溶解在
一定质量的二氧化锰溶解在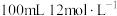 的浓盐酸中,当反应生成2.24L氯气(标况)时。请计算:
的浓盐酸中,当反应生成2.24L氯气(标况)时。请计算:a.反应耗用
 的质量
的质量b.反应结束时理论上最后能生成氯气的体积
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)现有下列11种物质:
①纯碱②Mn2O7③硫酸④CaO⑤CO2⑥Na2CO3
⑦CuSO4·5H2O⑧SO2⑨Na2O2⑩CO⑪NO2
其中属于正盐的是______________ ;属于酸性氧化物的是__________________ 。
(2)有关胶体的实验中:
①实验室制备Fe(OH)3胶体的化学方程式为_________
②将橘红色的硫化锑(Sb2S3)胶体,装入U形管,插入电极后通直流电,发现阳极负极橘红色加深,证明Sb2S3胶粒带______ (填“正”或“负”)电荷。
①纯碱②Mn2O7③硫酸④CaO⑤CO2⑥Na2CO3
⑦CuSO4·5H2O⑧SO2⑨Na2O2⑩CO⑪NO2
其中属于正盐的是
(2)有关胶体的实验中:
①实验室制备Fe(OH)3胶体的化学方程式为
②将橘红色的硫化锑(Sb2S3)胶体,装入U形管,插入电极后通直流电,发现阳极负极橘红色加深,证明Sb2S3胶粒带
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】焦亚硫酸钠 在医药、印染、食品等方面应用广泛,也可作为食品的抗氧化剂。
在医药、印染、食品等方面应用广泛,也可作为食品的抗氧化剂。
(1)工业上制备焦亚硫酸钠 常用
常用 与碳酸钠溶液的反应,当
与碳酸钠溶液的反应,当 加过量直至过饱和时,溶液中就会析出焦亚硫酸钠的晶体,写出该反应的化学方程式:
加过量直至过饱和时,溶液中就会析出焦亚硫酸钠的晶体,写出该反应的化学方程式:______ 。
(2)由于 具有毒性,因此国家对其在食品中的用量有严格的规定。某化学兴趣小组在测定某白葡萄酒中的残留量时,取40mL葡萄酒样品,用
具有毒性,因此国家对其在食品中的用量有严格的规定。某化学兴趣小组在测定某白葡萄酒中的残留量时,取40mL葡萄酒样品,用 的含有淀粉的碘的标准溶液滴定至终点,消耗碘标准溶液5mL,则滴定终点的现象为
的含有淀粉的碘的标准溶液滴定至终点,消耗碘标准溶液5mL,则滴定终点的现象为______ ,该样品中 的残留量为
的残留量为______ 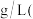 以
以 计
计 。
。
 在医药、印染、食品等方面应用广泛,也可作为食品的抗氧化剂。
在医药、印染、食品等方面应用广泛,也可作为食品的抗氧化剂。(1)工业上制备焦亚硫酸钠
 常用
常用 与碳酸钠溶液的反应,当
与碳酸钠溶液的反应,当 加过量直至过饱和时,溶液中就会析出焦亚硫酸钠的晶体,写出该反应的化学方程式:
加过量直至过饱和时,溶液中就会析出焦亚硫酸钠的晶体,写出该反应的化学方程式:(2)由于
 具有毒性,因此国家对其在食品中的用量有严格的规定。某化学兴趣小组在测定某白葡萄酒中的残留量时,取40mL葡萄酒样品,用
具有毒性,因此国家对其在食品中的用量有严格的规定。某化学兴趣小组在测定某白葡萄酒中的残留量时,取40mL葡萄酒样品,用 的含有淀粉的碘的标准溶液滴定至终点,消耗碘标准溶液5mL,则滴定终点的现象为
的含有淀粉的碘的标准溶液滴定至终点,消耗碘标准溶液5mL,则滴定终点的现象为 的残留量为
的残留量为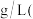 以
以 计
计 。
。
您最近一年使用:0次

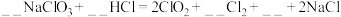 ,配平反应方程式并用单线桥表示电子转移的方向和数目
,配平反应方程式并用单线桥表示电子转移的方向和数目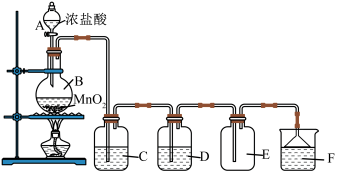
 的化学方程式为
的化学方程式为 Na
Na

