按要求填空:
(1)13gC2H2(g)完全燃烧生成CO2(g)和H2O(l)时,放出659kJ的热量,写出该反应的热化学方程式_____ 。
(2)试写出镁粉投入NH4Cl溶液中反应的离子方程式_____ 。
(3)AlCl3水溶液的pH值_____ 7(填“>”、“<”或“=”),原因是(用离子方程式表示)______ 。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是_____ 。
(4)在配制Na2S溶液时,为了防止发生水解,可以加入少量的_____ 。
(5)常温下,测得CH3COONH4溶液的pH=7,则说明CH3COO-的水解程度______ (填“>”、“<”或“=”)NH 的水解程度,CH3COO-与NH
的水解程度,CH3COO-与NH 浓度的大小关系是:c(CH3COO-)
浓度的大小关系是:c(CH3COO-)______ c(NH )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。
(1)13gC2H2(g)完全燃烧生成CO2(g)和H2O(l)时,放出659kJ的热量,写出该反应的热化学方程式
(2)试写出镁粉投入NH4Cl溶液中反应的离子方程式
(3)AlCl3水溶液的pH值
(4)在配制Na2S溶液时,为了防止发生水解,可以加入少量的
(5)常温下,测得CH3COONH4溶液的pH=7,则说明CH3COO-的水解程度
 的水解程度,CH3COO-与NH
的水解程度,CH3COO-与NH 浓度的大小关系是:c(CH3COO-)
浓度的大小关系是:c(CH3COO-) )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。
更新时间:2022-12-20 20:13:30
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】某学生通过测定反应过程中所放出的热量来计算中和反应的反应热,将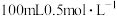 的盐酸与
的盐酸与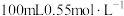 的
的 溶液在如图所示的装置中进行中和反应(在稀溶液中,可以近似地认为酸、碱的密度、比热容与水的相等,
溶液在如图所示的装置中进行中和反应(在稀溶液中,可以近似地认为酸、碱的密度、比热容与水的相等, 。)回答下列问题:
。)回答下列问题:

(1)从实验装置上看,图中缺少的一种玻璃仪器是___________ 。
(2)简易量热计如果不盖杯盖,生成 时所测得中和反应的反应热(
时所测得中和反应的反应热( )将
)将___________ (填“偏大”“偏小”或“不变”)。
(3)实验中改用 的盐酸和
的盐酸和 的
的 溶液进行反应,与上述实验相比,二者所放出的热量
溶液进行反应,与上述实验相比,二者所放出的热量___________ (填“相等”或“不相等”)。
(4)已知酸碱中和热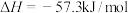 。若用
。若用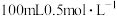 的醋酸与
的醋酸与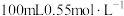 的
的 溶液进行上述实验,发现体系温度升高了
溶液进行上述实验,发现体系温度升高了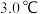 ,写出醋酸电离的热化学方程式
,写出醋酸电离的热化学方程式___________ 。
(5)下列说法正确的是___________(填字母)。
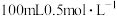 的盐酸与
的盐酸与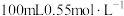 的
的 溶液在如图所示的装置中进行中和反应(在稀溶液中,可以近似地认为酸、碱的密度、比热容与水的相等,
溶液在如图所示的装置中进行中和反应(在稀溶液中,可以近似地认为酸、碱的密度、比热容与水的相等, 。)回答下列问题:
。)回答下列问题:
(1)从实验装置上看,图中缺少的一种玻璃仪器是
(2)简易量热计如果不盖杯盖,生成
 时所测得中和反应的反应热(
时所测得中和反应的反应热( )将
)将(3)实验中改用
 的盐酸和
的盐酸和 的
的 溶液进行反应,与上述实验相比,二者所放出的热量
溶液进行反应,与上述实验相比,二者所放出的热量(4)已知酸碱中和热
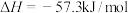 。若用
。若用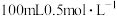 的醋酸与
的醋酸与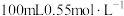 的
的 溶液进行上述实验,发现体系温度升高了
溶液进行上述实验,发现体系温度升高了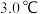 ,写出醋酸电离的热化学方程式
,写出醋酸电离的热化学方程式(5)下列说法正确的是___________(填字母)。
| A.向内筒中加入稀碱时,应当迅速加入 |
| B.将用量筒量取好的稀盐酸加入内筒后,应当快速用水冲洗量筒内壁剩余的稀盐酸至内筒中,以免造成测量误差 |
| C.整个实验装置看作反应体系,空气看作环境 |
D.内筒洗净后,未及时烘干,直接用该内筒进行实验,对生成 时所测得的中和反应的反应热( 时所测得的中和反应的反应热( )无影响 )无影响 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学反应都伴有能量变化,请回答下列问题:
(1)书写下列反应的热化学方程式。(每个热化学方程式3分)
①1L1mol/L稀盐酸跟1L1mol/LNaOH溶液发生中和反应放出57.3kJ热量。___________ 。
②24 与足量
与足量 反应生成
反应生成 和
和 ,吸收262.6kJ热量。
,吸收262.6kJ热量。___________
③已知16g固体硫完全燃烧时放出148.4kJ的热量,写出表示硫的燃烧的热化学方程式:___________ 。
④如图是298K、101kPa时, 与
与 反应过程中能量变化的曲线图。该反应的热化学方程式为:
反应过程中能量变化的曲线图。该反应的热化学方程式为: ___________ 。

(2)比较下列各组热化学方程式中 的大小关系。
的大小关系。
①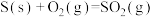

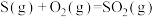


___________ 
②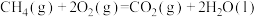

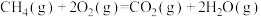


___________ 
③




___________ 
④煤作为燃料有2种途径:
途径1——直接燃烧:

途径2——先制水煤气:

再燃烧水煤气;

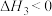
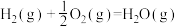
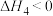
 、
、 、
、 、
、 的关系式是
的关系式是___________ 。
(1)书写下列反应的热化学方程式。(每个热化学方程式3分)
①1L1mol/L稀盐酸跟1L1mol/LNaOH溶液发生中和反应放出57.3kJ热量。
②24
 与足量
与足量 反应生成
反应生成 和
和 ,吸收262.6kJ热量。
,吸收262.6kJ热量。③已知16g固体硫完全燃烧时放出148.4kJ的热量,写出表示硫的燃烧的热化学方程式:
④如图是298K、101kPa时,
 与
与 反应过程中能量变化的曲线图。该反应的热化学方程式为:
反应过程中能量变化的曲线图。该反应的热化学方程式为: 
(2)比较下列各组热化学方程式中
 的大小关系。
的大小关系。①
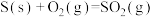

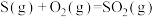



②
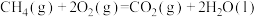

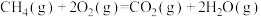



③






④煤作为燃料有2种途径:
途径1——直接燃烧:


途径2——先制水煤气:


再燃烧水煤气;

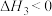
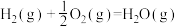
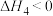
 、
、 、
、 、
、 的关系式是
的关系式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】写出下列反应的热化学方程式
(1)25℃ 1.01×105Pa下,1g 硫粉在氧气中充分燃烧放出 9.36kJ热量__________
(2)当10g丁烷完全燃烧生成CO2和液态水时,放出热量为500kJ,写出丁烷燃烧的热化学方程式:__________
(3)1mol C与1mol水蒸气反应生成1mol CO和1mol H2,吸热131.5kJ:_______ 。
(4)3 molNO2气体溶于水生成HNO3和NO气体,放出138kJ热量__________
(1)25℃ 1.01×105Pa下,1g 硫粉在氧气中充分燃烧放出 9.36kJ热量
(2)当10g丁烷完全燃烧生成CO2和液态水时,放出热量为500kJ,写出丁烷燃烧的热化学方程式:
(3)1mol C与1mol水蒸气反应生成1mol CO和1mol H2,吸热131.5kJ:
(4)3 molNO2气体溶于水生成HNO3和NO气体,放出138kJ热量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)常温下0.1mol/LNH4Cl溶液:
①溶液显酸性,用离子方程式解释:____ 。
②四种离子浓度大小排序____ ;电荷守恒关系____ 。
③c(Cl-)=c______ +c______ =0.1mol/L
④向溶液中滴加氨水至pH=7,则根据电荷守恒,c(NH )
)___ c(Cl-)(填“>”“<”或“=”,下同)。
(2)向20mL0.1mol/L氨水中滴加0.1mol/LHClVmL:
①当V=20,反应后溶液的溶质为____ ,显____ 性。
②当pH=7时,V____ 20。
③V=10时,溶质是NH4Cl和NH3·H2O(1:1),溶液显碱性,c(NH )
)____ c(Cl-)。
(3)配制FeCl3溶液时,先将FeCl3溶于浓盐酸,再稀释至指定浓度。结合平衡移动原理说明浓盐酸的作用:___ 。
(1)常温下0.1mol/LNH4Cl溶液:
①溶液显酸性,用离子方程式解释:
②四种离子浓度大小排序
③c(Cl-)=c
④向溶液中滴加氨水至pH=7,则根据电荷守恒,c(NH
 )
)(2)向20mL0.1mol/L氨水中滴加0.1mol/LHClVmL:
①当V=20,反应后溶液的溶质为
②当pH=7时,V
③V=10时,溶质是NH4Cl和NH3·H2O(1:1),溶液显碱性,c(NH
 )
)(3)配制FeCl3溶液时,先将FeCl3溶于浓盐酸,再稀释至指定浓度。结合平衡移动原理说明浓盐酸的作用:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】表述以下事实:
(1)碳酸钠溶液显碱性的原因___________ (用离子方程式表示)。
(2)①实验室配制的CuSO4溶液,常常出现浑浊,可采取在配制时加入少量___________ 防止浑浊
②泡沫灭火器中盛放的灭火剂包括Al2(SO4)3溶液(约1 mol/L)、NaHCO3溶液(约1 mol/L)及起泡剂。使用时发生反应的离子方程式是___________ 。
(3)在配制FeCl3溶液时,加入少许浓盐酸,其目的是:___________ ;如果不断加热FeCl3溶液,蒸干其水分并灼烧固体,最后得到的物质是___________ 。
(1)碳酸钠溶液显碱性的原因
(2)①实验室配制的CuSO4溶液,常常出现浑浊,可采取在配制时加入少量
②泡沫灭火器中盛放的灭火剂包括Al2(SO4)3溶液(约1 mol/L)、NaHCO3溶液(约1 mol/L)及起泡剂。使用时发生反应的离子方程式是
(3)在配制FeCl3溶液时,加入少许浓盐酸,其目的是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在0.5mol·L-1的NaHCO3溶液中滴入酚酞,溶液变红。试回答有关问题:
(1)该溶液中HCO3-的电离程度__________ (填“大于”、“小于”或“等于”)HCO3-的水解程度。溶液中Na+、HCO3-、CO32-、H+、OH-离子的浓度由大到小的顺序为______________ 。
(2)某温度下纯水中的c(H+)= 2×10-7mol/L,则此时溶液中的c(OH-)=_________ ;若温度不变,滴入稀盐酸,使c(H+)= 5×10-4mol/L,则溶液中c(OH-)=____________ ,此时溶液中由水电离产生的c(H+)= _________ 。
(3)物质的量浓度均为0.1 mol/L的下列溶液:①KNO3、②Na2CO3、③NaHCO3、④HCl 、⑤CH3COOH、⑥NaOH 、⑦Ba(OH)2、⑧NH4Cl, pH 由大到小的顺序为________________
(1)该溶液中HCO3-的电离程度
(2)某温度下纯水中的c(H+)= 2×10-7mol/L,则此时溶液中的c(OH-)=
(3)物质的量浓度均为0.1 mol/L的下列溶液:①KNO3、②Na2CO3、③NaHCO3、④HCl 、⑤CH3COOH、⑥NaOH 、⑦Ba(OH)2、⑧NH4Cl, pH 由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】有下列七种物质的溶液:①NaCl ②NH4Cl ③Na2CO3 ④CH3COONa ⑤CH3COOH ⑥NaHCO3。
(1)溶液呈酸性的有______ ,呈碱性的有____ 。
(2)分别写出②、④水解的离子方程式:_____ 、____ 。
(1)溶液呈酸性的有
(2)分别写出②、④水解的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电离平衡常数是衡量弱电解质电离程度强弱的量。已知如表数据。
(1)25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为__________________ 。
(2)25 ℃时,pH=3的CH3COOH溶液和pH=11的NaOH溶液混合,若所得溶液显酸性,则c(Na+)__________ c(CH3COO-)(填“>”、“<”或“=”)。
(3)NaCN溶液中通入少量CO2,所发生反应的化学方程式为___________ 。
(4)25 ℃时, pH=8的CH3COONa溶液中,c(Na+)-c(CH3COO-)=___________ 。
| 化学式 | 电离平衡常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
(1)25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为
(2)25 ℃时,pH=3的CH3COOH溶液和pH=11的NaOH溶液混合,若所得溶液显酸性,则c(Na+)
(3)NaCN溶液中通入少量CO2,所发生反应的化学方程式为
(4)25 ℃时, pH=8的CH3COONa溶液中,c(Na+)-c(CH3COO-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】全球气候变化对全球人类社会构成重大威胁。政府气候变化专门委员会(IPCC)报告认为,为了避免极端危害,世界必须将全球变暖幅度控制在1.5℃以内。只有全球都在21世纪中叶实现温室气体净零排放,才能有可能实现这一目标。请根据二氧化碳的利用回答下列问题:
(1)CO2催化氢化制甲烷的研究过程如图1:
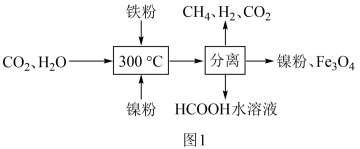
①上述过程中,加入铁粉的作用是__ 。
②HCOOH是CO2转化为CH4的中间体:CO2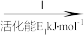 HCOOH
HCOOH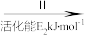 CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是
CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是__ 。
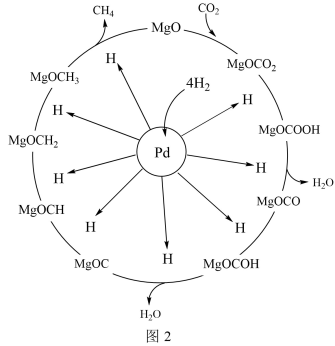
(2)一定条件下,Pd—Mg/SiO2催化剂可使CO2甲烷化从而变废为宝,其反应机理如图2所示,该反应的化学方程式为__ 。
(3)CO2加氢还可制备甲酸(HCOOH)。
①温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g) HCOOH(g) △H=-31.4kJ•mol-1 K=0.8。实验测得:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=
HCOOH(g) △H=-31.4kJ•mol-1 K=0.8。实验测得:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=__ k正。
②温度为T2℃时,k正=1.1k逆,则T2℃时平衡压强__ (填“>”“<”或“=”)T1℃时平衡压强。
(4)N—甲基二乙醇胺(用MDEA表示)水溶液具有吸收能力强、对设备腐蚀小等特点,MDEA吸收CO2的反应可以表示为:MDEA(aq)+CO2(g)+H2O(l) MDEAH+(aq)+HCO
MDEAH+(aq)+HCO (aq) △H。
(aq) △H。
①已知MDEA中的氮具有一元碱(类似于NH3)的性质,Kb=5.2×10-4,已知H2CO3的Ka1=4.3×10-7,Ka2=5.6×10-11,推测溶液MDEAHHCO3显__ 性(填酸,碱,中)。
②标准平衡常数Kθ可以表示平衡时各物质的浓度关系:如反应A(aq)+2B(g) C(g)+D(aq)的Kθ=
C(g)+D(aq)的Kθ=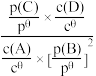 ,其中cθ=2mol/L,pθ为标准大气压,p(B)、p(C)分别为气体的分压,c为物质的量浓度,T℃时,在刚性密闭容器中有20L2.5mol/L的MDEA溶液,氮气(不参加反应)和二氧化碳混合气体14mol,起始气体总压为pθkPa,充分吸收后,MDEA浓度降低为20L2.2mol/L,二氧化碳的吸收率为60%,忽略反应过程中溶液的体积变化,则反应的标准平衡常数Kθ=
,其中cθ=2mol/L,pθ为标准大气压,p(B)、p(C)分别为气体的分压,c为物质的量浓度,T℃时,在刚性密闭容器中有20L2.5mol/L的MDEA溶液,氮气(不参加反应)和二氧化碳混合气体14mol,起始气体总压为pθkPa,充分吸收后,MDEA浓度降低为20L2.2mol/L,二氧化碳的吸收率为60%,忽略反应过程中溶液的体积变化,则反应的标准平衡常数Kθ=__ (计算结果保留两位小数)。
(5)设计二氧化碳熔盐捕获及电化学转化装置示意图如图:
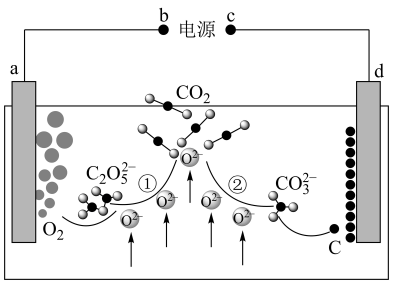
a极的电极反应式为__ 。
(1)CO2催化氢化制甲烷的研究过程如图1:

①上述过程中,加入铁粉的作用是
②HCOOH是CO2转化为CH4的中间体:CO2
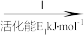 HCOOH
HCOOH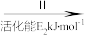 CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是
CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少,原因是(2)一定条件下,Pd—Mg/SiO2催化剂可使CO2甲烷化从而变废为宝,其反应机理如图2所示,该反应的化学方程式为

(3)CO2加氢还可制备甲酸(HCOOH)。
①温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g)
 HCOOH(g) △H=-31.4kJ•mol-1 K=0.8。实验测得:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=
HCOOH(g) △H=-31.4kJ•mol-1 K=0.8。实验测得:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=②温度为T2℃时,k正=1.1k逆,则T2℃时平衡压强
(4)N—甲基二乙醇胺(用MDEA表示)水溶液具有吸收能力强、对设备腐蚀小等特点,MDEA吸收CO2的反应可以表示为:MDEA(aq)+CO2(g)+H2O(l)
 MDEAH+(aq)+HCO
MDEAH+(aq)+HCO (aq) △H。
(aq) △H。①已知MDEA中的氮具有一元碱(类似于NH3)的性质,Kb=5.2×10-4,已知H2CO3的Ka1=4.3×10-7,Ka2=5.6×10-11,推测溶液MDEAHHCO3显
②标准平衡常数Kθ可以表示平衡时各物质的浓度关系:如反应A(aq)+2B(g)
 C(g)+D(aq)的Kθ=
C(g)+D(aq)的Kθ=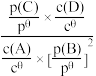 ,其中cθ=2mol/L,pθ为标准大气压,p(B)、p(C)分别为气体的分压,c为物质的量浓度,T℃时,在刚性密闭容器中有20L2.5mol/L的MDEA溶液,氮气(不参加反应)和二氧化碳混合气体14mol,起始气体总压为pθkPa,充分吸收后,MDEA浓度降低为20L2.2mol/L,二氧化碳的吸收率为60%,忽略反应过程中溶液的体积变化,则反应的标准平衡常数Kθ=
,其中cθ=2mol/L,pθ为标准大气压,p(B)、p(C)分别为气体的分压,c为物质的量浓度,T℃时,在刚性密闭容器中有20L2.5mol/L的MDEA溶液,氮气(不参加反应)和二氧化碳混合气体14mol,起始气体总压为pθkPa,充分吸收后,MDEA浓度降低为20L2.2mol/L,二氧化碳的吸收率为60%,忽略反应过程中溶液的体积变化,则反应的标准平衡常数Kθ=(5)设计二氧化碳熔盐捕获及电化学转化装置示意图如图:

a极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.回答下列问题:
(1)在实验室中配制FeCl3溶液时,配制方法是将FeCl3晶体溶于____ 中,然后加水稀释到所需浓度,这样操作的目的是____ 。
(2)如果盐的水解程度很大,则可用于无机化合物的制备。例如用TiCl4制备TiO2的反应可表示为:____ ,将所得产物TiO2·xH2O焙烧得到TiO2。
Ⅱ.以废旧铅酸蓄电池中的含铅废料和H2SO4为原料,可以制取高纯PbO,从而实现铅的再生利用。在此过程中涉及如下两个反应:
①2Fe2++PbO2+4H++SO =2Fe3++PbSO4+2H2O
=2Fe3++PbSO4+2H2O
②2Fe3++Pb+SO =2Fe2++PbSO4
=2Fe2++PbSO4
(3)写出Pb与PbO2反应生成PbSO4的化学方程式____ 。
(4)在上述过程中,Fe2+的作用是____ 。
(5)下列实验方案,可证实上述过程,请将方案补充完整。
a.向酸化的FeSO4溶液中加入____ 溶液,溶液几乎无色,再加入少量PbO2,溶液变红。
b.向a得到的溶液中加入____ 溶液恢复原来的颜色。
(1)在实验室中配制FeCl3溶液时,配制方法是将FeCl3晶体溶于
(2)如果盐的水解程度很大,则可用于无机化合物的制备。例如用TiCl4制备TiO2的反应可表示为:
Ⅱ.以废旧铅酸蓄电池中的含铅废料和H2SO4为原料,可以制取高纯PbO,从而实现铅的再生利用。在此过程中涉及如下两个反应:
①2Fe2++PbO2+4H++SO
 =2Fe3++PbSO4+2H2O
=2Fe3++PbSO4+2H2O②2Fe3++Pb+SO
 =2Fe2++PbSO4
=2Fe2++PbSO4(3)写出Pb与PbO2反应生成PbSO4的化学方程式
(4)在上述过程中,Fe2+的作用是
(5)下列实验方案,可证实上述过程,请将方案补充完整。
a.向酸化的FeSO4溶液中加入
b.向a得到的溶液中加入
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铬是人体必须的微量元素,在人体代谢中发挥着特殊作用。回答下列问题:
(1)金属铬可以通过焦炭高温还原铬铁矿(FeCr2O4)制取,同时生成一种有毒的气体,该反应的化学方程式为______ 。
(2)①取冶炼所得的金属铬溶解在盐酸中制取CrCl3溶液,其中混有FeCl2杂质,请完成除杂方案:向溶液中加入足量NaOH溶液,过滤,向滤液中______ ,过滤,将固体溶解在稀盐酸中(已知Cr(OH)3是两性氢氧化物)。
②由CrCl3溶液得到CrCl3•6H2O,除去其结晶水的操作是______ 。
(3)Cr3+在碱性条件下易被氧化成CrO ,写出向CrCl3溶液中加入氨水和过氧化氢发生反应的离子方程式
,写出向CrCl3溶液中加入氨水和过氧化氢发生反应的离子方程式______ 。
(4)CrO 在酸性条件下可转化为Cr2O
在酸性条件下可转化为Cr2O ,Cr2O
,Cr2O 可以用来检验H2O2,原理是Cr2O
可以用来检验H2O2,原理是Cr2O +4H2O2+2H+
+4H2O2+2H+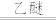 2CrO5(蓝色)+5H2O。
2CrO5(蓝色)+5H2O。
①CrO5中铬元素为+6价,其中过氧键的数目为______ 。
②酸化重铬酸钾选用的酸为______ (填标号)。
a.稀盐酸 b.稀硫酸 c.氢碘酸 d.磷酸
(1)金属铬可以通过焦炭高温还原铬铁矿(FeCr2O4)制取,同时生成一种有毒的气体,该反应的化学方程式为
(2)①取冶炼所得的金属铬溶解在盐酸中制取CrCl3溶液,其中混有FeCl2杂质,请完成除杂方案:向溶液中加入足量NaOH溶液,过滤,向滤液中
②由CrCl3溶液得到CrCl3•6H2O,除去其结晶水的操作是
(3)Cr3+在碱性条件下易被氧化成CrO
 ,写出向CrCl3溶液中加入氨水和过氧化氢发生反应的离子方程式
,写出向CrCl3溶液中加入氨水和过氧化氢发生反应的离子方程式(4)CrO
 在酸性条件下可转化为Cr2O
在酸性条件下可转化为Cr2O ,Cr2O
,Cr2O 可以用来检验H2O2,原理是Cr2O
可以用来检验H2O2,原理是Cr2O +4H2O2+2H+
+4H2O2+2H+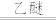 2CrO5(蓝色)+5H2O。
2CrO5(蓝色)+5H2O。①CrO5中铬元素为+6价,其中过氧键的数目为
②酸化重铬酸钾选用的酸为
a.稀盐酸 b.稀硫酸 c.氢碘酸 d.磷酸
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
【推荐3】铜是人类发现最早并广泛使用的一种金属。回答下列问题:
(1)实验室使用稀硫酸和H2O2溶解铜片,该反应的化学方程式为__________________ 。
(2)电子工业使用FeCl3溶液刻蚀印刷电路板铜箔,写出该过程的离子方程式____________ 。配制的FeCl3溶液应保持_______ (填“酸性”“碱性”或“中性”),原因是_____________ 。
(3)溶液中Cu2+的浓度可采用碘量法测得:
①2Cu2++5I-=2CuI↓+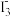 ②I3- +2
②I3- +2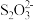 =3I-+2
=3I-+2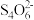
反应①中的氧化剂为_____________ 。现取20.00 mL含Cu2+的溶液,加入足量KI充分反应后,用0.1000 mol·L¯1 Na2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液25.00 mL,此溶液中Cu2+的浓度为_______ mol·L¯1。
(1)实验室使用稀硫酸和H2O2溶解铜片,该反应的化学方程式为
(2)电子工业使用FeCl3溶液刻蚀印刷电路板铜箔,写出该过程的离子方程式
(3)溶液中Cu2+的浓度可采用碘量法测得:
①2Cu2++5I-=2CuI↓+
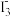 ②I3- +2
②I3- +2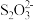 =3I-+2
=3I-+2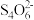
反应①中的氧化剂为
您最近一年使用:0次



