不同温度下,水的离子积常数如下所示。
下列说法不正确 的是
| T/℃ | 0 | 10 | 20 | 25 | 40 | 50 | 90 | 100 |
| Kw/10-14 | 0.1 | 0.3 | 0.7 | 1.0 | 2.9 | 5.3 | 37.1 | 54.5 |
| A.水的电离为吸热过程 |
| B.25℃,纯水中c(H+)=c(OH-)=10-7 mol/L |
| C.90℃,0.1 mol/LNaCl溶液的pH<7,呈中性 |
| D.pH=5的稀盐酸溶液中c(OH-)一定为10-9mol/L |
22-23高二上·北京东城·期末 查看更多[8]
北京市东城区2022-2023学年高二上学期期末统一检测化学试卷(已下线)第11讲 水的电离 溶液的酸碱性与pH-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)第三章 水溶液中的离子反应与平衡 第二节 水的电离和溶液的pH 第1课时 水的电离 溶液的酸碱性与pH河南省实验中学2023-2024学年高二上学期期中考试化学试题北京市第一六一中学2023-2024学年高二上学期期中阶段练习化学试题北京市第五十五中学2023-2024学年高二上学期12月月考调研化学试题北京市大兴区兴华中学2023-2024学年高二上学期期中考试化学试题湖南省长沙市德成学校2023-2024学年高二上学期12月月考化学试题
更新时间:2023-01-05 23:59:43
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在一定条件下,下列叙述与图像对应正确的是


A.图1表示 时, 时, 在水溶液中的沉淀溶解平衡曲线, 在水溶液中的沉淀溶解平衡曲线, 的 的 为 为 |
B.图2表示不同温度下水中 和 和 的浓度变化曲线,图中 的浓度变化曲线,图中 点对应温度高于 点对应温度高于 点 点 |
C.图3表示某温度下向 溶液中逐滴加入 溶液中逐滴加入 溶液,该滴定过程宜选用甲基橙作指示剂 溶液,该滴定过程宜选用甲基橙作指示剂 |
D.图4表示氢氟酸为弱酸,且 点对应 点对应 比 比 点对应 点对应 大 大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,用0.2mol•L-1盐酸滴定25.00mL0.2mol•L-1某弱碱ROH溶液,所得溶液pH、R+和ROH的物质的量分数与滴加盐酸体积的关系如图所示。下列叙述不正确的是

| A.曲线①代表φ(ROH),曲线②代表φ(R+) |
| B.b点溶液中存在c(Cl-)<c(R+)=c(ROH) |
| C.ROH的电离平衡常数为1.0×10-9 |
| D.a、b、c三点的溶液,水的电离程度a<b<c |
您最近一年使用:0次
单选题
|
适中
(0.65)
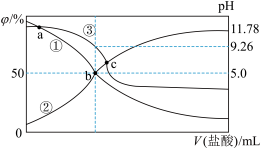
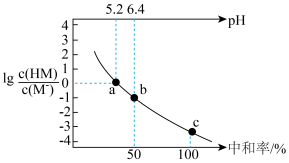
【推荐1】HM是一种一元弱酸,常温下向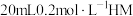 溶液中逐滴加入浓度为
溶液中逐滴加入浓度为 的
的 溶液,溶液中
溶液,溶液中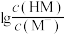 、
、 、中和率(中和率
、中和率(中和率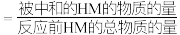 )的变化如图所示。下列说法错误的是
)的变化如图所示。下列说法错误的是
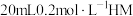 溶液中逐滴加入浓度为
溶液中逐滴加入浓度为 的
的 溶液,溶液中
溶液,溶液中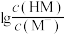 、
、 、中和率(中和率
、中和率(中和率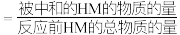 )的变化如图所示。下列说法错误的是
)的变化如图所示。下列说法错误的是
A.HM的电离常数为 |
B.b点时,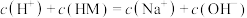 |
C.c点时,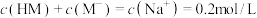 |
D.溶液中水电离出 : :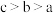 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知常温时HClO的Ka=3.0×10-8,HF的Ka=3.5×10-4。现将pH和体积都相同的次氯酸和氢氟酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示,下列叙述正确的是( )


| A.曲线Ⅰ为次氯酸稀释时pH变化曲线 |
| B.取a点的两种酸溶液,中和相同体积、相同浓度的NaOH溶液,消耗氢氟酸的体积较小 |
| C.b点溶液中水的电离程度比c点溶液中水的电离程度小 |
D.从b点到d点,溶液中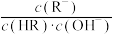 保持不变(HR代表HClO或HF) 保持不变(HR代表HClO或HF) |
您最近一年使用:0次

 H++OH-,常温下,Kw 的数值为 1×10-14.下列说法不正确的是
H++OH-,常温下,Kw 的数值为 1×10-14.下列说法不正确的是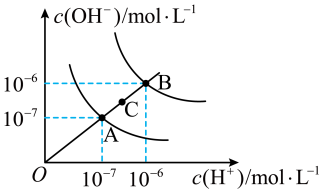
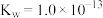 ,则此时
,则此时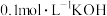 溶液的pH为12
溶液的pH为12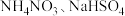 或
或 ,都能促进水的电离
,都能促进水的电离

