水存在电离平衡:H2O H++OH-,常温下,Kw 的数值为 1×10-14.下列说法不正确的是
H++OH-,常温下,Kw 的数值为 1×10-14.下列说法不正确的是
 H++OH-,常温下,Kw 的数值为 1×10-14.下列说法不正确的是
H++OH-,常温下,Kw 的数值为 1×10-14.下列说法不正确的是| A.常温下,水电离出的 c(H+)=c(OH-)=10-7mol·L-1 |
| B.向水中加入NaCl,H+与 Cl-结合生成 HCl,使水的电离平衡向正反应方向移动 |
| C.向水中加入HCl或者NaOH,水的电离平衡都向逆反应方向移动 |
| D.改变温度,Kw 也会发生改变 |
20-21高二上·北京昌平·期末 查看更多[7]
第1课时 水的电离 溶液的酸碱性与 pH辽宁省鞍山市普通高中2022-2023学年高二下学期第一次月考化学(A卷)试题(已下线)水溶液中的离子反应与平衡——课时3水的电离与溶液的酸碱性北京市第四十三中学2021-2022学年高二上学期12月月考化学试题(已下线)第16讲 水的电离-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)四川省射洪中学校2020—2021学年高二下学期入学考试化学试题北京市昌平区2020-2021学年高二上学期期末考试化学试题
更新时间:2021-02-20 15:21:39
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
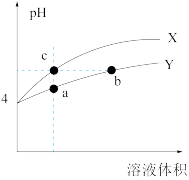
【推荐1】在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列关于离子共存说法中正确的是


| A.d点对应的溶液中大量存在:Na+、K+、ClO-、Cl- |
B.b点对应的溶液中大量存在:Fe2+、Ba2+、K+、 |
C.c点对应的溶液中大量存在:Na+、Ba2+、Cl-、 |
D.a点对应的溶液中大量存在: 、Na+、I-、Fe3+ 、Na+、I-、Fe3+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,向 浓度均为
浓度均为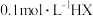 和
和 的混合溶液中滴加
的混合溶液中滴加 的
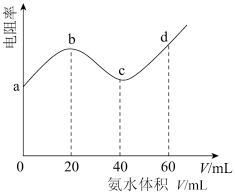
的 ,测得混合溶液的电阻率(溶液的电阻率越大,导电能力越弱)与加入氨水的体积
,测得混合溶液的电阻率(溶液的电阻率越大,导电能力越弱)与加入氨水的体积 的关系如图所示(忽略混合时体积变化),下列说法正确的是
的关系如图所示(忽略混合时体积变化),下列说法正确的是
 浓度均为
浓度均为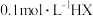 和
和 的混合溶液中滴加
的混合溶液中滴加 的
的 ,测得混合溶液的电阻率(溶液的电阻率越大,导电能力越弱)与加入氨水的体积
,测得混合溶液的电阻率(溶液的电阻率越大,导电能力越弱)与加入氨水的体积 的关系如图所示(忽略混合时体积变化),下列说法正确的是
的关系如图所示(忽略混合时体积变化),下列说法正确的是
A.常温下,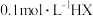 的 的 比同浓度 比同浓度 的 的 大 大 |
B.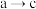 过程中水的电离程度先减小后增大 过程中水的电离程度先减小后增大 |
C. 点溶液中, 点溶液中,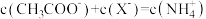 |
D. 点时, 点时,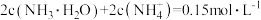 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列解释实验事实的方程式正确的是
A. 溶液滴加氨水产生白色胶状沉淀: 溶液滴加氨水产生白色胶状沉淀: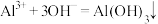 |
B. 时,测得纯水中 时,测得纯水中 : :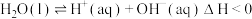 |
C.除去 中少量的 中少量的 的方法是加入足量饱和的 的方法是加入足量饱和的 溶液中充分搅拌、过滤、洗涤: 溶液中充分搅拌、过滤、洗涤: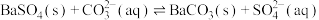 |
D.碳酸钠溶液滴入酚酞变红: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在25℃水中加入下列物质,不会使水的电离平衡发生移动的是
| A.KCl | B.Na2CO3 | C.硫酸 | D.热水 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】室温下,水的电离达到平衡:H2O⇌H++OH-。下列叙述正确的是
| A.将水加热,平衡向正反应方向移动,Kw不变 |
| B.向水中加入少量NaCl固体,平衡向正反应方向移动,c(OH-)=c(H+) |
| C.向水中加入少量NaOH固体,平衡向逆反应方向移动,c(OH-)降低 |
| D.向水中加入少量盐酸,平衡向逆反应方向移动,c(H+)增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述正确的是
A.室温下, 的盐酸与 的盐酸与 的氨水等体积混合后 的氨水等体积混合后 |
B.室温下,某溶液由水电离出来的 的浓度为 的浓度为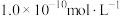 ,则该溶液的 ,则该溶液的 |
C.100℃时,将 的盐酸与 的盐酸与 的 的 溶液等体积混合,溶液显中性 溶液等体积混合,溶液显中性 |
D.常温下,硫酸铝在水溶液中的电离方程式为: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】对水的电离平衡不会产生影响的粒子是( )
A.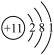 | B.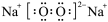 | C.O=C=O | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】水是最宝贵的资源之一,下列表述正确的是
A. 的水一定呈酸性 的水一定呈酸性 |
B.温度升高,纯水中的 增大, 增大, 减小 减小 |
| C.一定温度下,向水中加入酸或碱,都可抑制水的电离,使水的离子积减小 |
D.25℃时某溶液中由水电离产生的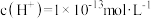 ,该溶液可能显酸性 ,该溶液可能显酸性 |
您最近一年使用:0次

 mol/L
mol/L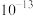 mol/L
mol/L 、
、 、
、 、
、
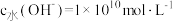 的溶液中:
的溶液中: 、
、 、
、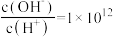 的溶液中:
的溶液中: 、
、 、
、 、
、

