室温下,水的电离达到平衡:H2O⇌H++OH-。下列叙述正确的是
| A.将水加热,平衡向正反应方向移动,Kw不变 |
| B.向水中加入少量NaCl固体,平衡向正反应方向移动,c(OH-)=c(H+) |
| C.向水中加入少量NaOH固体,平衡向逆反应方向移动,c(OH-)降低 |
| D.向水中加入少量盐酸,平衡向逆反应方向移动,c(H+)增大 |
更新时间:2023-12-28 20:38:30
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】在一定条件下的密闭容器中发生反应 ,当达到平衡时,下列各项措施中,既能提高反应速率又能提高乙烷平衡转化率的是
,当达到平衡时,下列各项措施中,既能提高反应速率又能提高乙烷平衡转化率的是
 ,当达到平衡时,下列各项措施中,既能提高反应速率又能提高乙烷平衡转化率的是
,当达到平衡时,下列各项措施中,既能提高反应速率又能提高乙烷平衡转化率的是| A.减小容器的容积 | B.升高反应的温度 | C.分离出部分氢气 | D.恒容下通入氦气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是( )
| A.“可燃冰”是将水变为油的新型燃料,具有热值高、无污染等优点 |
| B.淀粉、纤维素和油脂都是天然高分子化合物 |
C.N2(g)+3H2(g)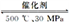 2NH3(g)采用高温、高压的条件有利于提高氨的产量 2NH3(g)采用高温、高压的条件有利于提高氨的产量 |
| D.催化剂能够加快化学反应速率是由于其参与了化学反应并改变了反应的路径,使反应所需的活化能降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】CH4与CO2重整生成H2和CO的过程中主要发生下列反应:
Ⅰ.CH4(g)+CO2(g) 2H2(g)+2CO(g) ΔH=+247.1 kJ·mol-1
2H2(g)+2CO(g) ΔH=+247.1 kJ·mol-1
Ⅱ.H2(g)+CO2(g) H2O(g)+CO(g) ΔH=+41.2 kJ·mol-1
H2O(g)+CO(g) ΔH=+41.2 kJ·mol-1
在恒压、反应物起始投料比n(CH4):n(CO2)=1:1条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的个数是
②800 K下,改变起始投料比,可使甲烷的转化率由X点提高至Y点
③曲线A表示CH4的平衡转化率
④相同条件下,使用高效催化剂不能使曲线A和曲线B相重叠
Ⅰ.CH4(g)+CO2(g)
 2H2(g)+2CO(g) ΔH=+247.1 kJ·mol-1
2H2(g)+2CO(g) ΔH=+247.1 kJ·mol-1Ⅱ.H2(g)+CO2(g)
 H2O(g)+CO(g) ΔH=+41.2 kJ·mol-1
H2O(g)+CO(g) ΔH=+41.2 kJ·mol-1在恒压、反应物起始投料比n(CH4):n(CO2)=1:1条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的个数是
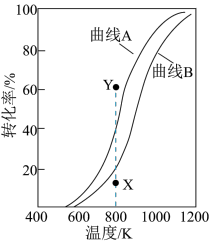
②800 K下,改变起始投料比,可使甲烷的转化率由X点提高至Y点
③曲线A表示CH4的平衡转化率
④相同条件下,使用高效催化剂不能使曲线A和曲线B相重叠
| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】用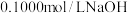 溶液滴定
溶液滴定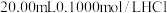 溶液过程中的
溶液过程中的 变化如下图所示。已知
变化如下图所示。已知 。下列说法错误的是
。下列说法错误的是

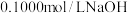 溶液滴定
溶液滴定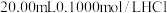 溶液过程中的
溶液过程中的 变化如下图所示。已知
变化如下图所示。已知 。下列说法错误的是
。下列说法错误的是
A.b点时,加入极少量 溶液都会引起 溶液都会引起 的突变 的突变 |
| B.滴定过程中,水的电离程度不断减小 |
C.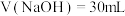 时, 时, |
D.选指示剂时,其变色范围应在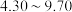 之间 之间 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】如图三条曲线表示不同温度下水的离子积常数,下列说法不正确的是


A.图中温度,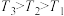 |
| B.C点可能是显酸性的溶液 |
C.四中五点 间的关系: 间的关系: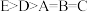 |
D.图中pH关系: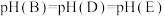 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,向苹果酸[结构简式为HOOCCH(OH)CH2COOH,用H2A表示]溶液中滴加NaOH溶液,所得混合溶液中 或
或 与溶液pH的变化关系如图所示。下 列叙述错误的是
与溶液pH的变化关系如图所示。下 列叙述错误的是

 或
或 与溶液pH的变化关系如图所示。下 列叙述错误的是
与溶液pH的变化关系如图所示。下 列叙述错误的是
A.曲线N表示 随pH的变化关系 随pH的变化关系 |
| B.水的电离程度: c>b>a |
| C.d点溶液中: c(Na+)>c(A2- )> c(H2A)>c(HA- ) |
| D.苹果酸的两级电离常数的乘积Ka1·Ka2的数量级为10 -8 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,向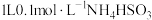 溶液中加入NaOH固体,
溶液中加入NaOH固体, 、
、 、
、 、
、 粒子浓度的变化情况如图所示(过程中溶液体积和温度保持不变)。
粒子浓度的变化情况如图所示(过程中溶液体积和温度保持不变)。

已知:常温下, 的
的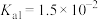 ,
,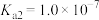 ,
,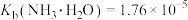 。下列说法错误的是
。下列说法错误的是
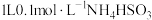 溶液中加入NaOH固体,
溶液中加入NaOH固体, 、
、 、
、 、
、 粒子浓度的变化情况如图所示(过程中溶液体积和温度保持不变)。
粒子浓度的变化情况如图所示(过程中溶液体积和温度保持不变)。
已知:常温下,
 的
的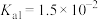 ,
,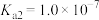 ,
,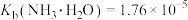 。下列说法错误的是
。下列说法错误的是A.曲线b、d分别表示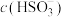 、 、 的变化情况 的变化情况 |
| B.随着NaOH的加入,水的电离程度先增大后减小 |
C.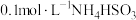 溶液中存在 溶液中存在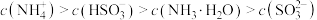 |
D.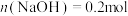 时溶液中存在 时溶液中存在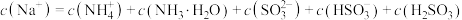 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】有关化学反应原理的下列说法中正确的是
A. 溶液水解的离子方程式: 溶液水解的离子方程式: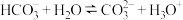 |
B.常温下,反应 不能自发进行,则该反应的 不能自发进行,则该反应的 |
| C.在酶催化淀粉水解反应中,温度越高淀粉水解速率越快 |
| D.常温下,向纯水中加入钠或氢氧化钠都能使水的电离平衡逆向移动,水离子积不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
A.碳酸氢根离子的电离方程式: HCO3-+H2O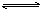 H3O++ CO32- H3O++ CO32- |
| B.从上到下,卤族元素的非金属性逐渐减弱,故氢卤酸的酸性依次减弱 |
| C.因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S |
| D.NaCl晶体中每个Na+同时吸引着6个Cl-,CsCl晶体中每个Cl-同时吸引着6个Cs+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】Cu2+与NH3可结合生成多种络合物,在水溶液中存在如下平衡: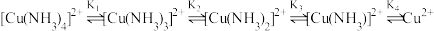 (K1、K2、K3、K4分别为每一步反应的化学平衡常数)。向某浓度的CuSO4溶液中滴加浓氨水,实验测得含Cu微粒的物质的量分布分数(δ)与溶液中游离氨的1gc(NH3)关系如图所示。下列说法正确的是
(K1、K2、K3、K4分别为每一步反应的化学平衡常数)。向某浓度的CuSO4溶液中滴加浓氨水,实验测得含Cu微粒的物质的量分布分数(δ)与溶液中游离氨的1gc(NH3)关系如图所示。下列说法正确的是
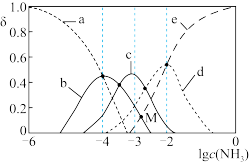
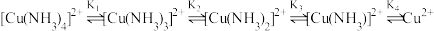 (K1、K2、K3、K4分别为每一步反应的化学平衡常数)。向某浓度的CuSO4溶液中滴加浓氨水,实验测得含Cu微粒的物质的量分布分数(δ)与溶液中游离氨的1gc(NH3)关系如图所示。下列说法正确的是
(K1、K2、K3、K4分别为每一步反应的化学平衡常数)。向某浓度的CuSO4溶液中滴加浓氨水,实验测得含Cu微粒的物质的量分布分数(δ)与溶液中游离氨的1gc(NH3)关系如图所示。下列说法正确的是
A.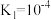 |
| B.曲线a表示[Cu(NH3)4]2+的物质的量分布分数曲线 |
C.lgc(NH3)=-3时,c(Cu2+)+c{[Cu(NH3)]2+}+ c{[Cu(NH3)2]2+}+ c{[Cu(NH3)3]2+}+ c{[Cu(NH3)4]2+}=0.5[c(OH-)-c(H+)-c( )] )] |
D.M点时,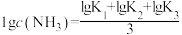 |
您最近一年使用:0次



