高炉废渣在循环利用前需要脱硫(硫元素主要存在形式为 ,少量为
,少量为 和
和 )处理。
)处理。
(1)高温“两段法”氧化脱硫。第一阶段在空气中,相关热化学方程式如下:
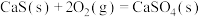
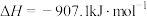

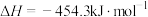
①第二阶段在惰性气体中,反应 的
的
________  。
。
②整个过程中, 完全转化生成
完全转化生成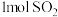 ,转移的电子为
,转移的电子为________  。
。
③生成的 用硫酸铜溶液吸收电解氧化,总反应为
用硫酸铜溶液吸收电解氧化,总反应为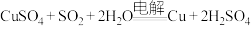 。写出电解时阳极的电极反应式
。写出电解时阳极的电极反应式________________ 。
(2)喷吹 脱硫。用水浸取炉渣,通入适量的
脱硫。用水浸取炉渣,通入适量的 ,将硫元素以含硫气体形式脱去。当
,将硫元素以含硫气体形式脱去。当 的流量、温度一定时,渣-水混合液的
的流量、温度一定时,渣-水混合液的 、含碳元素各种微粒(
、含碳元素各种微粒( 、
、 、
、 )的分布随喷吹时间变化如图1和图2所示。
)的分布随喷吹时间变化如图1和图2所示。

① 第二步电离的电离常数为
第二步电离的电离常数为 ,则
,则
________ (填数值,已知 )。
)。
②通入
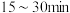 时,混合液中发生的主要脱硫反应的离子方程式为
时,混合液中发生的主要脱硫反应的离子方程式为_____________ 。
(3)硫酸工业生产中 吸收率与进入吸收塔的硫酸浓度和温度关系如图3,由图可知吸收
吸收率与进入吸收塔的硫酸浓度和温度关系如图3,由图可知吸收 所用硫酸的适宜浓度为98.3%,温度为
所用硫酸的适宜浓度为98.3%,温度为_____ ,而工业生产中一般采用60℃的可能原因是____________ 。
 ,少量为
,少量为 和
和 )处理。
)处理。(1)高温“两段法”氧化脱硫。第一阶段在空气中,相关热化学方程式如下:
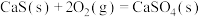
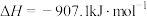

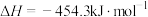
①第二阶段在惰性气体中,反应
 的
的
 。
。②整个过程中,
 完全转化生成
完全转化生成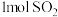 ,转移的电子为
,转移的电子为 。
。③生成的
 用硫酸铜溶液吸收电解氧化,总反应为
用硫酸铜溶液吸收电解氧化,总反应为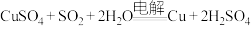 。写出电解时阳极的电极反应式
。写出电解时阳极的电极反应式(2)喷吹
 脱硫。用水浸取炉渣,通入适量的
脱硫。用水浸取炉渣,通入适量的 ,将硫元素以含硫气体形式脱去。当
,将硫元素以含硫气体形式脱去。当 的流量、温度一定时,渣-水混合液的
的流量、温度一定时,渣-水混合液的 、含碳元素各种微粒(
、含碳元素各种微粒( 、
、 、
、 )的分布随喷吹时间变化如图1和图2所示。
)的分布随喷吹时间变化如图1和图2所示。
①
 第二步电离的电离常数为
第二步电离的电离常数为 ,则
,则
 )。
)。②通入

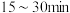 时,混合液中发生的主要脱硫反应的离子方程式为
时,混合液中发生的主要脱硫反应的离子方程式为(3)硫酸工业生产中
 吸收率与进入吸收塔的硫酸浓度和温度关系如图3,由图可知吸收
吸收率与进入吸收塔的硫酸浓度和温度关系如图3,由图可知吸收 所用硫酸的适宜浓度为98.3%,温度为
所用硫酸的适宜浓度为98.3%,温度为
更新时间:2023-01-09 12:10:37
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如下。

请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如下。
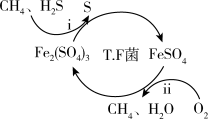
(1)过程i中H2S发生了________ (选填“氧化”或“还原”)反应。
(2)过程ⅱ的离子方程式是____________ 。
(3)已知:①Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
请结合以上信息,判断工业脱硫应选择的最佳pH范围____________ 。
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合下图回答问题。
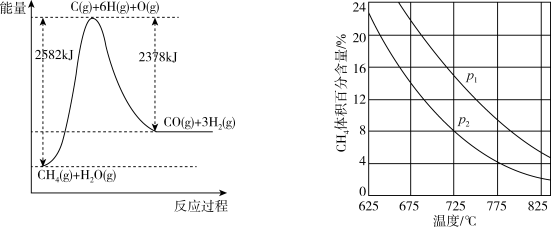
(4)①该过程的热化学方程式是__________________ 。
②比较压强p1和p2的大小关系:p1__ p2(选填“>”“<”或“=”)。
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.H2提纯:将CO2和H2分离得到H2的过程示意图如下。
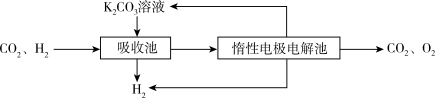
(5)①吸收池中发生反应的离子方程式是___________________ 。
②用化学语言解释K2CO3溶液的再生的原理:_____________________ 。

请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如下。

(1)过程i中H2S发生了
(2)过程ⅱ的离子方程式是
(3)已知:①Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
pH | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.4 | 2.7 | 3.0 |
Fe2+氧化速率/(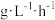 ) ) | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 | 6.2 | 5.6 |
请结合以上信息,判断工业脱硫应选择的最佳pH范围
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合下图回答问题。

(4)①该过程的热化学方程式是
②比较压强p1和p2的大小关系:p1
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.H2提纯:将CO2和H2分离得到H2的过程示意图如下。

(5)①吸收池中发生反应的离子方程式是
②用化学语言解释K2CO3溶液的再生的原理:
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】甲醇是一种可再生能源。工业上可用CO和 合成甲醇:
合成甲醇: 。一定条件下向2L的密闭容器中充入1mol CO和2mol
。一定条件下向2L的密闭容器中充入1mol CO和2mol  发生反应,CO的平衡转化率与温度、压强的关系如图所示:
发生反应,CO的平衡转化率与温度、压强的关系如图所示:
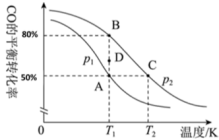
(1)该反应的△H_______ 0、△S_______ 0(填“>”“<”或“=”),_______ (填“低温”或“高温”)有利于该反应自发进行。
(2)生产中有利于增大CO平衡转化率的措施有_______ 。(至少写出3条)
(3)①A、B、C三点平衡常数 、
、 、
、 的大小关系是
的大小关系是_______ 。
②压强
_______  (填“>”“<”或“=”);若
(填“>”“<”或“=”);若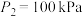 ,计算B点的
,计算B点的 =
=_______ 。(要求写出计算过程,结果保留2位有效数字; 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
③在 和
和 条件下,由D点到A点过程中,正、逆反应速率之间的关系:
条件下,由D点到A点过程中,正、逆反应速率之间的关系:
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
④比较B点和C点的逆反应速率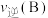
_______ 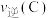 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
 合成甲醇:
合成甲醇: 。一定条件下向2L的密闭容器中充入1mol CO和2mol
。一定条件下向2L的密闭容器中充入1mol CO和2mol  发生反应,CO的平衡转化率与温度、压强的关系如图所示:
发生反应,CO的平衡转化率与温度、压强的关系如图所示:
(1)该反应的△H
(2)生产中有利于增大CO平衡转化率的措施有
(3)①A、B、C三点平衡常数
 、
、 、
、 的大小关系是
的大小关系是②压强

 (填“>”“<”或“=”);若
(填“>”“<”或“=”);若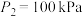 ,计算B点的
,计算B点的 =
= 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。③在
 和
和 条件下,由D点到A点过程中,正、逆反应速率之间的关系:
条件下,由D点到A点过程中,正、逆反应速率之间的关系:
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。④比较B点和C点的逆反应速率
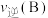
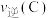 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】华为集团在通信网络、IT、智能终端和云服务等领域为客户提供有竞争力、安全可信赖的产品、解决方案与服务,与生态伙伴开放合作,持续为客户创造价值,释放个人潜能,丰富家庭生活,激发组织创新。华为坚持围绕客户需求持续创新,加大基础研究投入,厚积薄发,推动世界进步。其中MATE30手机采用锂离子电池,其正极材料为磷酸亚铁锂(LiFePO4),它具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用FeCl3、NH4H2PO4、LiCl和苯胺等作为原料制备。回答下列问题:
(1)在周期表中,与Li的化学性质最相似的邻族元素是________ ,该元素基态原子核外M层电子的自旋状态_______ (填“相同”或“相反”)。
(2)FeCl3中的化学键具有明显的共价性(类似于氯化铝),蒸汽状态下以双聚分子存在的FeCl3的结构式为____ ,其中Fe的配位数为____ 。
(3)苯胺(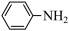 )的晶体类型是
)的晶体类型是_____ 。苯胺与甲苯(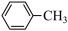 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是_______ 。
(4)NH4H2PO4中,电负性最高的元素是______ ;其中PO43-采用_______ 杂化。
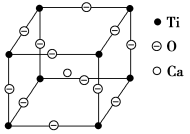
(5)如下图所示为高温超导领域里的一种化合物——钙钛矿的晶体结构,该结构是具有代表性的最小重复单位。该物质的化学式可表示为_____ ;若钙、钛、氧三元素的相对原子质量分别为a、b、c,晶体结构图中正方体边长(钛原子之间的距离)为d nm(1 nm=10-10Cm),则该晶体的密度为__ g·cm-3。
(1)在周期表中,与Li的化学性质最相似的邻族元素是
(2)FeCl3中的化学键具有明显的共价性(类似于氯化铝),蒸汽状态下以双聚分子存在的FeCl3的结构式为
(3)苯胺(
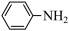 )的晶体类型是
)的晶体类型是 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是(4)NH4H2PO4中,电负性最高的元素是
(5)如下图所示为高温超导领域里的一种化合物——钙钛矿的晶体结构,该结构是具有代表性的最小重复单位。该物质的化学式可表示为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】已知25℃时,醋酸、氢硫酸、氢氰酸的电离平衡常数如下表:(单位省略)
(1)体积相同、 相同的三种酸溶液a.
相同的三种酸溶液a. ;b.
;b. ;c.
;c. 分别与同浓度的
分别与同浓度的 溶液完全中和,消耗
溶液完全中和,消耗 溶液的体积由大到小的排列顺序是(填字母)
溶液的体积由大到小的排列顺序是(填字母)_________ 。
(2)将浓度为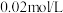 的
的 与
与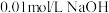 溶液等体积混合,测得混合洛液中
溶液等体积混合,测得混合洛液中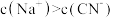 ,下列关系正确的是
,下列关系正确的是_________ 。
a. b.
b.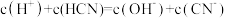 c.
c.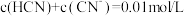
(3)25℃时,向 溶液中通入少量
溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为_________ ;
(4)25℃时,醋酸的电离常数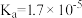 ,则该温度下
,则该温度下 的
的
_________ (保留一位小数)。
(5)25℃时, 的醋酸和
的醋酸和 的氢氧化钠等体积混合后溶液呈
的氢氧化钠等体积混合后溶液呈_________ (填“酸性”“中性”或“碱性”)
(6)25℃时,醋酸的电离常数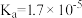 ,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的
,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的 ,则
,则 的电离常数
的电离常数
_________ 。
| 醋酸 | 氢硫酸 | 氢氰酸 |
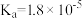 | 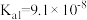 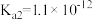 | 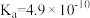 |
(1)体积相同、
 相同的三种酸溶液a.
相同的三种酸溶液a. ;b.
;b. ;c.
;c. 分别与同浓度的
分别与同浓度的 溶液完全中和,消耗
溶液完全中和,消耗 溶液的体积由大到小的排列顺序是(填字母)
溶液的体积由大到小的排列顺序是(填字母)(2)将浓度为
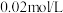 的
的 与
与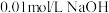 溶液等体积混合,测得混合洛液中
溶液等体积混合,测得混合洛液中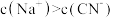 ,下列关系正确的是
,下列关系正确的是a.
 b.
b.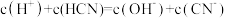 c.
c.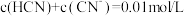
(3)25℃时,向
 溶液中通入少量
溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为(4)25℃时,醋酸的电离常数
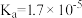 ,则该温度下
,则该温度下 的
的
(5)25℃时,
 的醋酸和
的醋酸和 的氢氧化钠等体积混合后溶液呈
的氢氧化钠等体积混合后溶液呈(6)25℃时,醋酸的电离常数
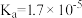 ,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的
,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的 ,则
,则 的电离常数
的电离常数
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】工业上以黄铁矿(主要成分为FeS2)为原料来制备硫酸,产生的含二氧化硫尾气和炉渣(主要成分为Fe2O3)经过资源化利用可减轻对环境的污染。
(1)工业制硫酸。沸腾炉中煅烧黄铁矿发生反应的化学方程式为_______ ,当有6 mol SO2生成时,转移电子_______ mol。
(2)生产焦亚硫酸钠(Na2S2O5)。Na2S2O5常用作食品的抗氧化剂,由NaHSO3过饱和溶液经结晶脱水制得,生产工艺流程如下:
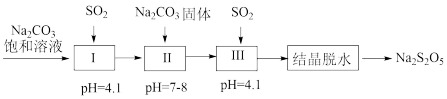
已知:H2SO3电离常数分别为Ka1=1.5×10-2、Ka2=1.0×10-7
H2CO3电离常数分别为Ka1=4.3×10-7、Ka2=5.6×10-11
生成Na2S2O5的化学方程式为2NaHSO3=Na2S2O5+H2O
①I中生成一种盐并放出气体,反应的离子方程式为_______ 。
②工艺中加入Na2CO3固体,并再次充入SO2的目的是_______ 。
③因为Na2S2O5具有还原性,导致产品中不可避免地存在Na2SO4,检验其中是否含有 的方法是
的方法是_______ 。
(3)由炉渣制备还原铁粉并分析纯度。利用CO与炉渣反应得到还原铁粉,得到的产品可用K2Cr2O7滴定分析法测定纯度。实验步骤如下:称取0.2240 g样品,加入过量稀硫酸充分溶解,用3.000×10−2 mol·L−1 K2Cr2O7溶液滴定至终点(滴定过程中 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液20.00 mL,计算该样品中还原铁粉的质量分数(写出计算过程)
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液20.00 mL,计算该样品中还原铁粉的质量分数(写出计算过程)_______ 。
(1)工业制硫酸。沸腾炉中煅烧黄铁矿发生反应的化学方程式为
(2)生产焦亚硫酸钠(Na2S2O5)。Na2S2O5常用作食品的抗氧化剂,由NaHSO3过饱和溶液经结晶脱水制得,生产工艺流程如下:

已知:H2SO3电离常数分别为Ka1=1.5×10-2、Ka2=1.0×10-7
H2CO3电离常数分别为Ka1=4.3×10-7、Ka2=5.6×10-11
生成Na2S2O5的化学方程式为2NaHSO3=Na2S2O5+H2O
①I中生成一种盐并放出气体,反应的离子方程式为
②工艺中加入Na2CO3固体,并再次充入SO2的目的是
③因为Na2S2O5具有还原性,导致产品中不可避免地存在Na2SO4,检验其中是否含有
 的方法是
的方法是(3)由炉渣制备还原铁粉并分析纯度。利用CO与炉渣反应得到还原铁粉,得到的产品可用K2Cr2O7滴定分析法测定纯度。实验步骤如下:称取0.2240 g样品,加入过量稀硫酸充分溶解,用3.000×10−2 mol·L−1 K2Cr2O7溶液滴定至终点(滴定过程中
 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液20.00 mL,计算该样品中还原铁粉的质量分数(写出计算过程)
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液20.00 mL,计算该样品中还原铁粉的质量分数(写出计算过程)
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】草酸(H2C2O4)是一种还原性二元酸,存在于菠菜等植物中。
已知:常温下,草酸的电离常数K1=5.4 × 10-2,K2=5.4 × 10-5;溶度积常数Ksp(CaC2O4)=2.34 × 10-9,Ksp(CaSO4)=9.10 × 10-6。
请回答下列问题:
(1)生活中,长期将豆腐与菠菜混合食用,容易损失钙元素且易患胆结石疾病。简述理由:________ 。
(2)写出草酸在水中的电离方程式:______________ 。
(3)已知KHC2O4溶液呈酸性,则溶液中c(H2C2O4)________ c( )(填“>”“<”或“=”,下同)。若0.1 mol·L-1 H2C2O4溶液中第二步电离的c(H+)=a mol·L-1,则0.1 mol·L-1KHC2O4溶液中
)(填“>”“<”或“=”,下同)。若0.1 mol·L-1 H2C2O4溶液中第二步电离的c(H+)=a mol·L-1,则0.1 mol·L-1KHC2O4溶液中 电离出来的c(H+)
电离出来的c(H+)____________ amol·L-1。
(4)常温下,将某浓度的1 mL H2C2O4溶液加蒸馏水稀释,其溶液pH与加水稀释后溶液体积的关系如图所示。

能代表H2C2O4溶液稀释情况的是曲线______________ (填“I”或“II”)。 在稀释该溶液过程中,下列物理量始终增大的是________________ (填字母代号)。
A.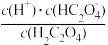 B.c(H+)·c(
B.c(H+)·c( )
)
C.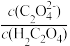 D.
D.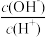
已知:常温下,草酸的电离常数K1=5.4 × 10-2,K2=5.4 × 10-5;溶度积常数Ksp(CaC2O4)=2.34 × 10-9,Ksp(CaSO4)=9.10 × 10-6。
请回答下列问题:
(1)生活中,长期将豆腐与菠菜混合食用,容易损失钙元素且易患胆结石疾病。简述理由:
(2)写出草酸在水中的电离方程式:
(3)已知KHC2O4溶液呈酸性,则溶液中c(H2C2O4)
 )(填“>”“<”或“=”,下同)。若0.1 mol·L-1 H2C2O4溶液中第二步电离的c(H+)=a mol·L-1,则0.1 mol·L-1KHC2O4溶液中
)(填“>”“<”或“=”,下同)。若0.1 mol·L-1 H2C2O4溶液中第二步电离的c(H+)=a mol·L-1,则0.1 mol·L-1KHC2O4溶液中 电离出来的c(H+)
电离出来的c(H+)(4)常温下,将某浓度的1 mL H2C2O4溶液加蒸馏水稀释,其溶液pH与加水稀释后溶液体积的关系如图所示。

能代表H2C2O4溶液稀释情况的是曲线
A.
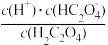 B.c(H+)·c(
B.c(H+)·c( )
)C.
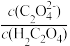 D.
D.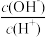
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】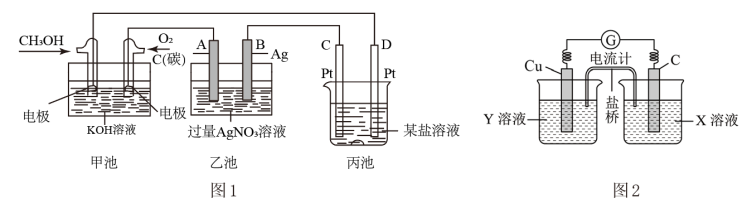
(1)如图1是一个化学过程的示意图。
①甲池中OH-移向______ 极(填“CH3OH”或“O2”)。
②写出通入CH3OH的电极的电极反应式_________ 。
③乙池中总反应的离子方程式____________ 。
④当乙池中B(Ag)极的质量增加5.40g,此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是________
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
(2)利用反应Cu+2FeCl3=CuCl2+2FeCl2设计成如图2所示原电池,回答下列问题:
①写出电极反应式:正极________ ;负极___________ 。
②图中X溶液是________ ,Y溶液是_________ 。
③原电池工作时,盐桥中的______ (填“阳”或“阴”)离子向X溶液方向移动。

(1)如图1是一个化学过程的示意图。
①甲池中OH-移向
②写出通入CH3OH的电极的电极反应式
③乙池中总反应的离子方程式
④当乙池中B(Ag)极的质量增加5.40g,此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
(2)利用反应Cu+2FeCl3=CuCl2+2FeCl2设计成如图2所示原电池,回答下列问题:
①写出电极反应式:正极
②图中X溶液是
③原电池工作时,盐桥中的
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】硝酸铵钙晶体是一种新型高效复合肥料,植物可以直接吸收,不会引起土壤板结。回答下列问题:
(1)硝酸铵钙晶体 的溶液显弱酸性,原因是
的溶液显弱酸性,原因是__________ 。(用离子方程式表示)。
(2)工业上生产硝酸铵钙的方法是以硝酸浸取磷矿石得到的粗硝酸钙(含硝酸钙、磷酸钙及硝酸)为原料制备,其生产流程为:
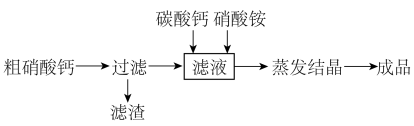
①加入适量的碳酸钙后发生反应的离子方程式为______ 。
②硝酸铵是一种易分解的物质,保存和利用时,需控制在较低温度。230~400℃时,它会分解成空气中含量最大的两种气体,其反应的化学方程式为__________ 。
(3)生产硝酸铵钙工厂的废水中常含有硝酸铵,净化方法有反硝化净化法和电解法。目前常用电解法净化,工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。

①阳极的电极反应式为_________ ,I室可回收的产品为_________ (填名称)。
②II室可回收到氨气,请解释其原因:_________ 。
(1)硝酸铵钙晶体
 的溶液显弱酸性,原因是
的溶液显弱酸性,原因是(2)工业上生产硝酸铵钙的方法是以硝酸浸取磷矿石得到的粗硝酸钙(含硝酸钙、磷酸钙及硝酸)为原料制备,其生产流程为:

①加入适量的碳酸钙后发生反应的离子方程式为
②硝酸铵是一种易分解的物质,保存和利用时,需控制在较低温度。230~400℃时,它会分解成空气中含量最大的两种气体,其反应的化学方程式为
(3)生产硝酸铵钙工厂的废水中常含有硝酸铵,净化方法有反硝化净化法和电解法。目前常用电解法净化,工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。

①阳极的电极反应式为
②II室可回收到氨气,请解释其原因:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】LFP是一种常见的锂离子电池正极材料,其中含有LiFePO4、炭黑、铝箔。利用废弃LFP正极材料回收金属、选择性提锂的工艺流程如下图所示。
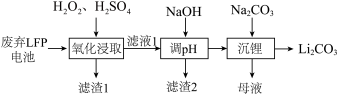
回答下列问题:
(1)Fe位于元素周期表的第___________ 周期___________ 族。
(2)若“滤渣1”中含有炭黑和FePO4,则“氧化浸取”中生成FePO4的离子方程式为___________ 。
(3)“滤渣2”的主要成分是___________ 。
(4) 和Na2SO4的溶解度曲线如下图所示,从母液中获Na2SO4的操作是加热浓缩至有大量晶体析出、
和Na2SO4的溶解度曲线如下图所示,从母液中获Na2SO4的操作是加热浓缩至有大量晶体析出、___________ 、干燥。
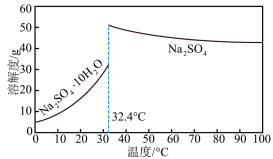
(5)利用FePO4和Li2CO3与葡萄糖在氮气氛围中加热能制备LiFePO4和CO,则发生的化学方程式为___________ 。
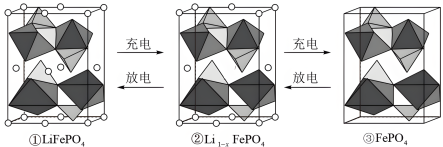
(6)LiFePO4的晶胞结构如图①所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。电池充电时,LiFeO4脱出部分 ,转化为
,转化为 (图②),最终变成FePO4(图③,晶胞参数为a pm、b pm、c pm),则FePO4的晶胞密度为
(图②),最终变成FePO4(图③,晶胞参数为a pm、b pm、c pm),则FePO4的晶胞密度为___________ g/cm3,LiFeO4转化 的电极反应式为
的电极反应式为___________ 。

回答下列问题:
(1)Fe位于元素周期表的第
(2)若“滤渣1”中含有炭黑和FePO4,则“氧化浸取”中生成FePO4的离子方程式为
(3)“滤渣2”的主要成分是
(4)
 和Na2SO4的溶解度曲线如下图所示,从母液中获Na2SO4的操作是加热浓缩至有大量晶体析出、
和Na2SO4的溶解度曲线如下图所示,从母液中获Na2SO4的操作是加热浓缩至有大量晶体析出、
(5)利用FePO4和Li2CO3与葡萄糖在氮气氛围中加热能制备LiFePO4和CO,则发生的化学方程式为
(6)LiFePO4的晶胞结构如图①所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。电池充电时,LiFeO4脱出部分
 ,转化为
,转化为 (图②),最终变成FePO4(图③,晶胞参数为a pm、b pm、c pm),则FePO4的晶胞密度为
(图②),最终变成FePO4(图③,晶胞参数为a pm、b pm、c pm),则FePO4的晶胞密度为 的电极反应式为
的电极反应式为
您最近半年使用:0次



