实验室制乙烯原理为:CH3CH2OH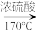 CH2=CH2↑+H2O,(可能的副反应为CH3CH2OH+6H2SO4(浓)
CH2=CH2↑+H2O,(可能的副反应为CH3CH2OH+6H2SO4(浓) 2CO2↑+6SO2↑+9H2O)装置如图所示。
2CO2↑+6SO2↑+9H2O)装置如图所示。
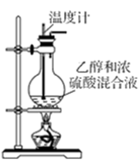
(1)盛装乙醇和浓硫酸混合溶液的玻璃仪器名称是_____ ,混合液中加入沸石的目的是_____ ,乙醇与浓硫酸应先在烧杯中混合好后再注入仪器,混合浓硫酸与乙醇的操作方法是_____ 。
(2)将生成的乙烯通入溴水之中,可以观察到的现象是溶液逐渐褪色、_____ ,发生的化学反应方程式是______ ,其反应类型是______ 。
(3)同学甲认为(2)中溶液褪色还可能是物质_____ (填写化学式)引起的,检验该物质的试剂为_____ (填序号)
A.BaCl2溶液 B.NaOH溶液 C.品红溶液
(4)已知乙烯在溴水中与溴反应的机理如下:
①溴分子在水分子作用下异裂为Br+和Br-;
②乙烯先与Br+作用生成中间体溴鎓离子( ),进而结合Br-完成反应。根据该反应机理,乙烯与溴水反应除上述产物外,还可能生成的其它产物的结构简式
),进而结合Br-完成反应。根据该反应机理,乙烯与溴水反应除上述产物外,还可能生成的其它产物的结构简式______ (一种即可)。
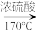 CH2=CH2↑+H2O,(可能的副反应为CH3CH2OH+6H2SO4(浓)
CH2=CH2↑+H2O,(可能的副反应为CH3CH2OH+6H2SO4(浓) 2CO2↑+6SO2↑+9H2O)装置如图所示。
2CO2↑+6SO2↑+9H2O)装置如图所示。
(1)盛装乙醇和浓硫酸混合溶液的玻璃仪器名称是
(2)将生成的乙烯通入溴水之中,可以观察到的现象是溶液逐渐褪色、
(3)同学甲认为(2)中溶液褪色还可能是物质
A.BaCl2溶液 B.NaOH溶液 C.品红溶液
(4)已知乙烯在溴水中与溴反应的机理如下:
①溴分子在水分子作用下异裂为Br+和Br-;
②乙烯先与Br+作用生成中间体溴鎓离子(
 ),进而结合Br-完成反应。根据该反应机理,乙烯与溴水反应除上述产物外,还可能生成的其它产物的结构简式
),进而结合Br-完成反应。根据该反应机理,乙烯与溴水反应除上述产物外,还可能生成的其它产物的结构简式
更新时间:2023-01-10 14:22:03
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
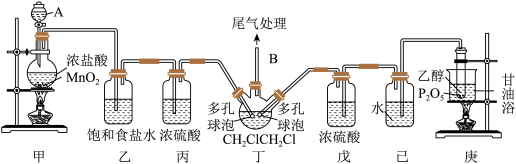
【推荐1】1,2-二氯乙烷(CH2ClCH2Cl)是重要的有机化工原料,不溶于水,易浴于有机溶剂,沸点83.6℃;在光照下逐渐分解;碱性条件下水解程度较大。实验室采用“乙烯液相直接氯化法”制备1,2-二氯乙烷,相关反应原理和实验装置图如下:
 该反应为放热反应
该反应为放热反应
回答下列问题:
(1)仪器A的名称是_________ 。
(2)①丁装置中多孔球泡的作用是_________ 。
②先装入1,2-二氯乙烷液体,其作用是_________ (选填序号)。
a.溶解Cl2和乙烯 b.作催化剂 c.促进气体反应物间的接触
③制得的1,2-二氯乙烷中溶解有Cl2、乙烯,逐出Cl2、乙烯采用的方法有_________ 。
(3)庚装置中采用甘油浴加热,该加热方式的优点是_________ ,写出该装置发生反应的化学方程式_________ 。
(4)产品纯度的测定:量取5.0mL逐出Cl2和乙烯后的产品,产品密度为1.2g·mL-1,加足量稀NaOH溶液,加热充分反应: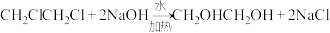 。所得溶液先用稀硝酸中和至酸性,然后加入1.000mol·L-1的AgNO3标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,求产品中1,2-二氯乙烷的纯度
。所得溶液先用稀硝酸中和至酸性,然后加入1.000mol·L-1的AgNO3标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,求产品中1,2-二氯乙烷的纯度_________ 。

 该反应为放热反应
该反应为放热反应回答下列问题:
(1)仪器A的名称是
(2)①丁装置中多孔球泡的作用是
②先装入1,2-二氯乙烷液体,其作用是
a.溶解Cl2和乙烯 b.作催化剂 c.促进气体反应物间的接触
③制得的1,2-二氯乙烷中溶解有Cl2、乙烯,逐出Cl2、乙烯采用的方法有
(3)庚装置中采用甘油浴加热,该加热方式的优点是
(4)产品纯度的测定:量取5.0mL逐出Cl2和乙烯后的产品,产品密度为1.2g·mL-1,加足量稀NaOH溶液,加热充分反应:
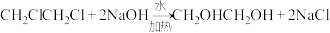 。所得溶液先用稀硝酸中和至酸性,然后加入1.000mol·L-1的AgNO3标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,求产品中1,2-二氯乙烷的纯度
。所得溶液先用稀硝酸中和至酸性,然后加入1.000mol·L-1的AgNO3标准溶液至不再产生沉淀,沉降后过滤、洗涤、低温干燥、称量,得到14.35g白色固体,求产品中1,2-二氯乙烷的纯度
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐2】已知:苯和卤代烃在催化剂作用下可生成烷基苯和卤化氢,例如:
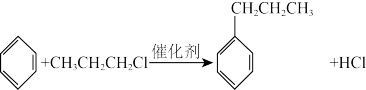
根据以下转化关系(生成物中所有无机物均已略去),其中F俗称PS,是一种高分子化合物,在建筑方面是一种良好的隔音、保温材料,回答下列问题:
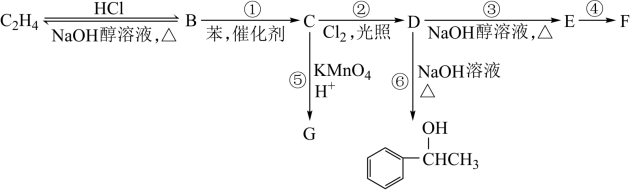
(1)G的结构简式为_______ 。
(2)在①~⑥反应中,属于取代反应的是_______ (填反应编号)。
(3)写出B生成乙烯的化学方程式:_______ 。
(4)分别写出④、⑥的化学方程式:_______ 、_______ 。

根据以下转化关系(生成物中所有无机物均已略去),其中F俗称PS,是一种高分子化合物,在建筑方面是一种良好的隔音、保温材料,回答下列问题:

(1)G的结构简式为
(2)在①~⑥反应中,属于取代反应的是
(3)写出B生成乙烯的化学方程式:
(4)分别写出④、⑥的化学方程式:
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】CO不仅是家用煤气的主要成分,也是重要的化工原料.下图是某些简单有机物在低温低压和催化剂存在下,合成具有优良性能的装饰性高分子涂料粘胶剂的基本过程.已知相间条件下A对氢气的相对密度为14,D具有水果香味且不易溶于水的油状液体.

(1)C的结构简式为________ ;
(2) 的化学方程式为
的化学方程式为________ ;
(3)下列说法正确的是________ .
A.D到E的反应类型属于加聚反应
B.A即使溴水溶液褪色,又能使酸性高锰酸钾褪色,且褪色原理相同
C.煤的气化可以得到CO和H2等气体,再经过催化合成可以得到液态烃、甲醇等液体燃料,被称为煤的液化
D.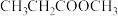 中含有少量C,可用饱和碳酸钠溶液除去
中含有少量C,可用饱和碳酸钠溶液除去

(1)C的结构简式为
(2)
 的化学方程式为
的化学方程式为(3)下列说法正确的是
A.D到E的反应类型属于加聚反应
B.A即使溴水溶液褪色,又能使酸性高锰酸钾褪色,且褪色原理相同
C.煤的气化可以得到CO和H2等气体,再经过催化合成可以得到液态烃、甲醇等液体燃料,被称为煤的液化
D.
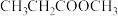 中含有少量C,可用饱和碳酸钠溶液除去
中含有少量C,可用饱和碳酸钠溶液除去
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室制备1,2—二溴乙烷的反应原理如下:
CH3CH2OH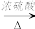 CH2=CH2+H2O
CH2=CH2+H2O
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。
用少量溴和足量的乙醇制备1,2—二溴乙烷的装置如图所示:

有关数据列表如下:
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是________ ;(填正确选项前的字母)
a. 引发反应 b. 加快反应速度
c. 防止乙醇挥发 d. 减少副产物乙醚生成
(2)在装置C中应加入________ ,其目的是吸收反应中可能生成的酸性气体;(填正确选项前的字母)
a 水 b 浓硫酸 c 氢氧化钠溶液 d 饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的方法是D装置中____________________________ ;
(4)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,溶液分层,产物应在______ 层(填“上”“下”);分离该有机物的方法叫_______________ 。
(5)若产物中有少量乙醚生成,最好用__________ 除去;(填正确选项前的字母)
a蒸发 b 蒸馏 c 重结晶
(6)反应过程中应用冷水冷却装置D,其主要目的是____________________ 。
CH3CH2OH
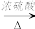 CH2=CH2+H2O
CH2=CH2+H2OCH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。
用少量溴和足量的乙醇制备1,2—二溴乙烷的装置如图所示:

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
密度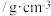 | 0.79 | 2.2 | 0.71 |
沸点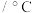 | 78.5 | 132 | 34.6 |
熔点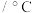 | -130 | 9 | -116 |
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是
a. 引发反应 b. 加快反应速度
c. 防止乙醇挥发 d. 减少副产物乙醚生成
(2)在装置C中应加入
a 水 b 浓硫酸 c 氢氧化钠溶液 d 饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的方法是D装置中
(4)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,溶液分层,产物应在
(5)若产物中有少量乙醚生成,最好用
a蒸发 b 蒸馏 c 重结晶
(6)反应过程中应用冷水冷却装置D,其主要目的是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】有机化合物A的分子式为 ,它与NaOH溶液共热后蒸馏,得到含B的蒸馏物。将B与浓硫酸混合加热,控制温度可以得到一种能使溴的四氯化碳溶液褪色,并可作果实催熟剂的无色气体C,B在一定温度和催化剂存在的条件下,能被空气氧化为D,D与新制的
,它与NaOH溶液共热后蒸馏,得到含B的蒸馏物。将B与浓硫酸混合加热,控制温度可以得到一种能使溴的四氯化碳溶液褪色,并可作果实催熟剂的无色气体C,B在一定温度和催化剂存在的条件下,能被空气氧化为D,D与新制的 在一定条件下反应,有砖红色沉淀和E生成。请写出下列变化的化学方程式。
在一定条件下反应,有砖红色沉淀和E生成。请写出下列变化的化学方程式。
(1)A→B________ 。
(2)B→C________ 。
(3)B→D________ 。
(4)D→E________ 。
 ,它与NaOH溶液共热后蒸馏,得到含B的蒸馏物。将B与浓硫酸混合加热,控制温度可以得到一种能使溴的四氯化碳溶液褪色,并可作果实催熟剂的无色气体C,B在一定温度和催化剂存在的条件下,能被空气氧化为D,D与新制的
,它与NaOH溶液共热后蒸馏,得到含B的蒸馏物。将B与浓硫酸混合加热,控制温度可以得到一种能使溴的四氯化碳溶液褪色,并可作果实催熟剂的无色气体C,B在一定温度和催化剂存在的条件下,能被空气氧化为D,D与新制的 在一定条件下反应,有砖红色沉淀和E生成。请写出下列变化的化学方程式。
在一定条件下反应,有砖红色沉淀和E生成。请写出下列变化的化学方程式。(1)A→B
(2)B→C
(3)B→D
(4)D→E
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室制取少量的乙烯时,常利用乙醇和浓硫酸快速加热到170℃来制取。此实验常因温度过高而发生副反应。有部分乙醇跟浓H2SO4反应生成SO2、C02、水蒸气和炭黑。
I.用方程式表示乙烯制备的反应原理____ ;乙烯制备时,在140℃常伴随有副反应发生,化学方程式为_____ 。
Ⅱ.有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。试完成下列问题:
(1)图中①②③④装置可盛放的试剂是(试剂可重复使用,也可不使用):(填写ABCD)
①_____ ;②____ ;③_____ ;④______ 。
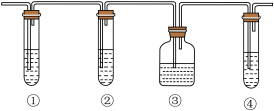
A.品红溶液 B.NaOH溶液 C.浓H2SO4 D.酸性KMnO4溶液
(2)能说明二氧化硫气体存在的现象是______ 。
(3)使用装置②的目的是___________ 。
(4)使用装置③的目的是______________ 。
(5)确证含有乙烯的现象是_______________
I.用方程式表示乙烯制备的反应原理
Ⅱ.有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。试完成下列问题:
(1)图中①②③④装置可盛放的试剂是(试剂可重复使用,也可不使用):(填写ABCD)
①

A.品红溶液 B.NaOH溶液 C.浓H2SO4 D.酸性KMnO4溶液
(2)能说明二氧化硫气体存在的现象是
(3)使用装置②的目的是
(4)使用装置③的目的是
(5)确证含有乙烯的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】亚硝酰氯(NOCl)是一种红褐色液体或黄色气体,其熔点-64.5℃,沸点-5.5℃,遇水易水解生成一种氢化物和两种氮的常见氧化物,其中一种呈红棕色。NOCl可由NO与纯净的Cl2在常温常压下合成,相关实验装置如图所示。

(1)装置F中的固体试剂为___________ ,E装置的作用是___________ 。
(2)实验开始时,先打开K1、K2,关闭K3,再打开分液漏斗活塞滴入适量稀硝酸,当观察到B中红棕色完全消失时关闭K1、K2,之后可能观察到B中现象为___________ 。然后再向装置C三颈瓶中通入干燥Cl2,当瓶中充满黄绿色气体时,再打开K1、K3,制备NOCl。
(3)制得的NOCl中可能含有少量N2O4杂质,为测定产品纯度进行如下实验:
Ⅰ.称取一定量的AgNO3晶体,溶于水,用250mL 容量瓶定容至250mL 溶液,再用某基准溶液滴定,测得其准确浓度为0.4000mol•L-1
Ⅱ.将所得亚硝酰氯(NOC1)产品13.10g溶于水,配制成250mL溶液;取出25.00mL,以___________ 溶液为指示剂,(已知:Ksp(AgCl)=1.8×10−10; Ksp(AgSCN)=7.0×10−18为白色固体;Ksp(Ag2CrO4) =1.0×10−12为砖红色固体)用上述0.4000mol•L-1AgNO3溶液滴定至终点,消耗AgNO3溶液的体积为22.50mL。
①NOCl可用AgNO3溶液滴定是因为它与水发生了反应,离子方程式为_________ 。
②亚硝酰氯(NOCl)的质量分数为_________ 。
③若配制AgNO3溶液时仰视容量瓶刻度线,则最终滴定测定结果_______ (填“偏高”、“偏低”或“无影响”)。

(1)装置F中的固体试剂为
(2)实验开始时,先打开K1、K2,关闭K3,再打开分液漏斗活塞滴入适量稀硝酸,当观察到B中红棕色完全消失时关闭K1、K2,之后可能观察到B中现象为
(3)制得的NOCl中可能含有少量N2O4杂质,为测定产品纯度进行如下实验:
Ⅰ.称取一定量的AgNO3晶体,溶于水,用250mL 容量瓶定容至250mL 溶液,再用某基准溶液滴定,测得其准确浓度为0.4000mol•L-1
Ⅱ.将所得亚硝酰氯(NOC1)产品13.10g溶于水,配制成250mL溶液;取出25.00mL,以
①NOCl可用AgNO3溶液滴定是因为它与水发生了反应,离子方程式为
②亚硝酰氯(NOCl)的质量分数为
③若配制AgNO3溶液时仰视容量瓶刻度线,则最终滴定测定结果
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室可由 、
、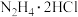 、
、 为原料制备
为原料制备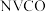 ,若反应后废液中的
,若反应后废液中的 排入水中,则过量的氮元素会使水体富营养化。此外考虑到其他污染源,污水一般还会含有
排入水中,则过量的氮元素会使水体富营养化。此外考虑到其他污染源,污水一般还会含有 、
、 、
、 等。
等。
(1)已知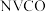 化学式可表示为
化学式可表示为 ,由常温下逐渐升温的过程中会发生分解。已知起始状态到A点是失去了部分结晶水,B点对应的物质是钒的氧化物,如下图所示。
,由常温下逐渐升温的过程中会发生分解。已知起始状态到A点是失去了部分结晶水,B点对应的物质是钒的氧化物,如下图所示。

①写出起始状态到A点发生分解反应的化学方程式:________________ 。
②B点对应物质的化学式是______________ 。
(2)废水中 和
和 的处理。通过形成铁炭(铁和活性炭)原电池可对废水中的有机物及含氮物质等进行处理,将酸性废水中以
的处理。通过形成铁炭(铁和活性炭)原电池可对废水中的有机物及含氮物质等进行处理,将酸性废水中以 和
和 形式存在的氮元素转化为
形式存在的氮元素转化为 除去。
除去。
①写出 在正极发生的电极反应式
在正极发生的电极反应式______________ 。
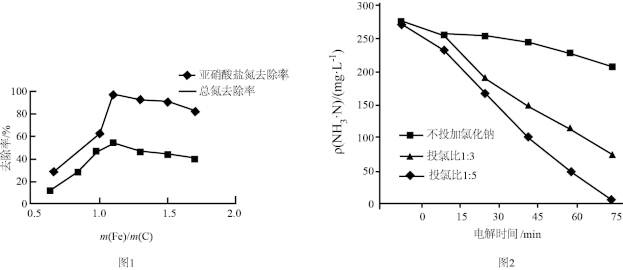
②不同 的脱氮效果如图1所示,则合适的
的脱氮效果如图1所示,则合适的 =
=________ 。
③实验测得当 时,对废水中的氮也有一定的脱除率,其原因为
时,对废水中的氮也有一定的脱除率,其原因为________ 。
(3)废水中 的处理。用电解法可对废水进行脱氮处理。
的处理。用电解法可对废水进行脱氮处理。
①电解时含氯离子转化为次氯酸, 与
与 反应生成
反应生成 ,当生成
,当生成 时,转移的电子数为
时,转移的电子数为________ mol。
②氯离子含量对废水脱氮效果的影响如图2所示,投氯比是指氨氮与氯离子物质的量的比,三种情况下投料为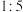 时脱氮效果
时脱氮效果________ (填“最好”“最差”或“居中”),原因可能是________ 。
 、
、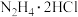 、
、 为原料制备
为原料制备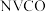 ,若反应后废液中的
,若反应后废液中的 排入水中,则过量的氮元素会使水体富营养化。此外考虑到其他污染源,污水一般还会含有
排入水中,则过量的氮元素会使水体富营养化。此外考虑到其他污染源,污水一般还会含有 、
、 、
、 等。
等。(1)已知
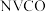 化学式可表示为
化学式可表示为 ,由常温下逐渐升温的过程中会发生分解。已知起始状态到A点是失去了部分结晶水,B点对应的物质是钒的氧化物,如下图所示。
,由常温下逐渐升温的过程中会发生分解。已知起始状态到A点是失去了部分结晶水,B点对应的物质是钒的氧化物,如下图所示。
①写出起始状态到A点发生分解反应的化学方程式:
②B点对应物质的化学式是
(2)废水中
 和
和 的处理。通过形成铁炭(铁和活性炭)原电池可对废水中的有机物及含氮物质等进行处理,将酸性废水中以
的处理。通过形成铁炭(铁和活性炭)原电池可对废水中的有机物及含氮物质等进行处理,将酸性废水中以 和
和 形式存在的氮元素转化为
形式存在的氮元素转化为 除去。
除去。①写出
 在正极发生的电极反应式
在正极发生的电极反应式②不同
 的脱氮效果如图1所示,则合适的
的脱氮效果如图1所示,则合适的 =
=③实验测得当
 时,对废水中的氮也有一定的脱除率,其原因为
时,对废水中的氮也有一定的脱除率,其原因为
(3)废水中
 的处理。用电解法可对废水进行脱氮处理。
的处理。用电解法可对废水进行脱氮处理。①电解时含氯离子转化为次氯酸,
 与
与 反应生成
反应生成 ,当生成
,当生成 时,转移的电子数为
时,转移的电子数为②氯离子含量对废水脱氮效果的影响如图2所示,投氯比是指氨氮与氯离子物质的量的比,三种情况下投料为
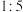 时脱氮效果
时脱氮效果
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】从海水中提取并制备碳酸锂,可以提高海水的综合利用价值,满足工业上对碳酸锂的需求。制备碳酸锂的一种工艺流程如下:
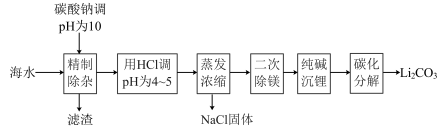
已知:①海水中某些离子浓度如下:
②碳酸锂的溶解度:
 几种难溶电解质的溶度积(25℃):
几种难溶电解质的溶度积(25℃):
请回答下列问题:
 精制除杂阶段的滤渣为MgCO3、
精制除杂阶段的滤渣为MgCO3、______  写化学式
写化学式
 用HCl调pH为4~5的目的是
用HCl调pH为4~5的目的是_________ 。
 二次除镁过程中,若使Mg2+浓度为6×10-4mol/L,应控制pH为
二次除镁过程中,若使Mg2+浓度为6×10-4mol/L,应控制pH为______ 。
 沉锂阶段,实际测得不同纯碱加入量条件下的碳酸锂沉淀结果如下表:
沉锂阶段,实际测得不同纯碱加入量条件下的碳酸锂沉淀结果如下表:
综合以上信息及考虑实际生产时的原料成本,应按照______  填序号
填序号 中CO32-与Li+物质的量之比加入纯碱制备碳酸锂。
中CO32-与Li+物质的量之比加入纯碱制备碳酸锂。
 沉锂温度需控制在
沉锂温度需控制在 ,主要原因是
,主要原因是______ 。
 碳化分解具体过程为:①向碳酸锂与水的浆料中通入CO2气体,充分反应后,过滤;②加热滤液使其分解。写出②反应中的化学方程式:
碳化分解具体过程为:①向碳酸锂与水的浆料中通入CO2气体,充分反应后,过滤;②加热滤液使其分解。写出②反应中的化学方程式:__________ 。写出在碳化分解中可循环利用物质的电子式:_________ 。

已知:①海水中某些离子浓度如下:
| 离子 | Li+ | Mg2+ | Ca2+ | Mn2+ | Cl- |
| 浓度(mol/L) | 0.113 | 0.049 | 0.001 | 0.010 | 0.501 |
| 温度(℃) | 0 | 10 | 30 | 50 | 70 | 90 |
| 溶解度(g/L) | 1.54 | 1.43 | 1.25 | 1.08 | 0.91 | 0.83 |
 几种难溶电解质的溶度积(25℃):
几种难溶电解质的溶度积(25℃):| 物质 | Li2CO3 | MgCO3 | MnCO3 | CaCO3 | Mg(OH)2 |
| Ksp | 2.5×10-2 | 6.8×10-6 | 2.3×10-11 | 2.8×10-9 | 6×10-10 |
 精制除杂阶段的滤渣为MgCO3、
精制除杂阶段的滤渣为MgCO3、 写化学式
写化学式
 用HCl调pH为4~5的目的是
用HCl调pH为4~5的目的是 二次除镁过程中,若使Mg2+浓度为6×10-4mol/L,应控制pH为
二次除镁过程中,若使Mg2+浓度为6×10-4mol/L,应控制pH为 沉锂阶段,实际测得不同纯碱加入量条件下的碳酸锂沉淀结果如下表:
沉锂阶段,实际测得不同纯碱加入量条件下的碳酸锂沉淀结果如下表:| 序号 | 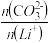 | 沉淀质量(g) | Li2CO3含量(%) | 锂回收率(%) |
| 0.9:2.0 | 10.09 | 92.36 | 77.67 | |
| 1.0:2.0 | 10.97 | 90.19 | 82.46 | |
| 1.1:2.0 | 11.45 | 89.37 | 85.27 | |
| 1.2:2.0 | 12.14 | 84.82 | 85.85 |
 填序号
填序号 中CO32-与Li+物质的量之比加入纯碱制备碳酸锂。
中CO32-与Li+物质的量之比加入纯碱制备碳酸锂。 沉锂温度需控制在
沉锂温度需控制在 ,主要原因是
,主要原因是 碳化分解具体过程为:①向碳酸锂与水的浆料中通入CO2气体,充分反应后,过滤;②加热滤液使其分解。写出②反应中的化学方程式:
碳化分解具体过程为:①向碳酸锂与水的浆料中通入CO2气体,充分反应后,过滤;②加热滤液使其分解。写出②反应中的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】亚硝酸钙是一种阻锈剂,可用于染料工业,某兴趣小组拟制备Ca(NO2)2并对其性质进行探究。
【背景素材】
I.Ca(NO2)2能被酸性KMnO4溶液氧化成NO3,MnO4-被还原为Mn2+。
II.在酸性条件下,Ca(NO2)2能将I-氧化为I2,S2O32能将I2还原为I。
III.HNO2是具有氧化性的一元弱酸且AgNO2是一种难溶于水的白色化合物。
(1)兴趣小组同学拟利用铜片和某浓度的硝酸制备物质的量之比为1:1的NO和NO2的混合气体,请写出此反应的离子方程式___________________________ ;
(2)兴趣小组同学拟利用(1)产生的氮氧化物制备Ca(NO2)2,装置如图。
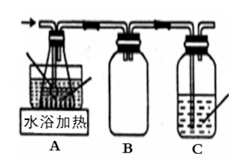
①装置A中导管末端接一玻璃球的作用是___________________________ ;
②装置B的作用是________________ ;
③若现有m mol NO2和n mol NO组成的混合气体进入装置C进行尾气处理,欲用a mol/L NaOH溶液吸收,至少需要a mol/L NaOH溶液的体积为____________ 升;
(3)兴趣小组同学拟测定Ca(NO2)2的纯度(杂质不参加反应),可供选择的试剂:
A.KI(酸性)溶液 B.淀粉溶液
C.Na2S2O3溶液 D.酸性KMnO4溶液
①利用Ca(NO2)2的还原性来测定其纯度,可选择的试剂是____________ (填字母);
②利用Ca(NO2)2的氧化性来测定其纯度,可选择的试剂是____________ (填字母);
(4)兴趣小组同学认为制备的Ca(NO2)2会混有Ca(NO3)2,能用来鉴别二者的试剂(_____ )
A.测溶液的pH B.加硫酸铁(酸性)溶液
C.加硝酸银溶液 D.加淀粉碘化钾(酸性)溶液
【背景素材】
I.Ca(NO2)2能被酸性KMnO4溶液氧化成NO3,MnO4-被还原为Mn2+。
II.在酸性条件下,Ca(NO2)2能将I-氧化为I2,S2O32能将I2还原为I。
III.HNO2是具有氧化性的一元弱酸且AgNO2是一种难溶于水的白色化合物。
(1)兴趣小组同学拟利用铜片和某浓度的硝酸制备物质的量之比为1:1的NO和NO2的混合气体,请写出此反应的离子方程式
(2)兴趣小组同学拟利用(1)产生的氮氧化物制备Ca(NO2)2,装置如图。

①装置A中导管末端接一玻璃球的作用是
②装置B的作用是
③若现有m mol NO2和n mol NO组成的混合气体进入装置C进行尾气处理,欲用a mol/L NaOH溶液吸收,至少需要a mol/L NaOH溶液的体积为
(3)兴趣小组同学拟测定Ca(NO2)2的纯度(杂质不参加反应),可供选择的试剂:
A.KI(酸性)溶液 B.淀粉溶液
C.Na2S2O3溶液 D.酸性KMnO4溶液
①利用Ca(NO2)2的还原性来测定其纯度,可选择的试剂是
②利用Ca(NO2)2的氧化性来测定其纯度,可选择的试剂是
(4)兴趣小组同学认为制备的Ca(NO2)2会混有Ca(NO3)2,能用来鉴别二者的试剂(
A.测溶液的pH B.加硫酸铁(酸性)溶液
C.加硝酸银溶液 D.加淀粉碘化钾(酸性)溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】如图是某同学研究铜与浓硫酸的反应装置:
完成下列填空:
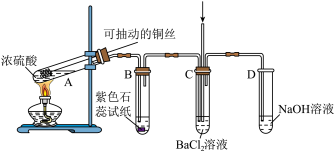
(1)写出A中发生反应的化学方程式______ ,采用可抽动铜丝进行实验的优点是______ 。
(2)反应一段时间后,可观察到B试管中的现象为______ 。
(3)从C试管的直立导管中向BaCl2溶液中通入另一种气体,产生白色沉淀,则气体可以是______ 、______ .(要求填一种化合物和一种单质的化学式)。
(4)反应完毕,将A中的混合物倒入水中,得到呈酸性的蓝色溶液与少量黑色不溶物,分离出该不溶物的操作是______ ,该黑色不溶物不可能是CuO,理由是______ 。
(5)对铜与浓硫酸反应产生的黑色不溶物进行探究,实验装置及现象如下:
①根据实验现象可判断黑色不溶物中一定含有______ 元素。
②若该黑色不溶物由两种元素组成且在反应前后质量保持不变,推测其化学式为______ 。
完成下列填空:

(1)写出A中发生反应的化学方程式
(2)反应一段时间后,可观察到B试管中的现象为
(3)从C试管的直立导管中向BaCl2溶液中通入另一种气体,产生白色沉淀,则气体可以是
(4)反应完毕,将A中的混合物倒入水中,得到呈酸性的蓝色溶液与少量黑色不溶物,分离出该不溶物的操作是
(5)对铜与浓硫酸反应产生的黑色不溶物进行探究,实验装置及现象如下:
| 实验装置 | 实验现象 |
 | 品红褪色 |
①根据实验现象可判断黑色不溶物中一定含有
②若该黑色不溶物由两种元素组成且在反应前后质量保持不变,推测其化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】海洋资源的利用具有非常广阔的前景。地球上99%的溴元素以溴离子的形式存在于海水中,因此人们也把溴称为“海洋元素”。空气吹出法工艺是目前“海水提溴”的最主要方法之一,海水提溴的工艺流程如图:______ 这一物理性质将低浓度Br2分离出来。
(2)“吸收塔”中发生的离子反应为______ ;请你设计实验说明“吸收塔”中含硫微粒的主要存在形式:______ 。
(3)已知常压下Br2的沸点是59℃。蒸馏塔中温度控制在______的范围内较合适。
(4)探究“氧化”的适宜条件,测得不同条件下溶液中被氧化的Br-的百分含量如图: 表示加入氯元素与海水中溴元素物质的量之比。
表示加入氯元素与海水中溴元素物质的量之比。
“氧化”的适宜条件为______ 。
(5)(CNO)2、(CN)2、(SCN)2被称为拟卤素单质,具有卤素相似的性质。为了探究Br2、(CN)2、(CNO)2、(SCN)2的氧化性强弱,进行实验,实验操作及现象如下:
已知:拟卤素单质及钾盐水溶液均为无色。
①如果氧化产物为(SCN)2,写出操作乙中反应的离子方程式:______ 。
②某同学得出结论,氧化性:(CNO)2>Br2>(CN)2>(SCN)2。该结论是否合理?并说明理由______

(2)“吸收塔”中发生的离子反应为
(3)已知常压下Br2的沸点是59℃。蒸馏塔中温度控制在______的范围内较合适。
| A.20℃~30℃ | B.45℃~55℃ | C.75℃~85℃ | D.100℃~110℃ |
(4)探究“氧化”的适宜条件,测得不同条件下溶液中被氧化的Br-的百分含量如图:
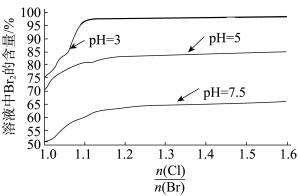
 表示加入氯元素与海水中溴元素物质的量之比。
表示加入氯元素与海水中溴元素物质的量之比。“氧化”的适宜条件为
(5)(CNO)2、(CN)2、(SCN)2被称为拟卤素单质,具有卤素相似的性质。为了探究Br2、(CN)2、(CNO)2、(SCN)2的氧化性强弱,进行实验,实验操作及现象如下:
实验操作 | 现象 | |
甲 | 向KCNO溶液中滴加几滴溴水,振荡 | 溶液不褪色 |
乙 | 向KSCN溶液中滴加溴水,振荡 | 溶液褪色 |
丙 | 向KCN溶液中滴加溴水,振荡 | 溶液褪色 |
①如果氧化产物为(SCN)2,写出操作乙中反应的离子方程式:
②某同学得出结论,氧化性:(CNO)2>Br2>(CN)2>(SCN)2。该结论是否合理?并说明理由
您最近一年使用:0次



