回答下列问题:
(1)已知某废水试样中可能含有表中的离子:
将废水试样分成甲、乙、丙、丁四份,进行如图所示探究。
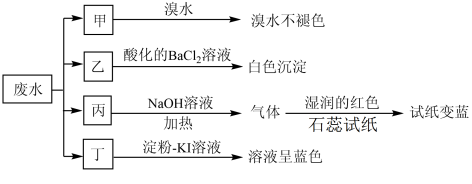
回答下列问题:
离子X是_______ (填化学式,下同),离子Y是_______ 。表中不能确定是否存在的阴离子是_______ ,能证明该阴离子是否存在的简单实验操作为_______ 。写出废水试样中滴加淀粉-KI溶液所发生反应的离子方程式:_______ 。
(2)已知某溶液中含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的氯气,则溶液中Cl-、Br-、I-与通入氯气的体积(标准状况下)关系如下表所示,回答下列问题:
原溶液中 、
、 、
、 的物质的量浓度之比为
的物质的量浓度之比为_______ 。
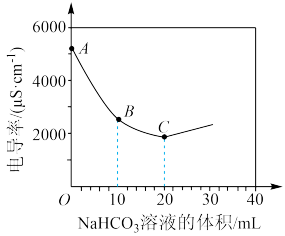
(3)向100mL 溶液中滴加
溶液中滴加 溶液,测得溶液电导率的变化如图。下列说法错误的是_______。
溶液,测得溶液电导率的变化如图。下列说法错误的是_______。
(1)已知某废水试样中可能含有表中的离子:
| 阳离子 |  、 、 、 、 、 、 |
| 阴离子 |  、 、 、 、 、 、 |

回答下列问题:
离子X是
(2)已知某溶液中含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的氯气,则溶液中Cl-、Br-、I-与通入氯气的体积(标准状况下)关系如下表所示,回答下列问题:
 的体积(标准状况下) 的体积(标准状况下) | 2.8L | 5.6L | 11.2L |
 | 1.25mol | 1.5mol | 2mol |
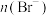 | 1.5mol | 1.4mol | 0.9mol |
 | a mol | 0 | 0 |
 、
、 、
、 的物质的量浓度之比为
的物质的量浓度之比为(3)向100mL
 溶液中滴加
溶液中滴加 溶液,测得溶液电导率的变化如图。下列说法错误的是_______。
溶液,测得溶液电导率的变化如图。下列说法错误的是_______。
A. 和 和 都是强电解质 都是强电解质 |
B.A→B电导率下降的主要原因是发生了反应 |
C.B→C溶液中的 减小 减小 |
| D.C点时,往溶液滴入少量酚酞,溶液呈红色 |
更新时间:2023-01-10 20:34:27
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如图所示。
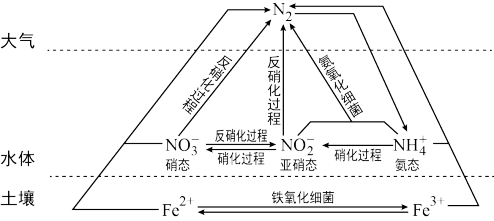
(1)如图所示氮循环中,属于氮的固定的有_____ (填字母序号)。
a.N2转化为氨态氮
b.硝化过程
c.反硝化过程
(2)氮肥是水体中 的主要来源之一,检验氮肥中
的主要来源之一,检验氮肥中 的实验方案是
的实验方案是_____ 。
(3)硝化过程中,含氮物质发生_____ (填“氧化”或“还原”)反应。
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为_____ mol。
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理_____ 。

(1)如图所示氮循环中,属于氮的固定的有
a.N2转化为氨态氮
b.硝化过程
c.反硝化过程
(2)氮肥是水体中
 的主要来源之一,检验氮肥中
的主要来源之一,检验氮肥中 的实验方案是
的实验方案是(3)硝化过程中,含氮物质发生
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理
您最近一年使用:0次
【推荐2】在抗击新冠肺炎疫情的战役中,民众的防疫意识不能松懈。为有效防止新冠病毒的传播,除了戴口罩,还需加强对隔离场所的消毒。常用的消毒剂有双氧水、医用酒精以及含氯消毒剂。其中含氯消毒剂的家族最庞大、应用最广泛。实验室制备 有三种常用方法:
有三种常用方法:
a.

b._______ +_______HCl(浓)→ _______KCl+_______
+_______HCl(浓)→ _______KCl+_______ +_______
+_______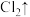 +_______
+_______
c.
(1)根据上述反应方程式,比较 、
、 、
、 的氧化性
的氧化性_______ 。
(2)对于反应a,氧化剂与还原剂的个数比为_______ ,该反应对应离子方程式为_______ 。
(3)用单线桥表示
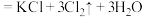 反应电子转移情况
反应电子转移情况______ 。
(4)配平反应b______
(5)对于反应b,当得到7.1g 时,消耗HCl的质量是
时,消耗HCl的质量是_______ ,若要得到等质量的 ,从节约HCl的角度考虑,最适宜选择
,从节约HCl的角度考虑,最适宜选择_______ 。(填“a”、“b”、“c”)反应。
 有三种常用方法:
有三种常用方法:a.


b._______
 +_______HCl(浓)→ _______KCl+_______
+_______HCl(浓)→ _______KCl+_______ +_______
+_______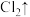 +_______
+_______
c.

(1)根据上述反应方程式,比较
 、
、 、
、 的氧化性
的氧化性(2)对于反应a,氧化剂与还原剂的个数比为
(3)用单线桥表示

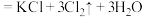 反应电子转移情况
反应电子转移情况(4)配平反应b
(5)对于反应b,当得到7.1g
 时,消耗HCl的质量是
时,消耗HCl的质量是 ,从节约HCl的角度考虑,最适宜选择
,从节约HCl的角度考虑,最适宜选择
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】高锰酸钾是一种典型的强氧化剂。完成下列填空:
Ⅰ.在用酸性KMnO4溶液处理Cu2S和CuS的混合物时,发生的反应如下:
①8MnO +5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
②6MnO +5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
(1)下列关于反应①的说法中错误的是_______ (填序号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8∶5
c.还原性的强弱关系是:Mn2+>Cu2S
d.生成2.24 L(标况下)SO2,转移电子的物质的量是0.8 mol
(2)用单线桥标出反应②中电子转移的方向和数目:_______ 。
6MnO +5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
Ⅱ.一个氧化还原反应可以看作是由得电子和失电子的两个半反应组成。在稀硫酸中,KMnO4和H2O2也能发生氧化还原反应
氧化反应:H2O2-2e-=2H++O2↑
还原反应:MnO +5e-+8H+=Mn2++4H2O
+5e-+8H+=Mn2++4H2O
(3)反应中若有0.5 mol H2O2参加此反应,转移电子的个数为_______ 。由上述反应得出的物质氧化性强弱的结论是_______ >_______ (填写化学式)。
(4)已知:2KMnO4+7H2O2+3H2SO4=K2SO4+2MnSO4+6O2↑+10H2O,则被1 mol KMnO4氧化的H2O2是_______ mol。
Ⅰ.在用酸性KMnO4溶液处理Cu2S和CuS的混合物时,发生的反应如下:
①8MnO
 +5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O②6MnO
 +5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O(1)下列关于反应①的说法中错误的是
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8∶5
c.还原性的强弱关系是:Mn2+>Cu2S
d.生成2.24 L(标况下)SO2,转移电子的物质的量是0.8 mol
(2)用单线桥标出反应②中电子转移的方向和数目:
6MnO
 +5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2OⅡ.一个氧化还原反应可以看作是由得电子和失电子的两个半反应组成。在稀硫酸中,KMnO4和H2O2也能发生氧化还原反应
氧化反应:H2O2-2e-=2H++O2↑
还原反应:MnO
 +5e-+8H+=Mn2++4H2O
+5e-+8H+=Mn2++4H2O(3)反应中若有0.5 mol H2O2参加此反应,转移电子的个数为
(4)已知:2KMnO4+7H2O2+3H2SO4=K2SO4+2MnSO4+6O2↑+10H2O,则被1 mol KMnO4氧化的H2O2是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】细菌可以促使铁、氮两种元素进行化还原反应,并耦合两种元素的循环。

(1)氮循环中,属于氮的固定的有_______ (填字母序号,下同),属于氧化反应的有_______ 。
a. 转化为氨态氮 b.硝化过程 c.反硝化过程
转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中铵根的主要来源之一,铵根的电子式为_______ ,检验某固态氮肥中铵根的实验操作与相应的现象及结论为_______ 。
(3)铵态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移电子的物质的量为_______ 。
(4)土壤中的铁循环可用于水体脱氮(指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中铵态氮的原理_______ 。
(5)实验室中也可以实现不同价态氮元素之间的转变,请写出符合以下要求的化学方程式:
①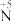 转化为
转化为 :
:_______
②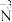 转化为
转化为 :
:_______

(1)氮循环中,属于氮的固定的有
a.
 转化为氨态氮 b.硝化过程 c.反硝化过程
转化为氨态氮 b.硝化过程 c.反硝化过程(2)氮肥是水体中铵根的主要来源之一,铵根的电子式为
(3)铵态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移电子的物质的量为
(4)土壤中的铁循环可用于水体脱氮(指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中铵态氮的原理
(5)实验室中也可以实现不同价态氮元素之间的转变,请写出符合以下要求的化学方程式:
①
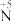 转化为
转化为 :
:②
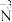 转化为
转化为 :
:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价物质类别关系图如下。
(1)写出实验室制备物质A的化学方程式:_______ 。在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是_______ 。
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:_______ 。
(3)实验室中,检验溶液中含有NH 的操作方法是
的操作方法是_______ 。
(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:_______ ,当反应消耗3.36 L(标准状况)物质B时,转移电子的物质的量为_______ mol。

(1)写出实验室制备物质A的化学方程式:
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:
(3)实验室中,检验溶液中含有NH
 的操作方法是
的操作方法是(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有一混合溶液,只可能含有以下离子中的若干种:K+、 、Cl-、Ba2+、
、Cl-、Ba2+、 、
、 取三份各100mL该混合溶液进行如下实验。
取三份各100mL该混合溶液进行如下实验。
实验①:向第一份混合溶液中加入AgNO3溶液,有沉淀产生;
实验②:向第二份混合溶液中加入足量NaOH溶液,加热,收集到0.08mol气体;
实验③:向第三份混合溶液中加入足量BaCl2溶液后,得到干燥的沉淀12.54g,经足量稀盐酸洗涤、干燥后,沉淀质量为4.66g。
(已知: +OH-
+OH- H2O+NH3↑)
H2O+NH3↑)
根据上述实验,回答以下问题。
(1)由实验①推断该混合溶液__________ (填“一定”或“不一定”)含有Cl-。
(2)由实验②推断该混合溶液中应含有__________ (填离子符号),其物质的量浓度为______________ 。
(3)由实验③可知12.54g沉淀的成分为_______________ (填化学式)。
(4)综合上述实验,你认为以下结论正确的是______________ (填标号)。
A.该混合溶液中一定含有K+、 、
、 、
、 ,可能含Cl-,且n(K+)≥0.04mol
,可能含Cl-,且n(K+)≥0.04mol
B.该混合溶液中一定含有 、
、 、
、 ,可能含Ba2+、K+、Cl-
,可能含Ba2+、K+、Cl-
C.该混合溶液中一定含有 、
、 、
、 ,可能含K+、Cl-
,可能含K+、Cl-
D.该混合溶液中一定含有 、
、 ,可能含K+、Cl-
,可能含K+、Cl-
 、Cl-、Ba2+、
、Cl-、Ba2+、 、
、 取三份各100mL该混合溶液进行如下实验。
取三份各100mL该混合溶液进行如下实验。实验①:向第一份混合溶液中加入AgNO3溶液,有沉淀产生;
实验②:向第二份混合溶液中加入足量NaOH溶液,加热,收集到0.08mol气体;
实验③:向第三份混合溶液中加入足量BaCl2溶液后,得到干燥的沉淀12.54g,经足量稀盐酸洗涤、干燥后,沉淀质量为4.66g。
(已知:
 +OH-
+OH- H2O+NH3↑)
H2O+NH3↑)根据上述实验,回答以下问题。
(1)由实验①推断该混合溶液
(2)由实验②推断该混合溶液中应含有
(3)由实验③可知12.54g沉淀的成分为
(4)综合上述实验,你认为以下结论正确的是
A.该混合溶液中一定含有K+、
 、
、 、
、 ,可能含Cl-,且n(K+)≥0.04mol
,可能含Cl-,且n(K+)≥0.04molB.该混合溶液中一定含有
 、
、 、
、 ,可能含Ba2+、K+、Cl-
,可能含Ba2+、K+、Cl-C.该混合溶液中一定含有
 、
、 、
、 ,可能含K+、Cl-
,可能含K+、Cl-D.该混合溶液中一定含有
 、
、 ,可能含K+、Cl-
,可能含K+、Cl-
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】有三溶液:a.Ba(OH)2,b.NaOH,c.NH3·H2O
(1)pH值相等时,三种溶液浓度由大到小的顺序为_________________
(2)物质的量浓度相等时,pH值由大到小的顺序为_________________
(3)pH=11时,各100mL与同浓度的HCl中和,消耗HCl体积由多到少的顺序为________________
(4)浓度相等时,各100mL与同浓度HCl中和,消耗HCl体积由多到少的顺序为_______________
(1)pH值相等时,三种溶液浓度由大到小的顺序为
(2)物质的量浓度相等时,pH值由大到小的顺序为
(3)pH=11时,各100mL与同浓度的HCl中和,消耗HCl体积由多到少的顺序为
(4)浓度相等时,各100mL与同浓度HCl中和,消耗HCl体积由多到少的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)用物质的量浓度为0.02mol/L的氢氧化钠溶液中和H+浓度为1×10-4 mol/L某一元弱酸溶液20mL,消耗氢氧化钠溶液50 mL,则此一元弱酸的物质的量浓度为_______ mol/L,Ka=_______ 。
(2)一定温度下,有①盐酸 ②硫酸 ③醋酸 三种酸,当三种酸的物质的量浓度相同且体积也相同时,同时与形状、密度、质量完全相同的锌(足量)反应,则开始时反应速率的大小关系是_______ (用序号填写,下同),相同状况下生成H2的体积大小关系是_______ 。
(1)用物质的量浓度为0.02mol/L的氢氧化钠溶液中和H+浓度为1×10-4 mol/L某一元弱酸溶液20mL,消耗氢氧化钠溶液50 mL,则此一元弱酸的物质的量浓度为
(2)一定温度下,有①盐酸 ②硫酸 ③醋酸 三种酸,当三种酸的物质的量浓度相同且体积也相同时,同时与形状、密度、质量完全相同的锌(足量)反应,则开始时反应速率的大小关系是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)配制FeSO4溶液时,常加入少量铁粉,目的是___________________________________ ;常加入少量H2SO4,目的是__________________________________________________ 。
(2)泡沫灭火剂包括Al2(SO4)3溶液(约1 mol·L-1)、NaHCO3溶液(约1 mol·L-1)及起泡剂。使用时发生的化学反应的离子方程式是_____________________________ 。
(3)已知 为难溶于水和酸的白色固体,
为难溶于水和酸的白色固体, 为难溶于水和酸是黑色固体。
为难溶于水和酸是黑色固体。 的悬浊液中加入足量的
的悬浊液中加入足量的 溶液并振荡,结果白色固体完全转化为黑色固体。
溶液并振荡,结果白色固体完全转化为黑色固体。
①写出白色固体转化黑色固体的化学方程式:____________________________ ;
②白色固体转化成黑色固体的原因是:__________________________________ 。
(4)已知下列物质在20℃下的Ksp如下,试回答下列问题:
①20℃时,上述四种银盐饱和溶液中,Ag+物质的量浓度由大到小的顺序是(填序号)_____________________ 。
②向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时, =
=_______________ 。
(2)泡沫灭火剂包括Al2(SO4)3溶液(约1 mol·L-1)、NaHCO3溶液(约1 mol·L-1)及起泡剂。使用时发生的化学反应的离子方程式是
(3)已知
 为难溶于水和酸的白色固体,
为难溶于水和酸的白色固体, 为难溶于水和酸是黑色固体。
为难溶于水和酸是黑色固体。 的悬浊液中加入足量的
的悬浊液中加入足量的 溶液并振荡,结果白色固体完全转化为黑色固体。
溶液并振荡,结果白色固体完全转化为黑色固体。 ①写出白色固体转化黑色固体的化学方程式:
②白色固体转化成黑色固体的原因是:
(4)已知下列物质在20℃下的Ksp如下,试回答下列问题:
| 化学式 | ① AgCl | ② AgBr | ③ Ag2S | ④ Ag2CrO4 |
| Ksp | 2.0×10-10 | 5.4×10-13 | 2.0×10-48 | 2.0×10-12 |
①20℃时,上述四种银盐饱和溶液中,Ag+物质的量浓度由大到小的顺序是(填序号)
②向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,
 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)配制 溶液时,常加入少量铁粉,目的是
溶液时,常加入少量铁粉,目的是_______ 。
(2)热的纯碱比冷的纯碱除油污效果好,原因是:_______ 。(用离子方程式及少量文字从平衡移动的角度进行解释)
(3)用离子方程式解释为什么不存在 :
:_______ 。
(4)书写以下溶液蒸干灼烧后得到的固体物质:
① 溶液——
溶液——_______ 。
② 溶液——
溶液——_______ 。
(1)配制
 溶液时,常加入少量铁粉,目的是
溶液时,常加入少量铁粉,目的是(2)热的纯碱比冷的纯碱除油污效果好,原因是:
(3)用离子方程式解释为什么不存在
 :
:(4)书写以下溶液蒸干灼烧后得到的固体物质:
①
 溶液——
溶液——②
 溶液——
溶液——
您最近一年使用:0次