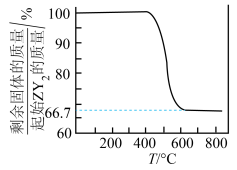
W、X、Y、Z为元素周期表中前四周期的元素,原子序数依次增大。W的一种核素无中子,X的最外层电子数是次外层的3倍,Y的原子M层有2对成对电子,Z的合金是用量最大、用途最广的合金。将ZY2在空气中氧化,测得氧化过程中剩余固体的质量与起始ZY2的质量的比值随温度变化的曲线如图所示。下列叙述正确

| A.W2X2为非极性分子 |
| B.W2Y2X8分子中X均为-2价 |
| C.ZY2是工业制备W2YX4的原料 |
| D.800℃时,ZY2氧化成含有两种元素的固体产物为Z3X4 |
23-24高三上·湖北恩施·阶段练习 查看更多[3]
湖北省部分重点中学2023届高三上学期第二次联考化学试题(已下线)专题卷09 根据原子结构和物质结构特点叙述型元素推断-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)湖北省恩施土家族苗族自治州2022-2023学年高三上学期期末考试化学试题
更新时间:2023-01-12 17:37:49
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】32g O2和1mol NO2进行比较,下列说法不正确的是( )
| A.分子数一定相同 | B.原子数一定不相同 |
| C.体积一定相同 | D.质量一定不相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温常压下,7g由N2与CO组成的混合物气体含有的原子数目为0.5NA |
| B.1L0.1mol·L-1硫酸钠溶液中含有的氧原子数为0.4NA |
| C.标准状况下,4.48LCl2通入水中,反应转移的电子数为0.2NA |
| D.5.6gFe与盐酸完全反应,转移的电子数为0.1NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知A,B,C,D,E是短周期中原子序数依次增大的5种元素,B、C同周期,D、E也同周期,D原子最外层电子数与最内层电子数相等,A,B,C,D的原子序数之和是E的两倍,D与C形成的化合物是一种耐高温材料,A、B形成的气态化合物的水溶液呈碱性。下列说法正确的是。
| A.A,B,C三种元素形成的化合物中肯定只含共价键 |
| B.A、C形成的化合物中只有A-C键 |
| C.工业上生产单质D可用海水作原料获得 |
| D.化合物DC与化合物EC2中化学键类型相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为18,X、Z基态原子的p轨道上均有2个未成对电子,W与X位于同一主族。下列说法正确的是
| A.WX2分子为极性分子 |
| B.元素电负性:Z>W |
| C.原子半径:r(W)>r(Z)>r(Y) |
| D.最高价氧化物水化物的酸性:Z>W |
您最近一年使用:0次
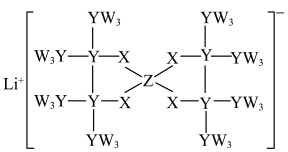
【推荐3】化合物M(结构如图所示)具有较大的阴离子,这使得其溶解度较大、电化学稳定性较高,因而被应用于电池电解液中。M的组成元素W、X、Y、Z、L均为短周期主族元素且原子半径依次增大,基态L原子仅s能级上填充电子,基态Y原子s能级上的电子数是p能级上的2倍,W的简单氢化物的沸点高于同主族相邻元素。下列说法正确的是
| A.元素的第一电离能:Y>X>W |
| B.M中属于p区的元素有4种 |
C.L形成的单质在X形成的单质中燃烧主要生成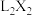 |
D.M中L和Z元素最外层均不满足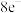 结构 结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】X、Y两元素可形成XY3型共价化合物,则X、Y最外层的电子排布可能是
| A.X:3s23p1 Y:3s23p4 | B.X:2s22p3 Y:2s22p4 |
| C.X:3s23p1 Y:2s22p5 | D.X:2s22p3 Y:1s1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关物质结构的说法正确的是
A. 和 和 中N原子VSEPR模型均为平面三角形 中N原子VSEPR模型均为平面三角形 |
B. 中C原子和N原子的杂化方式相同 中C原子和N原子的杂化方式相同 |
| C.基态Cr原子与基态Fe原子的未成对电子数相同 |
D.Se的轨道表示式若写作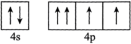 不符合洪特规则 不符合洪特规则 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.含有阴离子的晶体中必含有阳离子 |
| B.由极性键构成的AB2型分子必是极性分子 |
| C.非金属元素组成的化合物中只含有共价键 |
| D.离子晶体中必含有离子键,分子晶体中必含有共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法都正确的是
①CO和N2互为等电子体,且前者沸点低于后者;
②CH3-CH2-CH2-CH3和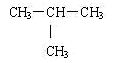 互为同分异构体,且前者熔沸点高于后者;
互为同分异构体,且前者熔沸点高于后者;
③BF3和NH3化学键的类型和分子的极性皆相同;
④F的电负性大于O,但H2O的熔沸点比HF高;
⑤CsCl晶格能小于NaCl;
⑥简单立方堆积和面心立方堆积是由非密置层堆积形成的;
①CO和N2互为等电子体,且前者沸点低于后者;
②CH3-CH2-CH2-CH3和
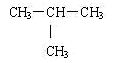 互为同分异构体,且前者熔沸点高于后者;
互为同分异构体,且前者熔沸点高于后者;③BF3和NH3化学键的类型和分子的极性皆相同;
④F的电负性大于O,但H2O的熔沸点比HF高;
⑤CsCl晶格能小于NaCl;
⑥简单立方堆积和面心立方堆积是由非密置层堆积形成的;
| A.①④⑥ | B.③④⑤ | C.②④⑤ | D.②④⑥ |
您最近一年使用:0次



