下表列出9种元素在元素周期表(元素周期表只给出部分)中的位置
请回答下列问题:
(1)考古工作者利用某元素的一种核素测定一些文物的年代,这种核素的元素符号是_______ 。
(2)写出由元素②和元素④形成原子个数比为1∶2的化合物的电子式:_______ 。
(3)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式为_______
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是_______ (填化学式;用“>”连接)。
(5)表中的ⅠA族、ⅡA族元素全部是金属元素,这种判断_______ (填“正确”或“错误”);根据元素周期律,自然界中最强的碱是_______ (填化学式)。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | |||||
| 4 | ⑨ |
(1)考古工作者利用某元素的一种核素测定一些文物的年代,这种核素的元素符号是
(2)写出由元素②和元素④形成原子个数比为1∶2的化合物的电子式:
(3)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式为
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是
(5)表中的ⅠA族、ⅡA族元素全部是金属元素,这种判断
22-23高一上·山东聊城·期末 查看更多[4]
江西省宜春市万载县万载二中 2023?2024 学年高一上学期期末模拟考试化学试卷安徽省六安市金寨县青山中学2023-2024学年高一下学期第一次月考化学试题(已下线)【知识图鉴】单元讲练测必修第一册第四单元03巩固练山东省莘县多校2022-2023学年高一上学期期末线上联考化学试题
更新时间:2023-01-16 23:08:34
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】用电子式表示下列物质的形成过程:
(1)CaCl2:_______ ;
(2)H2O:_______ 。
(1)CaCl2:
(2)H2O:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】判断正误
1.HCl的电子式: 。(_______)
。(_______)
2.CO2的电子式: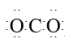 。(_______)
。(_______)
3.NaCl的电子式: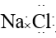 。(_______)
。(_______)
4.氯化镁的电子式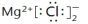 。(_______)
。(_______)
5.过氧化钠的电子式: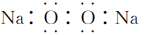 。(_______)
。(_______)
6.氨气的电子式: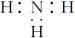 。(_______)
。(_______)
7.HClO电子式: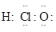 。(_______)
。(_______)
8.羟基的电子式: 。(_______)
。(_______)
9.氨基的电子式: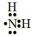 。(_______)
。(_______)
10. 。(_______)
。(_______)
11.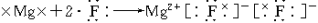 。(_______)
。(_______)
12.1个乙烷分子中存在8对共用电子对。(_______)
13.PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构。(_______)
1.HCl的电子式:
 。(_______)
。(_______)2.CO2的电子式:
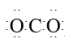 。(_______)
。(_______)3.NaCl的电子式:
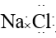 。(_______)
。(_______)4.氯化镁的电子式
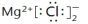 。(_______)
。(_______)5.过氧化钠的电子式:
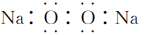 。(_______)
。(_______)6.氨气的电子式:
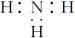 。(_______)
。(_______)7.HClO电子式:
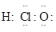 。(_______)
。(_______)8.羟基的电子式:
 。(_______)
。(_______)9.氨基的电子式:
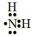 。(_______)
。(_______)10.
 。(_______)
。(_______)11.
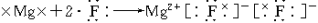 。(_______)
。(_______)12.1个乙烷分子中存在8对共用电子对。(_______)
13.PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构。(_______)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】《梦溪笔谈》有记:馆阁新书净本有误书处,以雌黄涂之。在中国古代,雌黄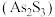 经常用来修改错字。
经常用来修改错字。
(1)S在元素周期表中的位置是第_______ 周期、第ⅥA族。
(2)写出S的最高价氧化物对应的水化物的化学式:_______ 。
(3)S的非金属性强于P的,用原子结构解释原因:S和P在同一周期,原子核外电子层数相同,_______ ,原子半径S小于P,得电子能力S强于P。
(4)在元素周期表中,砷( )位于第4周期,与P同主族。下列关于
)位于第4周期,与P同主族。下列关于 的推断中,正确的是
的推断中,正确的是_______ (填字母)。
a.原子的最外层电子数为5 b.原子半径: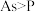 c.稳定性:
c.稳定性: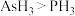
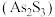 经常用来修改错字。
经常用来修改错字。(1)S在元素周期表中的位置是第
(2)写出S的最高价氧化物对应的水化物的化学式:
(3)S的非金属性强于P的,用原子结构解释原因:S和P在同一周期,原子核外电子层数相同,
(4)在元素周期表中,砷(
 )位于第4周期,与P同主族。下列关于
)位于第4周期,与P同主族。下列关于 的推断中,正确的是
的推断中,正确的是a.原子的最外层电子数为5 b.原子半径:
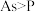 c.稳定性:
c.稳定性: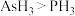
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】下表是元素周期表的一部分,针对表中的①~⑨九种元素,填写下列空白:
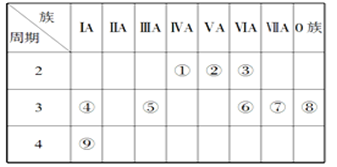
(1)在这些元素中,②位于元素周期表的第______ 纵行,④与③形成的淡黄色的固体的阴、阳离子的个数比为_______ 。
(2)用电子式表示元素④与⑥的化合物的形成过程__________________________
(3)元素③的简单氢化物常温下和元素⑦的单质反应的离子方程式为__________________ 。
(4)④⑤⑥⑦的简单离子半径由小到大为___________________ 。(用元素符号表示)
(5)元素③与元素⑥相比,能证明这两种元素非金属性强弱的事实是_______ (填选项序号)。
A.常温下③的单质和⑥的单质状态不同
B.③的简单氢化物比⑥的简单氢化物稳定
C.③的简单氢化物的沸点比⑥的简单氢化物的沸点高
D.③的单质能与⑥的简单氢化物反应生成⑥

(1)在这些元素中,②位于元素周期表的第
(2)用电子式表示元素④与⑥的化合物的形成过程
(3)元素③的简单氢化物常温下和元素⑦的单质反应的离子方程式为
(4)④⑤⑥⑦的简单离子半径由小到大为
(5)元素③与元素⑥相比,能证明这两种元素非金属性强弱的事实是
A.常温下③的单质和⑥的单质状态不同
B.③的简单氢化物比⑥的简单氢化物稳定
C.③的简单氢化物的沸点比⑥的简单氢化物的沸点高
D.③的单质能与⑥的简单氢化物反应生成⑥
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】按要求完成下列问题。
(1)硒(Se)是人体必需的微量元素,与O为同一主族元素,Se原子比O原子多两个电子层,则Se的原子序数为____ ,其最高价氧化物对应的水化物化学式为____ 。
(2)X射线衍射法可以测定某些分子结构,NH3分子结构为_____ 。
(3)水在液态时,几个水分子可以形成缔合水分子(H2O)n的原因是水分子之间存在____ 。
(4)漂白粉(有效成分Ca(ClO)2)与空气中CO2和水蒸气反应的化学方程式:____ 。
(5)完成氧化还原反应的离子方程式:____ 。
Cr2O +Fe2++_____=Cr3++Fe3++____
+Fe2++_____=Cr3++Fe3++____
(6)一定条件下金属钠和H2反应生成甲,甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。化合物甲和NaAlH4都是重要的还原剂。将4.80g甲加热至完全分解,得到金属钠和2.24L(已折算成标准状况)的H2。
①甲的化学式____ 。
②甲与AlCl3反应得到NaAlH4的化学方程式:____ 。
③NaAlH4与水发生氧化还原反应的化学方程式:____ 。
④甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式:____ 。
(1)硒(Se)是人体必需的微量元素,与O为同一主族元素,Se原子比O原子多两个电子层,则Se的原子序数为
(2)X射线衍射法可以测定某些分子结构,NH3分子结构为
(3)水在液态时,几个水分子可以形成缔合水分子(H2O)n的原因是水分子之间存在
(4)漂白粉(有效成分Ca(ClO)2)与空气中CO2和水蒸气反应的化学方程式:
(5)完成氧化还原反应的离子方程式:
Cr2O
 +Fe2++_____=Cr3++Fe3++____
+Fe2++_____=Cr3++Fe3++____(6)一定条件下金属钠和H2反应生成甲,甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。化合物甲和NaAlH4都是重要的还原剂。将4.80g甲加热至完全分解,得到金属钠和2.24L(已折算成标准状况)的H2。
①甲的化学式
②甲与AlCl3反应得到NaAlH4的化学方程式:
③NaAlH4与水发生氧化还原反应的化学方程式:
④甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】如图是元素周期表的一部分,请回答下列问题:
(1)在这些元素中,单质的化学性质最不活泼的 是______________ (填元素符号)。
(2)③的气态氢化物的电子式______________ ,②④形成的可溶于水的气态化合物的结构式______________ 。
(3)这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为______________ (填物质的化学式),酸性最强的含氧酸为______________ (填物质的化学式)。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在这些元素中,单质的化学性质
(2)③的气态氢化物的电子式
(3)这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】有四种短周期元素,相关信息如下表。
请根据表中信息回答:
(1) A在周期表中的位置______ 。
(2) B与C形成化合物的类型为______ (填“离子化合物”或“共价化合物”)
(3) 最高价氧化物对应的水化物的酸性C强于D,请用原子结构解释原因______ 。
(4) 已知硒(Se) 与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是______ 。
a.非金属性比D元素的强
b.SeO2既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为H2SeO4
| 元素 | 相关信息 |
| A | 气态氢化物极易溶于水,可用作制冷剂 |
| B | 单质的焰色反应为黄色 |
| C | 单质是黄绿色气体,可用于自来水消毒 |
| D | –2价阴离子的结构示意图是 |
请根据表中信息回答:
(1) A在周期表中的位置
(2) B与C形成化合物的类型为
(3) 最高价氧化物对应的水化物的酸性C强于D,请用原子结构解释原因
(4) 已知硒(Se) 与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
a.非金属性比D元素的强
b.SeO2既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为H2SeO4
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】已知有A、B、C、D、E五种短周期的主族元素,它们的原子序数依次递增,A是所有元素中原子半径最小的元素,B、C组成的某一种化合物能引起温室效应.常温下,金属D单质投入水中能与水剧烈反应.常温下E单质是常见的气体.请按要求回答下列几个问题:
(1)B、D的元素名称分别为:_____ 、_____ ;
(2)E在周期表中的位置为:_____ ,
(3)C离子的结构示意图为:_____ ;
(4)B、C、D三种元素的原子半径从大到小的顺序为_____ (用元素符号表示);
(5)B、E的最高价氧化物对应水化物的酸性从强到弱的顺序为:_____ (用对应的化学式表示)
(6)写出C、D两种元素组成的阴、阳离子个数比为1:2且只含离子键的化合物的电子式:_____ ;
(7)写出E与水反应的离子方程式:_____ .
(1)B、D的元素名称分别为:
(2)E在周期表中的位置为:
(3)C离子的结构示意图为:
(4)B、C、D三种元素的原子半径从大到小的顺序为
(5)B、E的最高价氧化物对应水化物的酸性从强到弱的顺序为:
(6)写出C、D两种元素组成的阴、阳离子个数比为1:2且只含离子键的化合物的电子式:
(7)写出E与水反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】⑴室温时,在下列物质中:①Na ②Cl2 ③Na2O ④FeCl2溶液 ⑤NaHCO3 ⑥蔗糖 ⑦NH3⑧NaCl晶体 ⑨HClO ⑩ Fe(OH)2
属于碱性氧化物的是(用序号填写,下同)__________ ,属于酸的是________ ,属于强电解质的是____________ ,属于非电解质的是____________ ,能导电的是___________ 。
⑵下列各组化学用语中:①3He、4He ② 2H2 O、1H2O ③ 1H、3H ④14N和13C质子数相同的有_________ ,中子数相同的有________ ,互为同位素的有________ 。
属于碱性氧化物的是(用序号填写,下同)
⑵下列各组化学用语中:①3He、4He ② 2H2 O、1H2O ③ 1H、3H ④14N和13C质子数相同的有
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在146C、147N、168O、3517Cl、23592U、23892U中:
(1)________ 和________ 互为同位素。
(2)________ 和________ 的质量数相等,但不能互称为同位素。
(3)________ 和________ 的中子数相等,但质子数不相等,所以不是同一种元素。
以上所共有________ 种元素。
(1)
(2)
(3)
以上所共有
您最近一年使用:0次

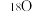 ;
;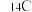 ;
;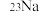 ;
;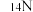 ;
;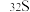 ;
; 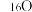 ;
;