H、N、 、S的原子半径由大到小的顺序为
、S的原子半径由大到小的顺序为_______ 。
 、S的原子半径由大到小的顺序为
、S的原子半径由大到小的顺序为
更新时间:2023-01-21 11:09:02
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3。请回答下列问题:
(1)Na3N的电子式是__ ,该化合物是由__ 键形成。
(2)Na3N与盐酸反应生成__ 种盐,反应的化学方程式是__ 。
(3)比较Na3N中两种微粒的半径:r(Na+)___ r(N3-)(填“>”、“=”、“<”)。
(1)Na3N的电子式是
(2)Na3N与盐酸反应生成
(3)比较Na3N中两种微粒的半径:r(Na+)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】元素周期表的建立是化学发展史上重要的里程碑之一,它揭示了元素之间的内在联系。如图是元素周期表的短周期示意图,相应方格中每个序号代表处于该位置的一种元素。
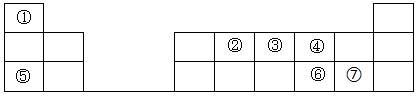
请回答下列问题:
(1)元素①的名称为___ 。
(2)元素③的最高价氧化物的水化物为___ (填化学式)
(3)⑥和⑦两种元素的气态氢化物中稳定性较强的是___ (填化学式)。
(4)②和④两种元素形成的常见气态化合物中化学键类型为___ 。
(5)⑤和⑦两种元素形成的化合物的电子式为___ 。

请回答下列问题:
(1)元素①的名称为
(2)元素③的最高价氧化物的水化物为
(3)⑥和⑦两种元素的气态氢化物中稳定性较强的是
(4)②和④两种元素形成的常见气态化合物中化学键类型为
(5)⑤和⑦两种元素形成的化合物的电子式为
您最近一年使用:0次
【推荐3】锶(Sr)位于元素周期表的第5周期ⅡA族。碳酸锶(SrCO3)是制取锶的原料,用天青石固体(主要成分SrSO4,难溶于水)和Na2CO3溶液混合浸泡可制取碳酸锶。
完成下列填空:
(1)在上述反应体系中出现的几种短周期元素,原子半径最大的是___________ ,非金属性最强的是___________ ;
(2)反应体系中出现的非金属元素可形成二硫化碳(CS2),其分子构型是直线型分子,写出该分子的电子式___________ ,该分子为___________ (选填“极性”、“非极性”)分子。
(3)已知:锶的原子序数为38,某锶原子的质量数为88,写出能包含这些信息的一种化学符号___________ ;写出锶原子的最外层电子排布式__________ 。
(4)下列关于锶及其化合物的叙述中,错误的是________ 。
a.锶的金属性比镁强 b.氢氢化锶呈两性
c.锶在化合物中呈+2价 d.锶在自然界中以游离态存在
完成下列填空:
(1)在上述反应体系中出现的几种短周期元素,原子半径最大的是
(2)反应体系中出现的非金属元素可形成二硫化碳(CS2),其分子构型是直线型分子,写出该分子的电子式
(3)已知:锶的原子序数为38,某锶原子的质量数为88,写出能包含这些信息的一种化学符号
(4)下列关于锶及其化合物的叙述中,错误的是
a.锶的金属性比镁强 b.氢氢化锶呈两性
c.锶在化合物中呈+2价 d.锶在自然界中以游离态存在
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】下表列出了A~R9种元素在周期表中的位置:
(1)在这9种元素中化学性质最不活泼的是_____
A.E B.D C.R D.H
(2)A、B、C三种元素按原子半径由大到小的顺序排列为_____
A.r(A)>r(B)>r(C) B.r(B)>r(A)>r(C)
C.r(A)>r(C)>r(B) D.r(B)>r(C)>r(A)
(3)F元素氢化物在常温下跟A发生反应所得溶液的pH______ 7
A.< B.> C.= D.无法确定
(4)在此周期表中,9种元素所形成的最高价氧化物对应的水化物,其中酸性最强和碱性最强的化学式是_____
A.H2SO4,NaOH B.H2SO4,KOH
C.HClO4,NaOH D.HClO4,KOH
(5)G元素和H元素两者核电荷数之差是_____
A.8 B.10 C.18 D.26
(6)H元素和A元素形成化合物的化学式以及高温灼烧该化合物时,火焰颜色____
A.NaBr 黄 B.NaCl 黄 C.KBr 紫 D.KCl 紫
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
A.E B.D C.R D.H
(2)A、B、C三种元素按原子半径由大到小的顺序排列为
A.r(A)>r(B)>r(C) B.r(B)>r(A)>r(C)
C.r(A)>r(C)>r(B) D.r(B)>r(C)>r(A)
(3)F元素氢化物在常温下跟A发生反应所得溶液的pH
A.< B.> C.= D.无法确定
(4)在此周期表中,9种元素所形成的最高价氧化物对应的水化物,其中酸性最强和碱性最强的化学式是
A.H2SO4,NaOH B.H2SO4,KOH
C.HClO4,NaOH D.HClO4,KOH
(5)G元素和H元素两者核电荷数之差是
A.8 B.10 C.18 D.26
(6)H元素和A元素形成化合物的化学式以及高温灼烧该化合物时,火焰颜色
A.NaBr 黄 B.NaCl 黄 C.KBr 紫 D.KCl 紫
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】氮化硅(Si3N4)陶瓷可代替金属制造发动机的耐热部件。工业上用气相沉淀法制备氨化硅: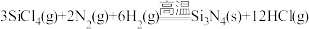 。请回答:
。请回答:
(1)Si原子与H原子结合时,Si呈正化合价,则电负性:Si___________ H(选填“<”或“>”)。
(2)Si4-与Cl-具有相同的电子构型,r(Si4-)大于r(Cl-),原因是___________ 。
(3)氮化硅(Si3N4)的晶体类型为___________
(4)锗(Ge)与Si是同一主族的元素。Ge元素可能的性质或应用有___________(填序号)。
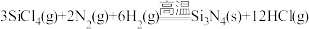 。请回答:
。请回答:(1)Si原子与H原子结合时,Si呈正化合价,则电负性:Si
(2)Si4-与Cl-具有相同的电子构型,r(Si4-)大于r(Cl-),原因是
(3)氮化硅(Si3N4)的晶体类型为
(4)锗(Ge)与Si是同一主族的元素。Ge元素可能的性质或应用有___________(填序号)。
| A.是一种活泼的金属元素 |
| B.其电负性大于硫 |
| C.其单质可作为半导体材料 |
| D.其气态氢化物的稳定性低于硅的气态氢化物 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】下表是元素周期表的一部分,请用化学符号和对应的化学式回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为___________ 。
(2)②、③两种元素非金属性较强的是___________ ,写出一个化学方程式能证明该结论的事实___________ 。⑧、⑨、⑩三种元素的气态氢化物稳定性由强到弱的顺序是___________ ,对应的的最高价氧化物的水化物中酸性最强的是___________ 。
(3)第三周期元素形成的简单离子中半径最小的微粒是___________ 。
(4)写出元素⑨的最高价氧化物对应水化物在水中的电离方程式:___________ 。写出实验室里,检验该水化物电离出的负离子的方法:___________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为
(2)②、③两种元素非金属性较强的是
(3)第三周期元素形成的简单离子中半径最小的微粒是
(4)写出元素⑨的最高价氧化物对应水化物在水中的电离方程式:
您最近一年使用:0次



