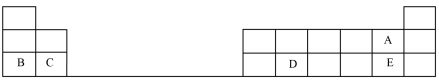
元素周期表的建立是化学发展史上重要的里程碑之一,它揭示了元素之间的内在联系。如图是元素周期表的短周期示意图,相应方格中每个序号代表处于该位置的一种元素。
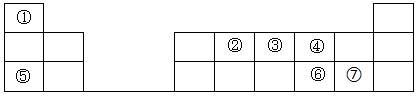
请回答下列问题:
(1)元素①的名称为___ 。
(2)元素③的最高价氧化物的水化物为___ (填化学式)
(3)⑥和⑦两种元素的气态氢化物中稳定性较强的是___ (填化学式)。
(4)②和④两种元素形成的常见气态化合物中化学键类型为___ 。
(5)⑤和⑦两种元素形成的化合物的电子式为___ 。

请回答下列问题:
(1)元素①的名称为
(2)元素③的最高价氧化物的水化物为
(3)⑥和⑦两种元素的气态氢化物中稳定性较强的是
(4)②和④两种元素形成的常见气态化合物中化学键类型为
(5)⑤和⑦两种元素形成的化合物的电子式为
更新时间:2021/05/28 10:53:49
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】元素周期表的一部分如图所示,其中每一个序号分别代表一种元素。回答下列问题。

(1)地壳中含量最多的金属元素为___________ (填化学式),该元素在元素周期表中的位置为___________ 。
(2)①和②形成的一种常温下极易溶于水且有刺激性气味的气体的电子式为___________ ,该物质___________ (填“属于”或“不属于”)电解质。
(3)③和④相比较,最简单氢化物的稳定性较强的是___________ (填化学式),简单离子半径:⑤___________ (填“>”、“<”或“=”)⑦。
(4)⑤和⑧相比较,金属性较强的是___________ (填元素符号),下列表述中,能证明这一事实的是___________ (填标号)。
A.⑤单质密度比⑧单质的大
B.⑧单质与水反应比⑤单质与水反应剧烈
C.⑤单质的熔点比⑧单质的高

(1)地壳中含量最多的金属元素为
(2)①和②形成的一种常温下极易溶于水且有刺激性气味的气体的电子式为
(3)③和④相比较,最简单氢化物的稳定性较强的是
(4)⑤和⑧相比较,金属性较强的是
A.⑤单质密度比⑧单质的大
B.⑧单质与水反应比⑤单质与水反应剧烈
C.⑤单质的熔点比⑧单质的高
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】若某非金属元素X的最高价氧化物对应的水化物的化学式为HnXOm,则X元素的族序数为______ ,它的最高价氧化物的化学式为______ ,氢化物的化学式为______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】某种牛奶的营养成分表如右图所示(NRV%是指每100g食品中营养素的含量占该营养素每日摄入量的比例)。
(1)请查阅资料,了解牛奶中的钙是以什么形式存在的_____ 。
(2)请查阅元素周期表,了解钙的有关信息,画出钙的原子结构示意图_____ 。
(3)已知与钙同族的镁能与 、
、 反应。请你参照第111页“整理与提升”的认识模型示例,或自己设计图示,推测钙的性质,并与同学交流
反应。请你参照第111页“整理与提升”的认识模型示例,或自己设计图示,推测钙的性质,并与同学交流_____ 。
(4)请你设计实验,比较镁、钙与水反应的难易程度_____ 。
(5)请结合钙的化学性质解释牛奶中钙的存在形式_____ 。
(1)请查阅资料,了解牛奶中的钙是以什么形式存在的
(2)请查阅元素周期表,了解钙的有关信息,画出钙的原子结构示意图
(3)已知与钙同族的镁能与
 、
、 反应。请你参照第111页“整理与提升”的认识模型示例,或自己设计图示,推测钙的性质,并与同学交流
反应。请你参照第111页“整理与提升”的认识模型示例,或自己设计图示,推测钙的性质,并与同学交流(4)请你设计实验,比较镁、钙与水反应的难易程度
(5)请结合钙的化学性质解释牛奶中钙的存在形式
| 营养成分表 | ||
| 项目 | 每100g | NRV% |
| 能量 | 309kJ | 4% |
| 蛋白质 | 3.6g | 6% |
| 脂肪 | 4.4g | 7% |
| 碳水化合物 | 5.0g | 2% |
| 钠 | 65mg | 3% |
| 钙 | 120mg | 15% |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】元素周期表是学习物质结构和性质的重要工具,如图是元素周期表的一部分,①~⑧分别代表一种元素。回答下列问题:
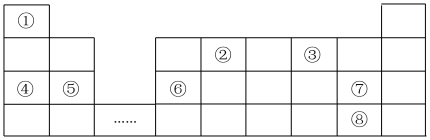
(1)元素①含2个中子的核素为_____ (填符号)。
(2)元素②、③形成的化合物_____ (填“属于”或“不属于”)电解质。
(3)元素③、⑤、⑦形成的简单离子半径由大到小的顺序为_____ (用离子符号填空)。
(4)元素④、⑤、⑥金属性由强到弱的顺序为_____ ,元素④和⑥的最高价氧化物对应的水化物反应的离子方程式为_____ 。
(5)将少量元素⑦的单质通入元素④与元素⑧形成化合物的水溶液中,溶液中的实验现象为_____ ,该反应的离子方程式为_____ 。

(1)元素①含2个中子的核素为
(2)元素②、③形成的化合物
(3)元素③、⑤、⑦形成的简单离子半径由大到小的顺序为
(4)元素④、⑤、⑥金属性由强到弱的顺序为
(5)将少量元素⑦的单质通入元素④与元素⑧形成化合物的水溶液中,溶液中的实验现象为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】人类利用化学反应不仅可以创造新物质,还能获取能量或实现不同形式能量之间的转化。已知下列化学反应方程式:
①氢气燃烧 ;
;
②太阳光分解水制氢气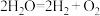 。
。
1.氧元素在元素周期表中的位置是___________ ,同周期非金属性最强的元素是___________ (填元素符号)。
2.反应①②是否构成可逆反应,请说明理由___________ 。
3.从能量转化角度分析,反应②为___________ 反应。(选填“吸热”或“放热”)反应②中主要能量转化形式为___________ 能转化为___________ 能。
4.100kPa时,单位质量或单位体积的燃料完全燃烧所放出的热量叫做该燃料的热值。根据下表一些燃料的热值及所学知识简要说明氢气作为能源的优点___________ 。
①氢气燃烧
 ;
;②太阳光分解水制氢气
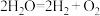 。
。1.氧元素在元素周期表中的位置是
2.反应①②是否构成可逆反应,请说明理由
3.从能量转化角度分析,反应②为
4.100kPa时,单位质量或单位体积的燃料完全燃烧所放出的热量叫做该燃料的热值。根据下表一些燃料的热值及所学知识简要说明氢气作为能源的优点
| 燃料 | 热值(kJ/g) |
| 氢气 | 142.9 |
| 一氧化碳 | 10.11 |
| 甲烷 | 55.64 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】填空:
(1)碱金属元素原子最外层的电子都是________ 个,在化学反应中它们容易失去________ 个电子。
(2)碱金属元素中还原性最强的是________ ,原子半径最小的是________ 。
(1)碱金属元素原子最外层的电子都是
(2)碱金属元素中还原性最强的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】下图是元素周期表的一部分,针对表中的①~⑥元素,回答下列问题
(1)最活泼的金属元素是_______________ (填元素符号)
(2)②和⑤两种元素原子半径较大的是_______________ (填元素符号),⑤和⑥两种元素最高价氧化物对应的水合物酸性较强的是_____________ (填元素符号);
(3)写出①的单质在⑥的单质中燃烧的化学方程式_______________________________________ 。
| 主族 周期 | ⅠA | 0族 | ||||||
一 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
二 | ② | |||||||
三 | ③ | ④ | ⑤ | ⑥ | ||||
(1)最活泼的金属元素是
(2)②和⑤两种元素原子半径较大的是
(3)写出①的单质在⑥的单质中燃烧的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】(1)在NaCl、NaOH、N2、H2O2、HCl中。只含有离子键的是________ ,只含有极性键的是_______ ,只含有非极性键的是_______ ,既含有离子键又含有极性键的是________ ,既含有极性键又含有非极性键的是____________ 。
(2)试分析下列各种情况下微粒间作用力的变化情况(填“离子键”“极性键”“非极性键”或“分子间作用力”):Na2O熔化时被破坏的化学键是__________ 。HCl溶于水时破坏__________ 。酒精溶于水时破坏__________ 。
(2)试分析下列各种情况下微粒间作用力的变化情况(填“离子键”“极性键”“非极性键”或“分子间作用力”):Na2O熔化时被破坏的化学键是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)已知:①金刚石;②MgF2;③NH4Cl;④固体碘;⑤Na2O2;⑥NaOH;⑦H2O2;⑧NH3;⑨N2;⑥HBr。用序号填写空白:只含非极性键而不含其他化学键的是_____ ;含有极性键和非极性键的是______ ;既存在离子键又存在共价键的是____ ;含有极性键的离子化合物是_____________ ,熔化时不需破坏化学键的是______________ 。
(2)若用50 mL 0.50 mol/L的盐酸与50 mL0.55 mol/L的NaOH溶液进行实验室的中和热测定,测定装置如图所示:

①仪器A的名称是________ ,碎泡沫塑料的作用是_______ ,大烧杯上如不盖硬纸板,则求得的中和热______ (填“偏大”、“偏小或“无影响")。
②某学生实验记录数据如下: ( 已知水的比热容c= 4. 18 J/(g·°C) 。
依据该学生的实验数据计算,该实验测得的中和热为△H=_______________ 。
③上述实验结果与57.3 kJ/mol(常温下中和热的值)有偏差,产生偏差的原因可能是(填字母)________ 。
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的温度
c.用量筒量取盐酸溶液的体积时仰视读数
d.分多次把NaOH溶液倒入盛有盐酸的小烧杯
(3)向50 mL0.50 mol/L的NaOH溶液中分别加入稀醋酸、稀盐酸、浓硫酸,则恰好完全反应时的放出热量Q1、Q2、 Q3从大到小的排序是_________________ 。
(2)若用50 mL 0.50 mol/L的盐酸与50 mL0.55 mol/L的NaOH溶液进行实验室的中和热测定,测定装置如图所示:

①仪器A的名称是
②某学生实验记录数据如下: ( 已知水的比热容c= 4. 18 J/(g·°C) 。
| 实验序号 | 起始温度t/℃ | 终止温度t/℃ | |
| 盐酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.0 | 20.2 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.4 | 20.6 | 24.0 |
③上述实验结果与57.3 kJ/mol(常温下中和热的值)有偏差,产生偏差的原因可能是(填字母)
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的温度
c.用量筒量取盐酸溶液的体积时仰视读数
d.分多次把NaOH溶液倒入盛有盐酸的小烧杯
(3)向50 mL0.50 mol/L的NaOH溶液中分别加入稀醋酸、稀盐酸、浓硫酸,则恰好完全反应时的放出热量Q1、Q2、 Q3从大到小的排序是
您最近一年使用:0次