碱式氯化铜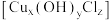 是一种难溶于水的固体,可溶于稀盐酸和氨水。
是一种难溶于水的固体,可溶于稀盐酸和氨水。
I.制备碱式氯化铜
向 溶液中通入
溶液中通入 ,滴加稀盐酸调节pH至5.0~5.5,控制反应温度为70-80℃。实验装置如图(部分加热和夹持装置略)。
,滴加稀盐酸调节pH至5.0~5.5,控制反应温度为70-80℃。实验装置如图(部分加热和夹持装置略)。
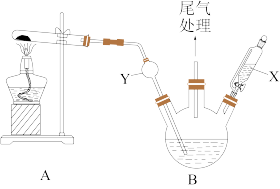
(1)仪器X的名称是_______ ;仪器Y的主要作用是_______ 。
(2)A装置试管中反应的化学方程式为_______ 。
(3)B中采用的加热方式是_______ 。滴入盐酸过量会导致碱式氯化铜的产量_______ (填“偏高”、“偏低”或“无影响”)。
(4)反应结束后,将三颈烧瓶中的混合物过滤、洗涤、干燥得到碱式氯化铜。判断沉淀洗涤干净的实验操作和现象是_______ 。
II.碱式氯化铜组成的测定
(5)称取定质量的碱式氯化铜,用少量稀 溶解后配成100.00mL待测液;取25.00mL待测液,加入足量
溶解后配成100.00mL待测液;取25.00mL待测液,加入足量 溶液,得
溶液,得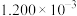 molAgCl;另取25.00mL待测液,调节pH至4~5,用浓度为0.08000
molAgCl;另取25.00mL待测液,调节pH至4~5,用浓度为0.08000 的EDTA
的EDTA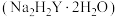 标准溶液滴定
标准溶液滴定 (
(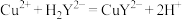 ),滴定至终点,消耗标准溶液30.00mL。该样品的化学式为
),滴定至终点,消耗标准溶液30.00mL。该样品的化学式为_______ 。
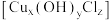 是一种难溶于水的固体,可溶于稀盐酸和氨水。
是一种难溶于水的固体,可溶于稀盐酸和氨水。I.制备碱式氯化铜
向
 溶液中通入
溶液中通入 ,滴加稀盐酸调节pH至5.0~5.5,控制反应温度为70-80℃。实验装置如图(部分加热和夹持装置略)。
,滴加稀盐酸调节pH至5.0~5.5,控制反应温度为70-80℃。实验装置如图(部分加热和夹持装置略)。
(1)仪器X的名称是
(2)A装置试管中反应的化学方程式为
(3)B中采用的加热方式是
(4)反应结束后,将三颈烧瓶中的混合物过滤、洗涤、干燥得到碱式氯化铜。判断沉淀洗涤干净的实验操作和现象是
II.碱式氯化铜组成的测定
(5)称取定质量的碱式氯化铜,用少量稀
 溶解后配成100.00mL待测液;取25.00mL待测液,加入足量
溶解后配成100.00mL待测液;取25.00mL待测液,加入足量 溶液,得
溶液,得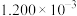 molAgCl;另取25.00mL待测液,调节pH至4~5,用浓度为0.08000
molAgCl;另取25.00mL待测液,调节pH至4~5,用浓度为0.08000 的EDTA
的EDTA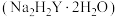 标准溶液滴定
标准溶液滴定 (
( ),滴定至终点,消耗标准溶液30.00mL。该样品的化学式为
),滴定至终点,消耗标准溶液30.00mL。该样品的化学式为
更新时间:2023-02-11 11:03:13
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某探究性学习小组在查阅资料中发现,常温下氯气可以氧化氨气获得氮气。该小组由此设计出制取氮气的思路:

实验室现有如下试剂及仪器:
试剂:①浓盐酸②饱和食盐水③浓硝酸④浓硫酸⑤碱石灰⑥二氧化锰⑦氯化铵⑧氢氧化钙
仪器:( 见图)请完成下列各题:
见图)请完成下列各题:

 写出制
写出制 的化学方程式:
的化学方程式:___________ 。
(2)用以上仪器(可重复使用)连接成制备纯净 、
、 的装置,按照前后顺序把图中的编号填入下表中,并写出对应仪器里试剂的编号。
的装置,按照前后顺序把图中的编号填入下表中,并写出对应仪器里试剂的编号。 下列空格不一定填满
下列空格不一定填满
(3)当反应装置里的氨气和氯气的物质的量之比大于__ 时,尾气里一定含有氨气。

实验室现有如下试剂及仪器:
试剂:①浓盐酸②饱和食盐水③浓硝酸④浓硫酸⑤碱石灰⑥二氧化锰⑦氯化铵⑧氢氧化钙
仪器:(
 见图)请完成下列各题:
见图)请完成下列各题:
 写出制
写出制 的化学方程式:
的化学方程式:(2)用以上仪器(可重复使用)连接成制备纯净
 、
、 的装置,按照前后顺序把图中的编号填入下表中,并写出对应仪器里试剂的编号。
的装置,按照前后顺序把图中的编号填入下表中,并写出对应仪器里试剂的编号。 下列空格不一定填满
下列空格不一定填满
制 | 仪器 | |||
| 试剂 | ||||
制 | 仪器 | |||
| 试剂 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某课外活动小组对教材中氨气的催化氧化实验进行了改进,并利用实验生成的产物检验氨的化学性质,实验装置如下(夹持装置略):

实验步骤如下:
①按装置图连接好装置,检查装置的气密性后,装入试剂;
②先点燃C处酒精灯,再点燃A处酒精灯,待F处有连续不断的气泡产生时,再点燃B处酒精灯;
③反应一段时间后,熄灭A处酒精灯;
④熄灭B处和C处酒精灯;
请回答下列问题:
(1)B装置中生成氨气的化学方程式为__________________ 。
(2)实验步骤①中检查装置的气密性的方法是___________ 。
(3)写出C中发生反应的化学方程式________________ 。
(4)描述实验过程中装置D和装置E的现象:
(5)装置F中的试剂是__________ 。

实验步骤如下:
①按装置图连接好装置,检查装置的气密性后,装入试剂;
②先点燃C处酒精灯,再点燃A处酒精灯,待F处有连续不断的气泡产生时,再点燃B处酒精灯;
③反应一段时间后,熄灭A处酒精灯;
④熄灭B处和C处酒精灯;
请回答下列问题:
(1)B装置中生成氨气的化学方程式为
(2)实验步骤①中检查装置的气密性的方法是
(3)写出C中发生反应的化学方程式
(4)描述实验过程中装置D和装置E的现象:
| 装置D | 装置E | |
| 点燃A、B、C处酒精灯 | 紫色石蕊溶液变红 | |
| 熄灭A处酒精灯继续加热B处酒精灯 | 红棕色慢慢褪去 | 溶液由红色变为蓝色, |
(5)装置F中的试剂是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氮是自然界各种生物体生命活动不可缺少的重要元素,氨元素的单质及化合物是中学化学中的重要物质。
(1)请回答下列问题:
① 的电子式为
的电子式为_______ 。
②下列说法涉及“氮的固定”的有_______ 。
A.谚语“雷雨发庄稼”
B.氨气遇到氯化氢时,生成氯化铵晶体
C.豆科植物的根瘤菌将氮气转化为氨
D.工业合成氨: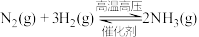
(2)某化学学习小组拟设计实验制取氨气并探究其有关性质,实验装置如下图。
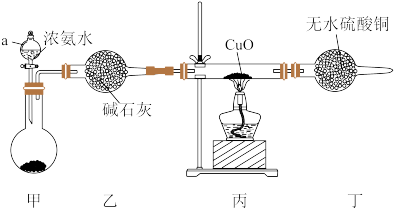
回答下列问题:
①仪器a的名称为_______ 。
②某同学提出该装置设计上有一定的缺陷,应在丁装置后添加一个盛有浓硫酸的洗气瓶,目的是_______ 。
③利用改进后的装置进行实验,一段时间后, 变为红色金属单质、无水
变为红色金属单质、无水 变蓝,同时生成一种无毒无污染的气体。根据上述信息写出
变蓝,同时生成一种无毒无污染的气体。根据上述信息写出 与
与 反应的化学方程式:
反应的化学方程式:_______ 。
④氨气可将有毒的 还原为氮气,该反应中氧化剂与还原剂的质量之比为
还原为氮气,该反应中氧化剂与还原剂的质量之比为_______ 。
(1)请回答下列问题:
①
 的电子式为
的电子式为②下列说法涉及“氮的固定”的有
A.谚语“雷雨发庄稼”
B.氨气遇到氯化氢时,生成氯化铵晶体
C.豆科植物的根瘤菌将氮气转化为氨
D.工业合成氨:
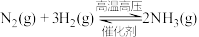
(2)某化学学习小组拟设计实验制取氨气并探究其有关性质,实验装置如下图。

回答下列问题:
①仪器a的名称为
②某同学提出该装置设计上有一定的缺陷,应在丁装置后添加一个盛有浓硫酸的洗气瓶,目的是
③利用改进后的装置进行实验,一段时间后,
 变为红色金属单质、无水
变为红色金属单质、无水 变蓝,同时生成一种无毒无污染的气体。根据上述信息写出
变蓝,同时生成一种无毒无污染的气体。根据上述信息写出 与
与 反应的化学方程式:
反应的化学方程式:④氨气可将有毒的
 还原为氮气,该反应中氧化剂与还原剂的质量之比为
还原为氮气,该反应中氧化剂与还原剂的质量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】PbI2(亮黄色粉末)是生产新型敏化太阳能电池的敏化剂——甲胺铅碘的原料。合成PbI2的实验流程如图1:
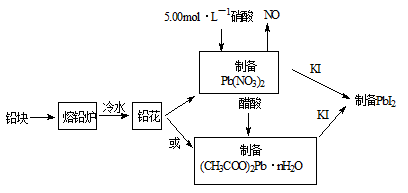

(1)将铅块制成铅花的目的是_____________ 。
(2)31.05g铅花用5.00mol·L-1的硝酸溶解,至少需消耗5.00 mol·L-1硝酸_______ mL。
(3)取一定质量(CH3COO)2Pb·nH2O样品在N2气氛中加热,测得样品固体残留率)( )随温度的变化如图2所示(已知:样品在75℃时已完全失去结晶水)。
)随温度的变化如图2所示(已知:样品在75℃时已完全失去结晶水)。
①(CH3COO)2Pb·nH2O中结晶水数目n=__________ (填整数)。
②100~200℃间分解产物为铅的氧化物和一种有机物,则该有机物为___________ (写分子式)。
(4)称取一定质量的PbI2固体,用蒸馏水配制成室温时的饱和溶液,准确移取25.00mL PbI2饱和溶液分次加入阳离子交换树脂RH中,发生:2RH(s) + Pb2+(aq) = R2Pb(s) +2H+(aq),用锥形瓶接收流出液,最后用蒸馏水淋洗树脂至流出液呈中性,将洗涤液合并到锥形瓶中。加入2~3滴酚酞溶液,用0.002500mol·L-1NaOH溶液滴定,到滴定终点时用去氢氧化钠标准溶液20.00mL。则室温时PbI2的Ksp为___________ 。
(5)探究浓度对磺化铅沉淀溶解平衡的影响。
该化学小组根据所提供试剂设计两个实验,来说明浓度对沉淀溶解平衡的影响。
提供试剂:NaI饱和溶液、NaCl饱和溶液、FeCl3饱和溶液、PbI2饱和溶液、PbI2悬浊液。
信息提示:Pb2+和Cl-能形成较稳定的PbCl42-络离子。
请填写下表的空白处:


(1)将铅块制成铅花的目的是
(2)31.05g铅花用5.00mol·L-1的硝酸溶解,至少需消耗5.00 mol·L-1硝酸
(3)取一定质量(CH3COO)2Pb·nH2O样品在N2气氛中加热,测得样品固体残留率)(
 )随温度的变化如图2所示(已知:样品在75℃时已完全失去结晶水)。
)随温度的变化如图2所示(已知:样品在75℃时已完全失去结晶水)。①(CH3COO)2Pb·nH2O中结晶水数目n=
②100~200℃间分解产物为铅的氧化物和一种有机物,则该有机物为
(4)称取一定质量的PbI2固体,用蒸馏水配制成室温时的饱和溶液,准确移取25.00mL PbI2饱和溶液分次加入阳离子交换树脂RH中,发生:2RH(s) + Pb2+(aq) = R2Pb(s) +2H+(aq),用锥形瓶接收流出液,最后用蒸馏水淋洗树脂至流出液呈中性,将洗涤液合并到锥形瓶中。加入2~3滴酚酞溶液,用0.002500mol·L-1NaOH溶液滴定,到滴定终点时用去氢氧化钠标准溶液20.00mL。则室温时PbI2的Ksp为
(5)探究浓度对磺化铅沉淀溶解平衡的影响。
该化学小组根据所提供试剂设计两个实验,来说明浓度对沉淀溶解平衡的影响。
提供试剂:NaI饱和溶液、NaCl饱和溶液、FeCl3饱和溶液、PbI2饱和溶液、PbI2悬浊液。
信息提示:Pb2+和Cl-能形成较稳定的PbCl42-络离子。
请填写下表的空白处:
| 实验内容 | 实验方法 | 实验现象及原因分析 |
| ①磺离子浓度增大对平衡的影响 | 取PbI2饱和溶液少量于一支试管中,再滴入几滴NaI饱和溶液 | 现象:溶液中c(I-)增大,使Q大于了PbI2的Ksp |
| ②铅离子浓度减小对平衡的影响 | 现象: 原因: | |
| ③ | 在PbI2悬浊液中滴入几滴FeCl3饱和溶液 | 现象:黄色浑浊消失 写出反应的离子方程式: |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】三氯氧磷(POCl3)是一种工业化工原料,可用于制取有机磷农药、长效磺胺药物等,还可用作染料中间体、有机合成的氯化剂和催化剂、阻燃剂等。利用O2和PCl3为原料可制备三氯氧磷,其制备装置如图所示(夹持装置略去):

已知PCl3和三氯氧磷的性质如表:
(1)仪器丙的名称是___________ ,实验过程中仪器丁的进水口为___________ (填“a”或“b”)口。
(2)装置B的作用是___________ (填标号)。
a.气体除杂b.加注浓硫酸c.观察气体流出速度d.调节气压
(3)写出装置C中发生反应的化学方程式___________ ,该装置中用温度计控制温度为60~65℃,原因是___________ 。
(4)称取16.73gPOCl3样品,配制成100mL溶液;取10.00mL溶液于锥形瓶中,加入3.2mol·L-1的AgNO3溶液10.00mL,并往锥形瓶中滴入5滴Fe2(SO4)3溶液;用0.20mol·L-1的KSCN溶液滴定,达到滴定终点时消耗KSCN溶液10.00mL(已知Ag++SCN-=AgSCN↓)。则加入Fe2(SO4)3溶液的作用是___________ ,样品中POCl3的纯度为___________ 。

已知PCl3和三氯氧磷的性质如表:
| 熔点/℃ | 沸点/℃ | 其他物理或化学性质 | |
| PCl3 | -112.0 | 76.0 | PCl3和POCl3互溶,均为无色液体,遇水均剧烈水解,发生复分解反应生成磷的含氧酸和HCl |
| POCl3 | 1.25 | 106.0 |
(2)装置B的作用是
a.气体除杂b.加注浓硫酸c.观察气体流出速度d.调节气压
(3)写出装置C中发生反应的化学方程式
(4)称取16.73gPOCl3样品,配制成100mL溶液;取10.00mL溶液于锥形瓶中,加入3.2mol·L-1的AgNO3溶液10.00mL,并往锥形瓶中滴入5滴Fe2(SO4)3溶液;用0.20mol·L-1的KSCN溶液滴定,达到滴定终点时消耗KSCN溶液10.00mL(已知Ag++SCN-=AgSCN↓)。则加入Fe2(SO4)3溶液的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学探究小组在实验室中制取Cl2并进行相关实验探究Cl2的性质。
I.制备Cl2实验
(1)实验室用浓盐酸与MnO2共热制取Cl2的化学方程式为___________ 。
(2)选用下列装置制取纯净干燥的Cl2,所需装置的接口连接顺序为:发生装置→___________ 。

(3)制备反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学提出下列实验方案:
甲方案:与足量AgNO3溶液反应,称量生成的AgCl质量。
乙方案:采用酸碱中和滴定法测定。
丙方案:与已知量CaCO3(过量)反应,称量剩余的CaCO3质量。
继而进行下列判断和实验:
①判定甲方案不可行,理由是___________ 。
②进行乙方案实验:准确量取残余清液稀释一定倍数后作为试样。
a.量取试样20.00mL,用0.1000 NaOH标准溶液滴定,消耗22.00mL,该次滴定测得试样中盐酸浓度为
NaOH标准溶液滴定,消耗22.00mL,该次滴定测得试样中盐酸浓度为___________  。
。
b.平行滴定后获得实验结果。
③判断丙方案的实验结果___________ (填“偏大”、“偏小”或“准确”)。
【已知: ,
,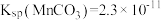 】
】
II.探究Cl2性质
(4)Cl2通入水中,所得溶液中具有氧化性的含氯粒子有___________ 。
(5)设计实验比较Cl2和Br2的氧化性,操作与现象是:取少量新制氯水和CCl4于试管中,___ 。
I.制备Cl2实验
(1)实验室用浓盐酸与MnO2共热制取Cl2的化学方程式为
(2)选用下列装置制取纯净干燥的Cl2,所需装置的接口连接顺序为:发生装置→

(3)制备反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学提出下列实验方案:
甲方案:与足量AgNO3溶液反应,称量生成的AgCl质量。
乙方案:采用酸碱中和滴定法测定。
丙方案:与已知量CaCO3(过量)反应,称量剩余的CaCO3质量。
继而进行下列判断和实验:
①判定甲方案不可行,理由是
②进行乙方案实验:准确量取残余清液稀释一定倍数后作为试样。
a.量取试样20.00mL,用0.1000
 NaOH标准溶液滴定,消耗22.00mL,该次滴定测得试样中盐酸浓度为
NaOH标准溶液滴定,消耗22.00mL,该次滴定测得试样中盐酸浓度为 。
。b.平行滴定后获得实验结果。
③判断丙方案的实验结果
【已知:
 ,
,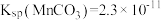 】
】II.探究Cl2性质
(4)Cl2通入水中,所得溶液中具有氧化性的含氯粒子有
(5)设计实验比较Cl2和Br2的氧化性,操作与现象是:取少量新制氯水和CCl4于试管中,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】 磁性材料在很多领域具有应用前景,其制备过程如下(各步均在
磁性材料在很多领域具有应用前景,其制备过程如下(各步均在 氛围中进行):
氛围中进行):
①称取 ,配成
,配成 溶液,转移至恒压滴液漏斗中。
溶液,转移至恒压滴液漏斗中。
②向三颈烧瓶中加入 溶液。
溶液。
③持续磁力搅拌,将 溶液以
溶液以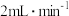 的速度全部滴入三颈烧瓶中,100℃下回流3h。
的速度全部滴入三颈烧瓶中,100℃下回流3h。
④冷却后过滤,依次用热水和乙醇洗涤所得黑色沉淀,在 干燥。
干燥。
⑤管式炉内焙烧2h,得产品3.24g。
部分装置如图:
(1)仪器a的名称是_______ ;使用恒压滴液漏斗的原因是_______ 。
(2)实验室制取 有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和装置,选出一种可行的方法,化学方程式为
有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和装置,选出一种可行的方法,化学方程式为_______ ,对应的装置为_______ (填标号)。
可供选择的试剂: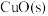 、
、 、
、 、
、 、饱和
、饱和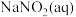 、饱和
、饱和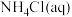
可供选择的发生装置(净化装置略去): ,离子方程式为
,离子方程式为_______ 。
(4)为保证产品性能,需使其粒径适中、结晶度良好,可采取的措施有_______。
(5)步骤④中判断沉淀是否已经用水洗涤干净,应选择的试剂为_______ ;使用乙醇洗涤的目的是_______ 。
(6)该实验所得磁性材料的产率为_______ (保留3位有效数字)。
 磁性材料在很多领域具有应用前景,其制备过程如下(各步均在
磁性材料在很多领域具有应用前景,其制备过程如下(各步均在 氛围中进行):
氛围中进行):①称取
 ,配成
,配成 溶液,转移至恒压滴液漏斗中。
溶液,转移至恒压滴液漏斗中。②向三颈烧瓶中加入
 溶液。
溶液。③持续磁力搅拌,将
 溶液以
溶液以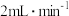 的速度全部滴入三颈烧瓶中,100℃下回流3h。
的速度全部滴入三颈烧瓶中,100℃下回流3h。④冷却后过滤,依次用热水和乙醇洗涤所得黑色沉淀,在
 干燥。
干燥。⑤管式炉内焙烧2h,得产品3.24g。
部分装置如图:
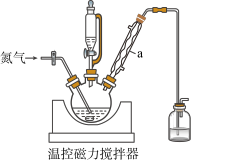
(1)仪器a的名称是
(2)实验室制取
 有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和装置,选出一种可行的方法,化学方程式为
有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和装置,选出一种可行的方法,化学方程式为可供选择的试剂:
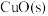 、
、 、
、 、
、 、饱和
、饱和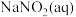 、饱和
、饱和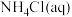
可供选择的发生装置(净化装置略去):

 ,离子方程式为
,离子方程式为(4)为保证产品性能,需使其粒径适中、结晶度良好,可采取的措施有_______。
| A.采用适宜的滴液速度 | B.用盐酸代替KOH溶液,抑制 水解 水解 |
| C.在空气氛围中制备 | D.选择适宜的焙烧温度 |
(6)该实验所得磁性材料的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】高锰酸钾是一种用途广泛的强氧化剂,实验室制备高锰酸钾所涉及的化学方程式如下:
MnO2熔融氧化:3MnO2+KClO3+6KOH 3K2MnO4+KCl+3H2O ;
3K2MnO4+KCl+3H2O ;
K2MnO4歧化:3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3。
请回答下列问题:
(1)在MnO2熔融氧化所得产物的热浸取液中通入CO2气体,使K2MnO4歧化的过程在如图装置中进行。

①检查虚框内装置气密性的方法是___________ 。
②仪器C的名称是___________ 。
(2)将C中所得产物进行过滤,将滤液倒入蒸发皿中,蒸发浓缩至溶液表面出现晶膜为止,自然冷却结晶,过滤,得到针状的高锰酸钾晶体。本实验应采用低温烘干的方法来干燥产品,原因是___________ 。
(3)利用氧化还原滴定法进行高锰酸钾纯度分析,原理为: 2 +5
+5 +6H+=2Mn2++5
+6H+=2Mn2++5 +3H2O
+3H2O
现称取制得的高锰酸钾产品7.245 g,配成500 mL溶液,用酸式滴定管准确量取25.00 mL待测液,用0.1000 mol·L-1亚硫酸钠标准溶液液进行滴定,终点时消耗标准液体积为50.0 0mL(不考虑其他因素的反应),如何判断滴定达到终点___________ ,高锰酸钾产品的纯度为___________ (保留4位有效数字,已知M(KMnO4)=158 g·mol-1);若酸式滴定管用蒸馏水洗净后没有用待测液润洗或烘干,则测定结果将______ 。(填“偏大”、“偏小”、“不变”)
MnO2熔融氧化:3MnO2+KClO3+6KOH
 3K2MnO4+KCl+3H2O ;
3K2MnO4+KCl+3H2O ;K2MnO4歧化:3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3。
请回答下列问题:
(1)在MnO2熔融氧化所得产物的热浸取液中通入CO2气体,使K2MnO4歧化的过程在如图装置中进行。

①检查虚框内装置气密性的方法是
②仪器C的名称是
(2)将C中所得产物进行过滤,将滤液倒入蒸发皿中,蒸发浓缩至溶液表面出现晶膜为止,自然冷却结晶,过滤,得到针状的高锰酸钾晶体。本实验应采用低温烘干的方法来干燥产品,原因是
(3)利用氧化还原滴定法进行高锰酸钾纯度分析,原理为: 2
 +5
+5 +6H+=2Mn2++5
+6H+=2Mn2++5 +3H2O
+3H2O现称取制得的高锰酸钾产品7.245 g,配成500 mL溶液,用酸式滴定管准确量取25.00 mL待测液,用0.1000 mol·L-1亚硫酸钠标准溶液液进行滴定,终点时消耗标准液体积为50.0 0mL(不考虑其他因素的反应),如何判断滴定达到终点
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】以黄铁矿为原料制硫酸会产生大量的废渣,合理利用废渣可以减少环境污染,变废为宝。工业上利用废渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe2O3)和回收(NH4)2SO4,具体生产流程如图:
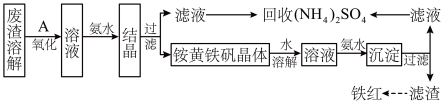
(1)在废渣溶解操作时,应选用___________溶解(填字母)。
(2)为了提高废渣的浸取率,可采用的措施有___________ , ___________ (至少写出两点)。
(3)物质A是一种氧化剂,工业上最好选用___________ (供选择使用的有:空气、Cl2、MnO2),其理由是___________ ,氧化过程中发生反应的离子方程式为___________ 。
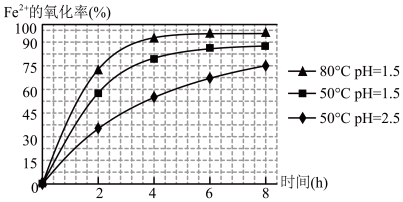
(4)根据如图有关数据,你认为工业上氧化操作时应控制的条件(从温度、pH和氧化时间三方面说明)是:___________ 。
(5)铵黄铁矾【NH4Fe(SO4)2】溶液中加入过量氨水发生反应的离子方程式是:_____

(1)在废渣溶解操作时,应选用___________溶解(填字母)。
| A.氨水 | B.氢氧化钠溶液 | C.盐酸 | D.硫酸 |
(3)物质A是一种氧化剂,工业上最好选用
(4)根据如图有关数据,你认为工业上氧化操作时应控制的条件(从温度、pH和氧化时间三方面说明)是:

(5)铵黄铁矾【NH4Fe(SO4)2】溶液中加入过量氨水发生反应的离子方程式是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】叠氮化钠(NaN3)是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原理、实验装置及实验步骤如下:
①关闭止水夹K2,打开止水夹K1,开始制取氨气。
②加热装置A中的金属钠,使其熔化并充分反应后,停止通入氨气并关闭止水夹K1。
③向装置A中的b容器内充入加热介质,并加热到210~220℃,然后打开止水夹K2,制取并通入N2O。
请回答下列问题:

(1)步骤①中先通氨气的目的是______ , 步骤②氨气与熔化的钠反应生成NaNH2的化学方程式为______ 。
(2)生成NaN3的化学方程式为______
(3)反应完全结束后,进行以下操作,得到NaN3固体:a中混合物

 NaN3固体。已知NaNH2能与水反应生成NaOH和氨气。操作II的目的是
NaN3固体。已知NaNH2能与水反应生成NaOH和氨气。操作II的目的是______ ,操作IV最好选用的试剂是______ 。
(4)实验室用滴定法测定叠氮化钠样品中NaN3的质量分数:①将2.500g试样配成500.00mL溶液。②取50.00mL溶液置于锥形瓶中,加入0.1010mol·L-1(NH4)2Ce(NO3)6溶液50.00mL。③充分反应后,将溶液稍稀释,向溶液中加入8mL浓硫酸,滴入3滴邻菲罗啉指示剂,用0.0500mol·L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+,消耗溶液体积为29.00mL。测定过程的反应方程式为:2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑、Ce4++Fe2+=Ce3++Fe3+,试样中NaN3的质量分数为______ 。(写出计算过程)
①关闭止水夹K2,打开止水夹K1,开始制取氨气。
②加热装置A中的金属钠,使其熔化并充分反应后,停止通入氨气并关闭止水夹K1。
③向装置A中的b容器内充入加热介质,并加热到210~220℃,然后打开止水夹K2,制取并通入N2O。
请回答下列问题:

(1)步骤①中先通氨气的目的是
(2)生成NaN3的化学方程式为
(3)反应完全结束后,进行以下操作,得到NaN3固体:a中混合物


 NaN3固体。已知NaNH2能与水反应生成NaOH和氨气。操作II的目的是
NaN3固体。已知NaNH2能与水反应生成NaOH和氨气。操作II的目的是(4)实验室用滴定法测定叠氮化钠样品中NaN3的质量分数:①将2.500g试样配成500.00mL溶液。②取50.00mL溶液置于锥形瓶中,加入0.1010mol·L-1(NH4)2Ce(NO3)6溶液50.00mL。③充分反应后,将溶液稍稀释,向溶液中加入8mL浓硫酸,滴入3滴邻菲罗啉指示剂,用0.0500mol·L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+,消耗溶液体积为29.00mL。测定过程的反应方程式为:2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑、Ce4++Fe2+=Ce3++Fe3+,试样中NaN3的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】金属钛在航天、医疗等领域有着广泛的应用。工业上用钛铁矿(主要成分为FeTiO3,含有Fe2O3、CaO、SiO2等杂质)为原料制备金属钛的工艺流程如下:
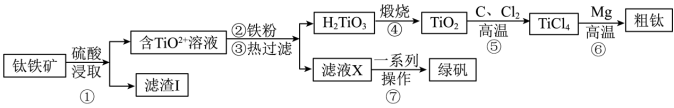
(1)钛的性质比铁活泼,但金属钛具有较强的抗腐蚀性,原因可能是___________ 。
(2)若转化①的反应中,用到了10L密度为1.83g·mL−1、质量分数为98%的浓硫酸,则其中所含H2SO4的物质的量为___________ 。
(3)“滤渣Ⅰ”的主要成分为___________ 。
(4)转化⑤反应中每消耗1molC,反应共转移2mol电子。该反应的化学方程式为___________ 。
(5)转化⑥有副产品MgCl2生成,为节约原料,实现物质的循环利用,对副产物MgCl2的最佳利用方式是___________ 。
(6)以绿矾(FeSO4·7H2O)为原料,可以制取铁铬氧体Cr2Fe20O27(Cr为+3价)。制取的方法如下:向含1mol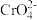 的溶液中,加入10mol FeSO4·7H2O,充分反应后向溶液中边通入空气边滴加NaOH溶液,反应后过滤得到铁铬氧体。反应共消耗O2的物质的量为
的溶液中,加入10mol FeSO4·7H2O,充分反应后向溶液中边通入空气边滴加NaOH溶液,反应后过滤得到铁铬氧体。反应共消耗O2的物质的量为___________ 。
(7)煅烧所得TiO2可以采用如下实验测定其纯度:称取2.000gTiO2样品,加酸溶解为TiO2+离子,向所得溶液中加入足量铝粉,充分反应后过滤,将滤液稀释定容至250mL,取25.00mL于锥形瓶中,加入指示剂,用0.1000mol·L−1NH4Fe(SO4)2标准溶液滴定,恰好完全反应时,消耗NH4Fe(SO4)2标准溶液的体积为23.00mL。实验过程中发生的反应如下:Al+3TiO2++6H+=Al3++3Ti3++3H2O,Fe3++Ti3++H2O=Fe2++TiO2++2H+。计算煅烧所得TiO2的纯度,并写出计算过程。___________

(1)钛的性质比铁活泼,但金属钛具有较强的抗腐蚀性,原因可能是
(2)若转化①的反应中,用到了10L密度为1.83g·mL−1、质量分数为98%的浓硫酸,则其中所含H2SO4的物质的量为
(3)“滤渣Ⅰ”的主要成分为
(4)转化⑤反应中每消耗1molC,反应共转移2mol电子。该反应的化学方程式为
(5)转化⑥有副产品MgCl2生成,为节约原料,实现物质的循环利用,对副产物MgCl2的最佳利用方式是
(6)以绿矾(FeSO4·7H2O)为原料,可以制取铁铬氧体Cr2Fe20O27(Cr为+3价)。制取的方法如下:向含1mol
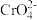 的溶液中,加入10mol FeSO4·7H2O,充分反应后向溶液中边通入空气边滴加NaOH溶液,反应后过滤得到铁铬氧体。反应共消耗O2的物质的量为
的溶液中,加入10mol FeSO4·7H2O,充分反应后向溶液中边通入空气边滴加NaOH溶液,反应后过滤得到铁铬氧体。反应共消耗O2的物质的量为(7)煅烧所得TiO2可以采用如下实验测定其纯度:称取2.000gTiO2样品,加酸溶解为TiO2+离子,向所得溶液中加入足量铝粉,充分反应后过滤,将滤液稀释定容至250mL,取25.00mL于锥形瓶中,加入指示剂,用0.1000mol·L−1NH4Fe(SO4)2标准溶液滴定,恰好完全反应时,消耗NH4Fe(SO4)2标准溶液的体积为23.00mL。实验过程中发生的反应如下:Al+3TiO2++6H+=Al3++3Ti3++3H2O,Fe3++Ti3++H2O=Fe2++TiO2++2H+。计算煅烧所得TiO2的纯度,并写出计算过程。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】化合物X由四种常见元素组成,摩尔质量为100g/mol~150g/mol,其焰色反应为黄色,X的水溶液能使紫色石蕊试液变红色。取一定量的X进行下图实验:
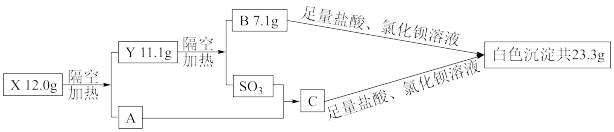
回答下列问题:
(1)X溶于水的电离方程式是____________________________________________________
(2)简述气体A的检验方法______________________________________________________
(3)Y→B+SO3的化学反应方程式___________________________________________________

回答下列问题:
(1)X溶于水的电离方程式是
(2)简述气体A的检验方法
(3)Y→B+SO3的化学反应方程式
您最近一年使用:0次



