下图为元素周期表的一部分 ,图中所列字母分别代表一种化学元素
(1)元素b、c、e形成的常见稳定单质中最易与H2化合的是_______ (填化学式)。
(2)元素d、e所形成的某化合物的摩尔质量为110 g·mol-1, 该化合物的化学式为_______ ,其中所含化学键的类型有_______ 。
(3)推测原子序数为35的元素在元素周期表中的位置是_______ 。
(4)依据元素周期律推测,元素f的单质及其化合物的性质正确的是_______(填字母)。
(5)气体分子(ab)2中各原子最外层都达到8电子结构,该分子的电子式为_______ ,(ab)2称为拟卤素,性质与卤素单质相似,常温下其与NaOH溶液反应的化学方程式为_______ 。
| a | b | c | |||||||||||||||
| d | e | ||||||||||||||||
| …… | f | ||||||||||||||||
(2)元素d、e所形成的某化合物的摩尔质量为110 g·mol-1, 该化合物的化学式为
(3)推测原子序数为35的元素在元素周期表中的位置是
(4)依据元素周期律推测,元素f的单质及其化合物的性质正确的是_______(填字母)。
| A.f的单质常温下呈气态 |
| B.f的单质具有强氧化性 |
| C.fc3属于酸性氧化物 |
| D.fc2既有氧化性又有还原性 |
更新时间:2023-02-09 14:39:22
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组用培养皿探究 的部分化学性质,装置如图。实验时向
的部分化学性质,装置如图。实验时向 固体上滴加浓盐酸,立即盖上盖子并观察现象。
固体上滴加浓盐酸,立即盖上盖子并观察现象。
已知:

回答下列问题:
(1)①中发生反应的离子方程式是_______ 。
(2)②、③的实验现象分别为_______ 、_______ 。
(3)④可观察到滴加有酚酞的 溶液褪色。甲同学认为溶液褪色是
溶液褪色。甲同学认为溶液褪色是 与水反应生成酸,酸和
与水反应生成酸,酸和 发生了中和反应。乙同学认为溶液褪色是因为
发生了中和反应。乙同学认为溶液褪色是因为 与水或
与水或 反应生成了具有漂白性的物质。要证实甲乙同学的观点可向④处滴加
反应生成了具有漂白性的物质。要证实甲乙同学的观点可向④处滴加_______ 溶液。
(4)该实验装置的优点是_______ (任写一条)。
 的部分化学性质,装置如图。实验时向
的部分化学性质,装置如图。实验时向 固体上滴加浓盐酸,立即盖上盖子并观察现象。
固体上滴加浓盐酸,立即盖上盖子并观察现象。已知:


回答下列问题:
(1)①中发生反应的离子方程式是
(2)②、③的实验现象分别为
(3)④可观察到滴加有酚酞的
 溶液褪色。甲同学认为溶液褪色是
溶液褪色。甲同学认为溶液褪色是 与水反应生成酸,酸和
与水反应生成酸,酸和 发生了中和反应。乙同学认为溶液褪色是因为
发生了中和反应。乙同学认为溶液褪色是因为 与水或
与水或 反应生成了具有漂白性的物质。要证实甲乙同学的观点可向④处滴加
反应生成了具有漂白性的物质。要证实甲乙同学的观点可向④处滴加(4)该实验装置的优点是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】完成下列问题。
(1)漂白粉和漂粉精是常用的消毒清洁用品,有效成分均为 ,相应的生产流程如下。
,相应的生产流程如下。
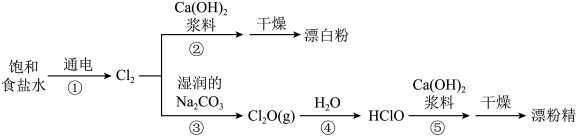
回答下列问题:
I.写出③中化学反应方程式为___________ 。
Ⅱ.上述过程不涉及反应主要有___________ 。
A.氧化还原反应B.化合反应C.复分解反应D.分解反应
(2) 的漂白能力是漂白粉的4~5倍,
的漂白能力是漂白粉的4~5倍, 广泛用于造纸工业、污水处理等。工业上生产
广泛用于造纸工业、污水处理等。工业上生产 的工艺流程如下:
的工艺流程如下:
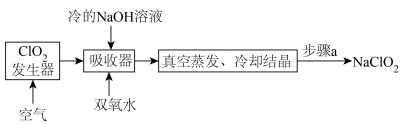
已知: 气体发生器中的反应为:
气体发生器中的反应为: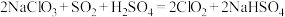 。
。
I.实际生产中可用硫磺、浓硫酸代替反应原料中的 ,其原因是
,其原因是___________ (用化学方程式表示)。
Ⅱ.步骤a的操作包括哪些具体步骤___________ ,反应结束后,向 发生器中通入一定量空气的目的:
发生器中通入一定量空气的目的:___________ 。
Ⅲ.吸收器中生成 的离子反应方程式为
的离子反应方程式为___________ ,吸收器中的反应温度不能太高,可能的原因为___________ 。
(1)漂白粉和漂粉精是常用的消毒清洁用品,有效成分均为
 ,相应的生产流程如下。
,相应的生产流程如下。
回答下列问题:
I.写出③中化学反应方程式为
Ⅱ.上述过程不涉及反应主要有
A.氧化还原反应B.化合反应C.复分解反应D.分解反应
(2)
 的漂白能力是漂白粉的4~5倍,
的漂白能力是漂白粉的4~5倍, 广泛用于造纸工业、污水处理等。工业上生产
广泛用于造纸工业、污水处理等。工业上生产 的工艺流程如下:
的工艺流程如下:
已知:
 气体发生器中的反应为:
气体发生器中的反应为: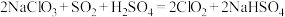 。
。I.实际生产中可用硫磺、浓硫酸代替反应原料中的
 ,其原因是
,其原因是Ⅱ.步骤a的操作包括哪些具体步骤
 发生器中通入一定量空气的目的:
发生器中通入一定量空气的目的:Ⅲ.吸收器中生成
 的离子反应方程式为
的离子反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】含氯消毒剂是消毒剂中常用的一类产品。
I.某实验小组用如图装置制备家用消毒液。
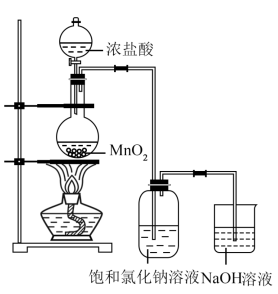
(1)图中盛装浓盐酸的仪器名称是___________ ,写出利用上述装置制备消毒液涉及的化学反应方程式,制氯气的反应方程式:__________ ,制消毒液的反应方程式:_____________ 。此方法获得的消毒液的有效成分是_________ (填名称)。
(2)洗气瓶中饱和氯化钠溶液的作用是_____________ 。
(3)此消毒液在使用时应注意一些事项,下列说法正确的是_____________ 。
a.与洁厕灵(含盐酸)混合使用效果更好
b.可以用于瓷砖、大理石地面的消毒
c.可以用于皮肤消毒
(4)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(g)+8NH3(g)=6NH4Cl(s)+N2(g),若反应中消耗Cl2 1.5个,则被氧化的NH3为______ 个,该过程中电子转移的总数为____ 个。
II.(5)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。氯酸钠与盐酸在50℃的条件下反应得到二氧化氯和氯气的混合气体。 控制50℃的加热方法是______ ,写出该反应的化学方程式___________ 。
I.某实验小组用如图装置制备家用消毒液。

(1)图中盛装浓盐酸的仪器名称是
(2)洗气瓶中饱和氯化钠溶液的作用是
(3)此消毒液在使用时应注意一些事项,下列说法正确的是
a.与洁厕灵(含盐酸)混合使用效果更好
b.可以用于瓷砖、大理石地面的消毒
c.可以用于皮肤消毒
(4)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(g)+8NH3(g)=6NH4Cl(s)+N2(g),若反应中消耗Cl2 1.5个,则被氧化的NH3为
II.(5)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。氯酸钠与盐酸在50℃的条件下反应得到二氧化氯和氯气的混合气体。 控制50℃的加热方法是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
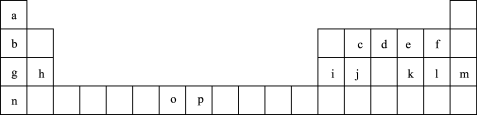
(1)基态o原子的外围电子排布图为_______ ;基态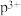 的最外层电子排布式为
的最外层电子排布式为_______ ;n的原子结构示意图为_______ 。表中所列元素的原子中,没有未成对电子的元素有_______ 种。
(2)原子序数为52的元素x在元素周期表中的位置为_______ 。
(3)上表中o、p两个字母表示的元素的第三电离能分别为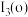 和
和 ,则
,则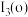
_______  (填“>”或“<”)。理由是
(填“>”或“<”)。理由是_______ 。
(4)将以上周期表中g、h、i、j四种元素的电负性由大到小排序为_______ (用元素符号表示),第一电离能由大到小排序_______ (用元素符号表示)。

(1)基态o原子的外围电子排布图为
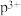 的最外层电子排布式为
的最外层电子排布式为(2)原子序数为52的元素x在元素周期表中的位置为
(3)上表中o、p两个字母表示的元素的第三电离能分别为
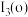 和
和 ,则
,则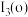
 (填“>”或“<”)。理由是
(填“>”或“<”)。理由是(4)将以上周期表中g、h、i、j四种元素的电负性由大到小排序为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表一种元素。
试回答下列问题(注意:每问中的字母代号为上表中的字母代号,并非为元素符号)
(1)N的单质和水蒸气反应能生成固体X,则I的单质与X高温下反应的化学方程式______ 。
(2)D的简单气态氢化物的VSEPR模型的名称为______ 。
(3)由A、C、D形成的ACD分子中,σ键和π键个数=______ 。
(4)元素M的化合物(ME2L2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。回答问题:
①ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是______ (填“极性”或“非极性”)分子。
②将N和O的单质用导线连接后插入D的最高价氧化物对应的水化物浓溶液中,可制成原电池,则组成负极材料的元素的外围电子轨道表示式为______ 。
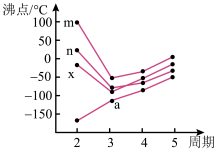
(5)如图四条折线分别表示ⅣA族、ⅤA族、ⅥA族、ⅦA族元素气态氢化物沸点变化,则E的氢化物所在的折线是______ (填m、n、x或y)。
| A | R | |||||||||||||||||
| B | C | D | E | F | T | |||||||||||||
| G | H | I | J | K | L | |||||||||||||
| M | N | O | ||||||||||||||||
试回答下列问题(注意:每问中的字母代号为上表中的字母代号,并非为元素符号)
(1)N的单质和水蒸气反应能生成固体X,则I的单质与X高温下反应的化学方程式
(2)D的简单气态氢化物的VSEPR模型的名称为
(3)由A、C、D形成的ACD分子中,σ键和π键个数=
(4)元素M的化合物(ME2L2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。回答问题:
①ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是
②将N和O的单质用导线连接后插入D的最高价氧化物对应的水化物浓溶液中,可制成原电池,则组成负极材料的元素的外围电子轨道表示式为
(5)如图四条折线分别表示ⅣA族、ⅤA族、ⅥA族、ⅦA族元素气态氢化物沸点变化,则E的氢化物所在的折线是

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】如图是部分短周期主族元素原子半径与原子序数的关系图。

回答下列问题(对应的微粒均用相应的元素符号表示):
(1)比较Z、Q两种元素的简单离子半径大小______ ;M的原子结构示意简图为______ 。
(2)图中最活泼的金属是______ ,将其单质在氧气中加热,生成的产物为______ 。
该元素的最高价氧化物对应的水化物与L的最高价氧化物对应的水化物发生反应的离子方程式为______ 。
(3)比较X、R两种元素的气态氢化物的沸点______ ;B的氢化物在常温下跟R的氢化物混合发生反应的化学方程式为______ ;现象为______ 。
(4)设计一个实验方案,比较X、Q单质氧化性的强弱:______ (注明操作、现象及结论)。

回答下列问题(对应的微粒均用相应的元素符号表示):
(1)比较Z、Q两种元素的简单离子半径大小
(2)图中最活泼的金属是
该元素的最高价氧化物对应的水化物与L的最高价氧化物对应的水化物发生反应的离子方程式为
(3)比较X、R两种元素的气态氢化物的沸点
(4)设计一个实验方案,比较X、Q单质氧化性的强弱:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、M、Q、R是六种短周期主族元素,其原子半径及主要化合价如下表所示:
(1)X、Y、Z的简单离子中,离子半径最小的是______ (填离子符号),R与Q按原子个数比为1:1形成的化合物T属于___________ 化合物(填“离子"或“共价”)。
(2)化合物T与化合物YQ2反应的化学方程式为:__________________________ 。
(3)Y、M两种元素相比较非金属性较强的是_______ (填元素符号),下列事实能证明这一结论的是______ (选填字母序号)。
a.简单气态氢化物的热稳定性:M> Y b. Y与M形成的化合物中Y呈正价
c. 常温下Y的单质呈固态,M的单质呈气态 d.简单氢化物的水溶液酸性;M>Y
e.含氧酸的酸性:HMO3> H2YO3
(4)以X、Z为电极材料,R的最高价氧化物对应的水化物为电解质溶液,将两电极用导线相连插入该电解质溶液中可形成原电池,该电池中正极材料为_______ (填材料名称),负极反应式为___________________________________ 。
| 元素代号 | X | Y | Z | M | Q | R |
| 原子半径/nm | 0.160 | 0.102 | 0.143 | 0.099 | 0.074 | 0.186 |
| 主要化合价 | +2 | +6、-2 | +3 | +7、-1 | -2 | + 1 |
(2)化合物T与化合物YQ2反应的化学方程式为:
(3)Y、M两种元素相比较非金属性较强的是
a.简单气态氢化物的热稳定性:M> Y b. Y与M形成的化合物中Y呈正价
c. 常温下Y的单质呈固态,M的单质呈气态 d.简单氢化物的水溶液酸性;M>Y
e.含氧酸的酸性:HMO3> H2YO3
(4)以X、Z为电极材料,R的最高价氧化物对应的水化物为电解质溶液,将两电极用导线相连插入该电解质溶液中可形成原电池,该电池中正极材料为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,A的简单离子半径是同周期元素简单离子中半径最小的,C的最简单氢化物的水溶液呈碱性。请回答下列问题:
(1)描述D在元素周期表中的位置:___________ ;B最简单的气态氢化物的电子式为:___________ 。
(2)在A、B、C、E四种元素最高价氧化物对应的水化物中酸性最强的是___________ (写化学式,下同),非金属最简单气态氢化物最不稳定的是 ___________ 。请写出B最简单的气态氢化物与E单质发生的第一步化学反应方程式___________ 。
(3)写出A的最高价氧化物与盐酸反应的离子方程式:___________ 。
| B | C | D | ||
| A | E |
(2)在A、B、C、E四种元素最高价氧化物对应的水化物中酸性最强的是
(3)写出A的最高价氧化物与盐酸反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:①___________ ,⑥___________ ,⑦___________ 。
(2)画出原子的结构示意图:④___________ ,⑤___________ ,⑧___________ 。
(3)在这些元素中,最活泼的金属元素是___________ ,最活泼的非金属元素是___________ ,最不活泼的元素是___________ 。(均用元素符号表示)
(4)在这些元素的最高价氧化物对应水化物中,酸性最强的是___________ ,碱性最强的是___________ ,(均写出物质的化学式)
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA |  |
 |  |  | ||||||
 |  |  |  |  |  |  |  | |
 |  | ⑪ |  |
(2)画出原子的结构示意图:④
(3)在这些元素中,最活泼的金属元素是
(4)在这些元素的最高价氧化物对应水化物中,酸性最强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E、F均为短周期元素,其原子序数依次增大。已知:A的最外层电子数等于其电子层数;B的最外层电子数是次外层电子数的两倍;D是地壳中含量最高的元素;D和F、A和E分别同主族;E是所有短周期主族元素中原子半径最大的元素。根据以上信息回答下列问题:
(1)B与D形成化合物BD2的结构式为___________ ,B元素形成的同素异形体的晶体类型可能是_____________ 。
(2)A、C、D三元素能形成一种强酸甲,写出单质B与甲的浓溶液反应的化学反应方程式______________ 。FD2气体通入BaCl2和甲的混合溶液,生成白色沉淀和无色气体CD,有关反应的离子方程式为_____________ 。
(3)均由A、D、E、F四种元素组成的两种盐,其相对分子质量相差16,写出它们在溶液中相互作用的离子方程式为___________ ;由B、D、E组成的盐溶于水后溶液显碱性,其原因是(用离子方程式表示)______________ 。
(4)C2A4 ─ 空气燃料电池是一种碱性燃料电池。电解质溶液是20%~30%的KOH溶液。则燃料电池放电时:正极的电极反应式是____________ 。
(1)B与D形成化合物BD2的结构式为
(2)A、C、D三元素能形成一种强酸甲,写出单质B与甲的浓溶液反应的化学反应方程式
(3)均由A、D、E、F四种元素组成的两种盐,其相对分子质量相差16,写出它们在溶液中相互作用的离子方程式为
(4)C2A4 ─ 空气燃料电池是一种碱性燃料电池。电解质溶液是20%~30%的KOH溶液。则燃料电池放电时:正极的电极反应式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】如表列出了九种元素在元素周期表中的位置。
请回答下列问题。
(1)元素①用于制造氢弹的两种核素的中子数分别为1和2,两者互称为______ ;当今考古工作者利用元素③的一种质量数为14的核素即(写出同位素原子符号)______ ,测定一些文物的年代,该核素的中子数为______ 。
(2)这九种元素中,原子半径最大的是_______ (填元素符号);元素⑦的最高氧化物对应水化物的化学式为______ 。
(3)③和⑥两种元素最高价氧化物对应的水化物中,酸性较强的是______ (填化学式)。③、④、⑤三种元素的简单气态氢化物中,稳定性最弱的是______ (填化学式)。
(4)元素X是比元素⑧质子数小8的同主族元素,其过氧化物的电子式为______ ;若将该过氧化物7.8g加入足量水充分反应,可制得的气体体积在标准状况下为_______ 。
(5)写出证明元素⑦比元素⑨非金属性强的反应的离子方程式:______ 。
| 周期 | IA | 0 | ||||||
| 一 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ||||||
| 四 | ⑧ | ⑨ |
(1)元素①用于制造氢弹的两种核素的中子数分别为1和2,两者互称为
(2)这九种元素中,原子半径最大的是
(3)③和⑥两种元素最高价氧化物对应的水化物中,酸性较强的是
(4)元素X是比元素⑧质子数小8的同主族元素,其过氧化物的电子式为
(5)写出证明元素⑦比元素⑨非金属性强的反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,按要求回答下列问题:
I.
(1)⑧的单质的电子式为_______ 。
(2)①~⑧对应元素中,非金属性最强的是_______ (填元素符号)。
(3)⑤⑥两种元素的最高价氧化物对应水化物中,碱性最强的是_______ (填化学式)。
(4)实验室用 和
和 制备②的简单氢化物,其化学方程式为
制备②的简单氢化物,其化学方程式为_______ 。
(5)下列不能用于验证氯元素比硫元素非金属性强的依据是_______(填字母)。
II.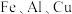 是重要的金属元素,它们的单质及其化合物在工业上有广泛的应用。
是重要的金属元素,它们的单质及其化合物在工业上有广泛的应用。
工业上用废铁锈(主要成分为 ,含少量的
,含少量的 与Cu)制取绿矾(
与Cu)制取绿矾( )的流程图如下。请回答下列问题。
)的流程图如下。请回答下列问题。

(6)X与Y分别为_______ 、_______ (填化学式)。
(7)废铁锈加入过量 溶液发生的离子方程式为
溶液发生的离子方程式为_______ 。
(8)流程中获得的Cu,可用铁盐溶解,写出反应的离子方程式为_______ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)⑧的单质的电子式为
(2)①~⑧对应元素中,非金属性最强的是
(3)⑤⑥两种元素的最高价氧化物对应水化物中,碱性最强的是
(4)实验室用
 和
和 制备②的简单氢化物,其化学方程式为
制备②的简单氢化物,其化学方程式为(5)下列不能用于验证氯元素比硫元素非金属性强的依据是_______(填字母)。
A. 比 比 稳定 稳定 |
B.铁与 反应生成 反应生成 ,而铁与硫反应生成 ,而铁与硫反应生成 |
C. 的酸性比 的酸性比 的强 的强 |
D. 的氧化性比 的氧化性比 的强 的强 |
II.
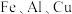 是重要的金属元素,它们的单质及其化合物在工业上有广泛的应用。
是重要的金属元素,它们的单质及其化合物在工业上有广泛的应用。工业上用废铁锈(主要成分为
 ,含少量的
,含少量的 与Cu)制取绿矾(
与Cu)制取绿矾( )的流程图如下。请回答下列问题。
)的流程图如下。请回答下列问题。
(6)X与Y分别为
(7)废铁锈加入过量
 溶液发生的离子方程式为
溶液发生的离子方程式为(8)流程中获得的Cu,可用铁盐溶解,写出反应的离子方程式为
您最近一年使用:0次



