某化学兴趣小组为了探究催化剂对H2O2分解速率的影响,进行了一系列实验,请回答相关问题。
(1)将0.10molMnO2粉末加入到40mLH2O2溶液中,在标准状况下放出气体的体积和时间的关系如右图所示。
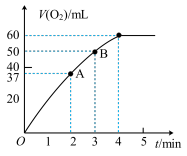
①该实验放出气体的总体积是_______ mL。
②A、B两点反应速率较慢的为_______ 点,理由是_______ 。
③H2O2的初始物质的量浓度是_______ (保留两位有效数字)。
(2)已知:Fe3+和Cu2+也能作为H2O2分解的催化剂,为了比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如下图甲、乙所示的实验。
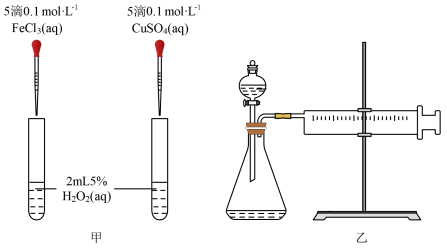
①定性分析:如图甲可通过观察_______ ,定性比较得出结论。小红认为此方案还需要进一步控制变量,提出可将试剂CuSO4更换为_______ (填化学式)。
②定量分析:如图乙所示,实验时均以生成40mL气体为标准,其它可能影响实验的因素均忽略。实验中需要测量的数据是_______ 。
(1)将0.10molMnO2粉末加入到40mLH2O2溶液中,在标准状况下放出气体的体积和时间的关系如右图所示。

①该实验放出气体的总体积是
②A、B两点反应速率较慢的为
③H2O2的初始物质的量浓度是
(2)已知:Fe3+和Cu2+也能作为H2O2分解的催化剂,为了比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如下图甲、乙所示的实验。

①定性分析:如图甲可通过观察
②定量分析:如图乙所示,实验时均以生成40mL气体为标准,其它可能影响实验的因素均忽略。实验中需要测量的数据是
更新时间:2023-02-13 15:45:37
|
相似题推荐
【推荐1】CO2和SO2的大量排放会对环境产生影响,科学家在积极探索用化学方法吸收并综合利用CO2和SO2。
I.重整吸收CO2.主要反应如下:
①CO2(g)+CH4(g)⇌2H2(g)+2CO(g) -Q1(Q1大于0)
②CO2(g)+H2(g)⇌H2O(g)+CO(g) -Q2(Q2大于0)
在容积固定的某密闭容器中,反应物投料比按n(CO2):n(CH4)=1:1发生上述反应,CO2、CH4的平衡转化率 随温度变化的曲线如图所示。
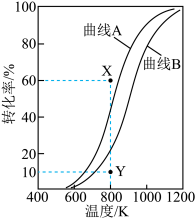
(1)根据消耗情况可以判断:图中曲线___________ (选填“A”或“B”)表示CO2的平衡转化率随温度的变化趋势。提高CH4的平衡转化率的措施为___________ (列举一条)。
(2)图中X点的v(CH4,正)___________ v(CH4,逆)。(选填“>”、“<”或“=”)若起始c(CO2)=2mol·L-1,反应至5min时,CH4的转化率到达Y点,且c(H2)为0.2mol·L-1,则0~5min内H2O(g)的平均反应速率v=___________ mol·L-1·min-1。
II.ZnO悬浊液吸收SO2,再催化氧化得到硫酸盐。
向ZnO悬浊液中缓缓通入SO2,SO2吸收率及溶液pH变化如图所示。已知:ZnSO3微溶于水,Zn(HSO3)2易溶于水。
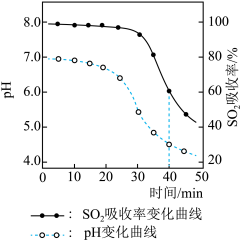
(3)在0~10min,溶液pH几乎保持不变,该阶段主要产物为___________ (填化学式);在30~40min,SO2吸收率迅速降低,该阶段主要反应的离子方程式为___________ 。
(4)调节吸收SO2所得溶液的pH为4.5~6.5,缓缓通入O2,则溶液pH将___________ (选填“增大”、“减小”或“不变”)。
I.重整吸收CO2.主要反应如下:
①CO2(g)+CH4(g)⇌2H2(g)+2CO(g) -Q1(Q1大于0)
②CO2(g)+H2(g)⇌H2O(g)+CO(g) -Q2(Q2大于0)
在容积固定的某密闭容器中,反应物投料比按n(CO2):n(CH4)=1:1发生上述反应,CO2、CH4的

(1)根据消耗情况可以判断:图中曲线
(2)图中X点的v(CH4,正)
II.ZnO悬浊液吸收SO2,再催化氧化得到硫酸盐。
向ZnO悬浊液中缓缓通入SO2,SO2吸收率及溶液pH变化如图所示。已知:ZnSO3微溶于水,Zn(HSO3)2易溶于水。

(3)在0~10min,溶液pH几乎保持不变,该阶段主要产物为
(4)调节吸收SO2所得溶液的pH为4.5~6.5,缓缓通入O2,则溶液pH将
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】在一容积为4 L的密闭容器中,加入0.4mol的N2和1.2mol的H2,在一定条件下发生如下反应:
N2(g)+3H2(g) 2NH3(g ) △H<0,反应中NH3的物质的量浓度变化情况如右图:
2NH3(g ) △H<0,反应中NH3的物质的量浓度变化情况如右图:
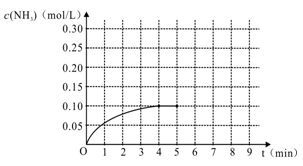
(1)根据上图,计算从反应开始到平衡时,平均反应速率v(H2)为____________ mol/(L·min)。
(2)该反应的化学平衡常数表达式K_____________ ,随温度的升高,K值将________ (填“增大”、“减小”“不变”)
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为______________ 。
A. 0.20 mol/L B. 0.12 mol/L C. 0.10 mol/L D. 0.08 mol/L
(4)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡___________________ 移动(填“向逆反应方向”、“向正反应方向”或“不”),化学平衡常数___________ (填“增大”、“减小”或“不变”)。
(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线___ 。
(6)在三个相同容器中各充入1 molN2和3molH2,在某一不同条件下反应并达到平衡,氨的体积分数随时间变化曲线如下图。下列说法正确的是___________ (填序号) 。
A.图Ⅰ可能是不同压强对反应的影响,且P2>P1
B.图Ⅱ可能是不同压强对反应的影响,且P1>P2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
D.图Ⅱ可能是同温同压下,催化剂性能对反应的影响,且1>2

N2(g)+3H2(g)
 2NH3(g ) △H<0,反应中NH3的物质的量浓度变化情况如右图:
2NH3(g ) △H<0,反应中NH3的物质的量浓度变化情况如右图:
(1)根据上图,计算从反应开始到平衡时,平均反应速率v(H2)为
(2)该反应的化学平衡常数表达式K
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为
A. 0.20 mol/L B. 0.12 mol/L C. 0.10 mol/L D. 0.08 mol/L
(4)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡
(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线
(6)在三个相同容器中各充入1 molN2和3molH2,在某一不同条件下反应并达到平衡,氨的体积分数随时间变化曲线如下图。下列说法正确的是
A.图Ⅰ可能是不同压强对反应的影响,且P2>P1
B.图Ⅱ可能是不同压强对反应的影响,且P1>P2
C.图Ⅲ可能是不同温度对反应的影响,且T1>T2
D.图Ⅱ可能是同温同压下,催化剂性能对反应的影响,且1>2

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】石油经分馏后可以获得汽油、煤油、柴油等含碳原子少的轻质油,但其产量难以满足社会需求,而含碳原子多的重油却供大于求。因此,需要通过催化裂化过程将重油裂化为汽油等物质,再进一步裂解,可以获得很多重要的化工原料。
以十六烷为例了解这一过程: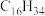 (十六烷)
(十六烷)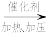 A(辛烷)+B(辛烯);A
A(辛烷)+B(辛烯);A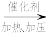 C+D(丁烷)
C+D(丁烷)
D(丁烷)继续分解可制得多种重要的基本化工原料:D(丁烷,g)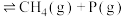 ;D(丁烷,g)
;D(丁烷,g)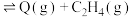
Ⅰ.向一体积为5 L的恒容密闭容器中充入2 mol丁烷,在一定温度和催化剂作用下发生上述2个分解反应,测得丁烷、甲烷的物质的量与时间关系如图所示。
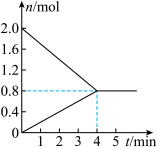
(1)下列数据中___________(填标号)不随时间变化能表明上述反应达到平衡状态。
(2)0~4 min内,乙烷的平均反应速率为___________  ;在该条件下,丁烷的平衡转化率为
;在该条件下,丁烷的平衡转化率为___________ 。
Ⅱ.关于A—D及D分解所得的有机物有如下问题:
(3)B中含有的官能团是:___________ (写结构式)。
(4)A有多种同分异构体,其中一种的分子结构中存在6个甲基,写出它与氯气进行一元取代的反应方程式:___________ 。
(5)Q与氯气在光照条件下反应可能得到的有机物共___________ 种,如果每一种有机产物生成量均相等,则3 mol Q需要与___________ mol氯气反应。
Ⅲ.P可通过加聚反应获得H。(一种常见的合成纤维——丙纶)及其他常见有机物E、F、G,过程如下图:
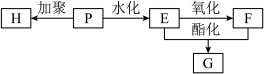
(6)写出H的结构简式___________ 。
(7)M既是G的同分异构体,又是F的同系物,满足此要求的有机物M共有___________ 种。
以十六烷为例了解这一过程:
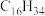 (十六烷)
(十六烷)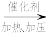 A(辛烷)+B(辛烯);A
A(辛烷)+B(辛烯);A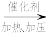 C+D(丁烷)
C+D(丁烷)D(丁烷)继续分解可制得多种重要的基本化工原料:D(丁烷,g)
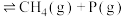 ;D(丁烷,g)
;D(丁烷,g)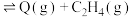
Ⅰ.向一体积为5 L的恒容密闭容器中充入2 mol丁烷,在一定温度和催化剂作用下发生上述2个分解反应,测得丁烷、甲烷的物质的量与时间关系如图所示。

(1)下列数据中___________(填标号)不随时间变化能表明上述反应达到平衡状态。
| A.碳原子总数 | B.总压强 | C.密度 | D.平均摩尔质量 |
 ;在该条件下,丁烷的平衡转化率为
;在该条件下,丁烷的平衡转化率为Ⅱ.关于A—D及D分解所得的有机物有如下问题:
(3)B中含有的官能团是:
(4)A有多种同分异构体,其中一种的分子结构中存在6个甲基,写出它与氯气进行一元取代的反应方程式:
(5)Q与氯气在光照条件下反应可能得到的有机物共
Ⅲ.P可通过加聚反应获得H。(一种常见的合成纤维——丙纶)及其他常见有机物E、F、G,过程如下图:

(6)写出H的结构简式
(7)M既是G的同分异构体,又是F的同系物,满足此要求的有机物M共有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】CO2的捕获是实现资源利用的重要途径。
(1)烟气中CO2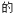 捕集可通过如下所示的物质转化实现。
捕集可通过如下所示的物质转化实现。_______ 。
(2)CO2和H2催化合成CH4。
主要发生反应为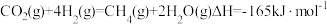 ,一定温度和压强下,将一定比例CO2和H2分别通过装有两种不同催化剂的反应器,反应相同时间,测得CO2转化率随温度变化情况如图1所示。
,一定温度和压强下,将一定比例CO2和H2分别通过装有两种不同催化剂的反应器,反应相同时间,测得CO2转化率随温度变化情况如图1所示。_______ 。
②高于320℃后,用Ni-CeO2作催化剂,CO2转化率略有下降,可能原因是_______ 。
(3)一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原CO2的装置示意图如图2所示。控制其他条件相同,将一定量的CO2通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图3所示。_______ 。
②b电极生成HCOOH的电极反应式为_______ 。
③科研小组利用13CO2代替原有的CO2进行研究,其目的是_______ 。
④控制电压为0.8V,电解时转移电子的物质的量为_______ mol。
(1)烟气中CO2
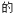 捕集可通过如下所示的物质转化实现。
捕集可通过如下所示的物质转化实现。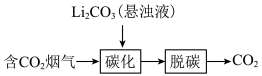
(2)CO2和H2催化合成CH4。
主要发生反应为
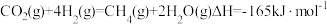 ,一定温度和压强下,将一定比例CO2和H2分别通过装有两种不同催化剂的反应器,反应相同时间,测得CO2转化率随温度变化情况如图1所示。
,一定温度和压强下,将一定比例CO2和H2分别通过装有两种不同催化剂的反应器,反应相同时间,测得CO2转化率随温度变化情况如图1所示。
②高于320℃后,用Ni-CeO2作催化剂,CO2转化率略有下降,可能原因是
(3)一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原CO2的装置示意图如图2所示。控制其他条件相同,将一定量的CO2通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图3所示。
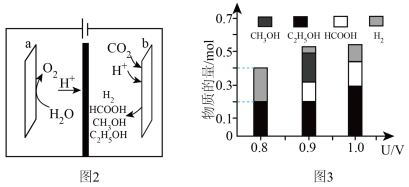
②b电极生成HCOOH的电极反应式为
③科研小组利用13CO2代替原有的CO2进行研究,其目的是
④控制电压为0.8V,电解时转移电子的物质的量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】 是形成PM2.5的重要前驱体,高效脱除
是形成PM2.5的重要前驱体,高效脱除 日趋成为重要的研究课题。
日趋成为重要的研究课题。
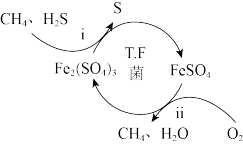
(1)生物技术在酸性溶液中,利用微生物T。F菌能够实现天然气中 的脱除,其原理如图所示。该脱除过程总反应的化学方程式为
的脱除,其原理如图所示。该脱除过程总反应的化学方程式为___________ 。
(2)化学技术利用高温加热法能够在脱除 的同时,还获得
的同时,还获得 和
和 ,实现资源再生,其反应原理为
,实现资源再生,其反应原理为 。
。
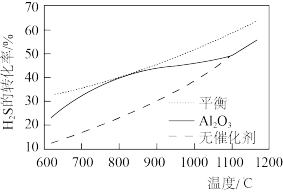
①常压下,将 以一定流速通过反应管,分别在无催化剂、
以一定流速通过反应管,分别在无催化剂、 作催化剂条件下,反应相同时间,实验测得
作催化剂条件下,反应相同时间,实验测得 的转化率与温度的关系如图示。温度高于1100℃后,无论是否使用催化剂
的转化率与温度的关系如图示。温度高于1100℃后,无论是否使用催化剂 ,
, 的转化率都几乎相等,其原因是
的转化率都几乎相等,其原因是___________ 。
②在 作催化剂条件下,保持反应器压强、温度不变,在
作催化剂条件下,保持反应器压强、温度不变,在 中按一定的比例掺入惰性气体Ar,能提高热分解反应时
中按一定的比例掺入惰性气体Ar,能提高热分解反应时 的平衡转化率,其原因是
的平衡转化率,其原因是___________ 。
(3)光催化技术在紫外光照射下, 光催化剂表面的活性位点能将空气中的
光催化剂表面的活性位点能将空气中的 和
和 转化成具有强氧化性的光生自由基,光生自由基再将已吸附在催化剂活性位点上的
转化成具有强氧化性的光生自由基,光生自由基再将已吸附在催化剂活性位点上的 快速氧化生成硫酸盐,实现
快速氧化生成硫酸盐,实现 的高效脱除。
的高效脱除。
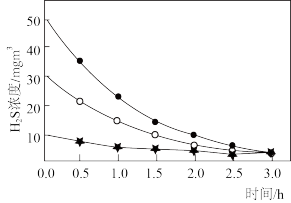
①其他条件相同,向装有8g 光催化剂的反应舱内通入
光催化剂的反应舱内通入 。调整
。调整 的不同初始浓度,反应舱内
的不同初始浓度,反应舱内 浓度随时间变化关系如图所示。结合光催化技术原理分析,
浓度随时间变化关系如图所示。结合光催化技术原理分析, 初始浓度较小,其脱除速率较慢的原因是
初始浓度较小,其脱除速率较慢的原因是___________ 。
(3分),
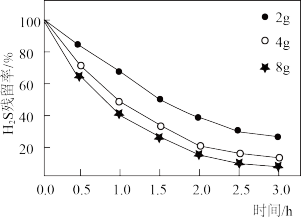
②其他条件相同,反应舱内 初始浓度为30 mg/m3。调整反应舱内
初始浓度为30 mg/m3。调整反应舱内 光催化剂的质量,
光催化剂的质量, 残留率随时间变化关系如图所示。随着
残留率随时间变化关系如图所示。随着 光催化剂的质量增加,
光催化剂的质量增加, 脱除速率逐渐提高,但提高的程度在逐渐减小,其原因可能是
脱除速率逐渐提高,但提高的程度在逐渐减小,其原因可能是___________ 。(3分)
 是形成PM2.5的重要前驱体,高效脱除
是形成PM2.5的重要前驱体,高效脱除 日趋成为重要的研究课题。
日趋成为重要的研究课题。(1)生物技术在酸性溶液中,利用微生物T。F菌能够实现天然气中
 的脱除,其原理如图所示。该脱除过程总反应的化学方程式为
的脱除,其原理如图所示。该脱除过程总反应的化学方程式为
(2)化学技术利用高温加热法能够在脱除
 的同时,还获得
的同时,还获得 和
和 ,实现资源再生,其反应原理为
,实现资源再生,其反应原理为 。
。①常压下,将
 以一定流速通过反应管,分别在无催化剂、
以一定流速通过反应管,分别在无催化剂、 作催化剂条件下,反应相同时间,实验测得
作催化剂条件下,反应相同时间,实验测得 的转化率与温度的关系如图示。温度高于1100℃后,无论是否使用催化剂
的转化率与温度的关系如图示。温度高于1100℃后,无论是否使用催化剂 ,
, 的转化率都几乎相等,其原因是
的转化率都几乎相等,其原因是
②在
 作催化剂条件下,保持反应器压强、温度不变,在
作催化剂条件下,保持反应器压强、温度不变,在 中按一定的比例掺入惰性气体Ar,能提高热分解反应时
中按一定的比例掺入惰性气体Ar,能提高热分解反应时 的平衡转化率,其原因是
的平衡转化率,其原因是(3)光催化技术在紫外光照射下,
 光催化剂表面的活性位点能将空气中的
光催化剂表面的活性位点能将空气中的 和
和 转化成具有强氧化性的光生自由基,光生自由基再将已吸附在催化剂活性位点上的
转化成具有强氧化性的光生自由基,光生自由基再将已吸附在催化剂活性位点上的 快速氧化生成硫酸盐,实现
快速氧化生成硫酸盐,实现 的高效脱除。
的高效脱除。①其他条件相同,向装有8g
 光催化剂的反应舱内通入
光催化剂的反应舱内通入 。调整
。调整 的不同初始浓度,反应舱内
的不同初始浓度,反应舱内 浓度随时间变化关系如图所示。结合光催化技术原理分析,
浓度随时间变化关系如图所示。结合光催化技术原理分析, 初始浓度较小,其脱除速率较慢的原因是
初始浓度较小,其脱除速率较慢的原因是(3分),

②其他条件相同,反应舱内
 初始浓度为30 mg/m3。调整反应舱内
初始浓度为30 mg/m3。调整反应舱内 光催化剂的质量,
光催化剂的质量, 残留率随时间变化关系如图所示。随着
残留率随时间变化关系如图所示。随着 光催化剂的质量增加,
光催化剂的质量增加, 脱除速率逐渐提高,但提高的程度在逐渐减小,其原因可能是
脱除速率逐渐提高,但提高的程度在逐渐减小,其原因可能是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】苯乙烯是重要的有机化工原料,可用乙苯为原料制备苯乙烯。制备方法有直接脱氢法和氧化脱氢法。在 时反应的热化学方程式及其平衡常数如下:
时反应的热化学方程式及其平衡常数如下:
(ⅰ)直接脱氢:
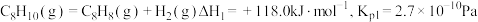
(ⅱ)氧化脱氢:

回答下列问题:
(1)①反应 的
的
_______  ,平衡常数
,平衡常数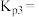
_______ (用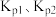 表示)。
表示)。
②氧化脱氢的反应趋势远大于直接脱氢,其原因是_______ 。
③提高氧化脱氢反应平衡转化率的措施有_______ 、_______ 。
(2)已知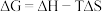 ,忽略
,忽略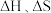 随温度的变化。当
随温度的变化。当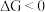 时,反应能自发进行。在
时,反应能自发进行。在 下,直接脱氢反应的
下,直接脱氢反应的 和
和 随温度变化的理论计算结果如图所示。
随温度变化的理论计算结果如图所示。

①直接脱氢反应在常温下_______ (选填“能”或“不能”)自发。
② 随温度的变化曲线为
随温度的变化曲线为_______ (选填“a”或“b”),判断的理由是_______ 。
③在某温度、 下,向密闭容器中通入
下,向密闭容器中通入 气态乙苯发生直接脱氢反应,达到平衡时,混合气体中乙苯和氢气的分压相等,该反应的平衡常数
气态乙苯发生直接脱氢反应,达到平衡时,混合气体中乙苯和氢气的分压相等,该反应的平衡常数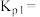
_______  (保留小数点后一位;分压
(保留小数点后一位;分压 总压
总压 物质的量分数)。
物质的量分数)。
(3)乙苯脱氢制苯乙烯往往伴随副反应,生成苯和甲苯等芳香烃副产物。一定温度和压强条件下,为了提高反应速率和苯乙烯选择性,应当_______ 。
 时反应的热化学方程式及其平衡常数如下:
时反应的热化学方程式及其平衡常数如下:(ⅰ)直接脱氢:
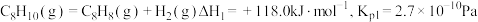
(ⅱ)氧化脱氢:

回答下列问题:
(1)①反应
 的
的
 ,平衡常数
,平衡常数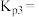
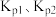 表示)。
表示)。②氧化脱氢的反应趋势远大于直接脱氢,其原因是
③提高氧化脱氢反应平衡转化率的措施有
(2)已知
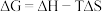 ,忽略
,忽略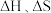 随温度的变化。当
随温度的变化。当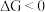 时,反应能自发进行。在
时,反应能自发进行。在 下,直接脱氢反应的
下,直接脱氢反应的 和
和 随温度变化的理论计算结果如图所示。
随温度变化的理论计算结果如图所示。
①直接脱氢反应在常温下
②
 随温度的变化曲线为
随温度的变化曲线为③在某温度、
 下,向密闭容器中通入
下,向密闭容器中通入 气态乙苯发生直接脱氢反应,达到平衡时,混合气体中乙苯和氢气的分压相等,该反应的平衡常数
气态乙苯发生直接脱氢反应,达到平衡时,混合气体中乙苯和氢气的分压相等,该反应的平衡常数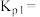
 (保留小数点后一位;分压
(保留小数点后一位;分压 总压
总压 物质的量分数)。
物质的量分数)。(3)乙苯脱氢制苯乙烯往往伴随副反应,生成苯和甲苯等芳香烃副产物。一定温度和压强条件下,为了提高反应速率和苯乙烯选择性,应当
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
【推荐1】为了探究AgNO3的氧化性和热稳定性,某化学兴趣小组设计了如下实验。
Ⅰ.AgNO3的氧化性
将光亮的铁丝伸入AgNO3溶液中,一段时间后将铁丝取出。为检验溶液中Fe的氧化产物,将溶液中的Ag+除尽后,进行了如下实验。可选用第试剂KSCN溶液、K3[Fe(CN)6]溶液、氯水。
(1)请完成下表:
【实验结论】Fe的氧化产物为存在Fe2+和Fe3+
Ⅱ. AgNO3的热稳定性性
用下图所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体。当反应结束以后,试管中残留固体为黑色。
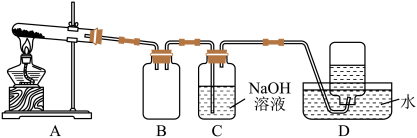
(2)装置B的作用是____________________ 。
(3)经小组讨论并验证该无色气体为O2,其验证方法是_____________________________ 。
(4)【查阅资料】Ag2O和粉末的Ag均为黑色;Ag2O可溶于氨水。
【提出假设】试管中残留的黑色固体可能是:ⅰAg;ⅱ.Ag2O;ⅲ.Ag和Ag2O
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验。
【实验评价】根据上述实验,不能确定固体产物成分的实验是__ (填实验编号)。
【实验结论】根据上述实验结果,该小组得出的AgNO3固体热分解的产物有__ 。
Ⅰ.AgNO3的氧化性
将光亮的铁丝伸入AgNO3溶液中,一段时间后将铁丝取出。为检验溶液中Fe的氧化产物,将溶液中的Ag+除尽后,进行了如下实验。可选用第试剂KSCN溶液、K3[Fe(CN)6]溶液、氯水。
(1)请完成下表:
| 操作 | 现象 | 结论 |
| 取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡 | 存在Fe3+ | |
| 取少量除尽Ag+后的溶液于试管中,加入 | 存在Fe2+ |
【实验结论】Fe的氧化产物为存在Fe2+和Fe3+
Ⅱ. AgNO3的热稳定性性
用下图所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体。当反应结束以后,试管中残留固体为黑色。

(2)装置B的作用是
(3)经小组讨论并验证该无色气体为O2,其验证方法是
(4)【查阅资料】Ag2O和粉末的Ag均为黑色;Ag2O可溶于氨水。
【提出假设】试管中残留的黑色固体可能是:ⅰAg;ⅱ.Ag2O;ⅲ.Ag和Ag2O
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验。
| 实验编号 | 操作 | 现象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硫酸,振荡 | 黑色固体溶解,并有气体产生 |
【实验评价】根据上述实验,不能确定固体产物成分的实验是
【实验结论】根据上述实验结果,该小组得出的AgNO3固体热分解的产物有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学利用Cl2氧化K2MnO4制备KMnO4的装置如下图所示(夹持装置略):
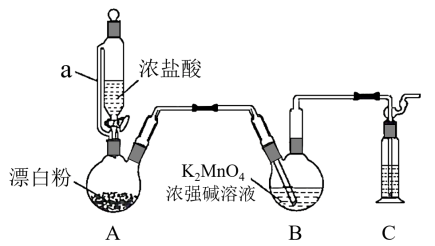
已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3MnO +2H2O=2MnO
+2H2O=2MnO +MnO2↓+4OH‒,回答下列问题:
+MnO2↓+4OH‒,回答下列问题:
(1)装置A中a的作用是___________ ;装置C中的试剂为___________ ;装置A中制备Cl2的化学方程式为___________ 。
(2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是___________ 。
(3) KMnO4常作氧化还原滴定的氧化剂,滴定时应将KMnO4溶液加入___________ (填“酸式”或“碱式”)滴定管中;
(4)某FeC2O4•2H2O样品中可能含有的杂质为Fe2(C2O4)3、H2C2O4•2H2O,采用KMnO4滴定法测定该样品的组成,实验步骤如下:
Ⅰ.称取mg样品于锥形瓶中,加入稀H2SO4溶解,水浴加热至75℃。用cmol•L-1的KMnO4溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗KMnO4溶液V1mL。
Ⅱ.向上述溶液中加入适量还原剂将Fe3+完全还原为Fe2+,加入稀H2SO4酸化后,在75℃继续用KMnO4溶液滴定至溶液出现粉红色且30s内不褪色,又消耗KMnO4溶液V2mL。样品中所含H2C2O4•2H2O (M=126g•mol-1)的质量分数表达式为___________ 。
下列关于样品组成分析的说法,正确的是___________ (填标号)。
A.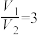 时,样品中一定不含杂质
时,样品中一定不含杂质
B.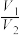 越大,样品中H2C2O4•2H2O含量一定越高
越大,样品中H2C2O4•2H2O含量一定越高
C. 若步骤Ⅰ中滴入KMnO4溶液不足,则测得样品中Fe元素含量偏低
D. 若所用KMnO4溶液实际浓度偏低,则测得样品中Fe元素含量偏高

已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3MnO
 +2H2O=2MnO
+2H2O=2MnO +MnO2↓+4OH‒,回答下列问题:
+MnO2↓+4OH‒,回答下列问题:(1)装置A中a的作用是
(2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是
(3) KMnO4常作氧化还原滴定的氧化剂,滴定时应将KMnO4溶液加入
(4)某FeC2O4•2H2O样品中可能含有的杂质为Fe2(C2O4)3、H2C2O4•2H2O,采用KMnO4滴定法测定该样品的组成,实验步骤如下:
Ⅰ.称取mg样品于锥形瓶中,加入稀H2SO4溶解,水浴加热至75℃。用cmol•L-1的KMnO4溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗KMnO4溶液V1mL。
Ⅱ.向上述溶液中加入适量还原剂将Fe3+完全还原为Fe2+,加入稀H2SO4酸化后,在75℃继续用KMnO4溶液滴定至溶液出现粉红色且30s内不褪色,又消耗KMnO4溶液V2mL。样品中所含H2C2O4•2H2O (M=126g•mol-1)的质量分数表达式为
下列关于样品组成分析的说法,正确的是
A.
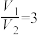 时,样品中一定不含杂质
时,样品中一定不含杂质B.
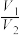 越大,样品中H2C2O4•2H2O含量一定越高
越大,样品中H2C2O4•2H2O含量一定越高C. 若步骤Ⅰ中滴入KMnO4溶液不足,则测得样品中Fe元素含量偏低
D. 若所用KMnO4溶液实际浓度偏低,则测得样品中Fe元素含量偏高
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】利用富锗ZnO烟尘(还含有CuO、CaO、PbO2、FeO、MnO2等)生产锗精矿和碱式碳酸锌[aZnCO3·bZn(OH)2]。其流程如下:
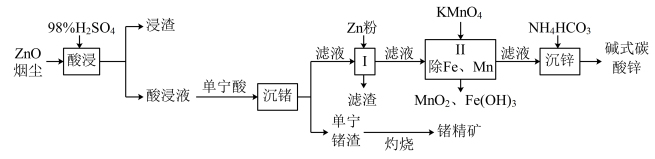
已知:酸浸时,锰与铅元素被还原为+2价,锗以Ge4+存在。
请回答:
(1)酸浸得到的浸渣主要含有的两种物质是______ (填化学式)。
(2)为了提高锗的浸出率,可以采取______ (填两种方法)。
(3)流程Ⅱ除Fe、Mn的过程中控制pH不宜过低,除防止锰的形态发生变化外,其原因还可能是______ 。
(4)沉锌中得到沉淀的化学式表示为aZnCO3·bZn(OH)2,为了确定其组成,称取34.9g该沉淀充分灼烧,最终获得24.3g氧化锌,计算确定aZnCO3·bZn(OH)2中a与b之比为______ ,则沉锌的化学方程式为______ 。

已知:酸浸时,锰与铅元素被还原为+2价,锗以Ge4+存在。
请回答:
(1)酸浸得到的浸渣主要含有的两种物质是
(2)为了提高锗的浸出率,可以采取
(3)流程Ⅱ除Fe、Mn的过程中控制pH不宜过低,除防止锰的形态发生变化外,其原因还可能是
(4)沉锌中得到沉淀的化学式表示为aZnCO3·bZn(OH)2,为了确定其组成,称取34.9g该沉淀充分灼烧,最终获得24.3g氧化锌,计算确定aZnCO3·bZn(OH)2中a与b之比为
您最近一年使用:0次



