电离平衡常数意义
电离平衡常数表示弱电解质的电离能力。一定温度下,K值_______ ,弱电解质的电离程度_______ ,酸性(或碱性)_______ 。
电离平衡常数表示弱电解质的电离能力。一定温度下,K值
22-23高二·全国·课时练习 查看更多[1]
(已下线)第三章水溶液中的离子反应与平衡——整体认识
更新时间:2023-03-08 17:53:02
|
【知识点】 电离平衡常数及影响因素解读
相似题推荐
填空题
|
容易
(0.94)
【推荐1】向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中 减小。( )
减小。( )
 减小。( )
减小。( )
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐2】电解质溶液中存在多种平衡。请回答下列问题:
(1)已知:
物质的量浓度均为0.1mol/L的下列溶液:a. CH3COOH b. HClO ,比较二者C(H+)的大小:a______ b(填“>”、“<”或“=”)。
(2)常温下,将 0.1mol/L 的 CH3COOH 溶液加水稀释,在稀释过程中,下列表达式的数值变大的__________ (填字母)。
A. c(H+) B. C. c(H+)·c(OH-)
C. c(H+)·c(OH-)
(3)25℃时,体积均为 10mL,pH 均为 2 的醋酸溶液与一元酸 HX 溶液分别加水稀释至 1000mL,稀释过程中 pH 的变化如图所示。已知:pH= -lgC(H+),则:
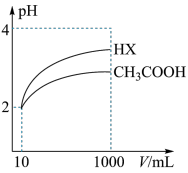
①25℃时,醋酸的电离常数________ HX的电离常数。(填“>”、“<”或“=”)
②稀释100倍后, 醋酸溶液中由水电离出的 c(H+)________ HX溶液中由水电离出的c(H+)。(填“>”、“<”或“=”)
(1)已知:
| 化学式 | CH3COOH | HClO |
| 电离常数(25℃) | 1.8×10-5 | 3.0×10-8 |
物质的量浓度均为0.1mol/L的下列溶液:a. CH3COOH b. HClO ,比较二者C(H+)的大小:a
(2)常温下,将 0.1mol/L 的 CH3COOH 溶液加水稀释,在稀释过程中,下列表达式的数值变大的
A. c(H+) B.
 C. c(H+)·c(OH-)
C. c(H+)·c(OH-) (3)25℃时,体积均为 10mL,pH 均为 2 的醋酸溶液与一元酸 HX 溶液分别加水稀释至 1000mL,稀释过程中 pH 的变化如图所示。已知:pH= -lgC(H+),则:

①25℃时,醋酸的电离常数
②稀释100倍后, 醋酸溶液中由水电离出的 c(H+)
您最近一年使用:0次



