电离平衡常数的影响因素
(1)内因:弱电解质本身的性质。
(2)外因:电离平衡常数只跟温度有关,温度_______ ,电离平衡常数_______ 。
(1)内因:弱电解质本身的性质。
(2)外因:电离平衡常数只跟温度有关,温度
22-23高二·全国·课时练习 查看更多[1]
(已下线)第三章水溶液中的离子反应与平衡——整体认识
更新时间:2023-03-08 17:53:02
|
【知识点】 电离平衡常数及影响因素解读
相似题推荐
填空题
|
容易
(0.94)
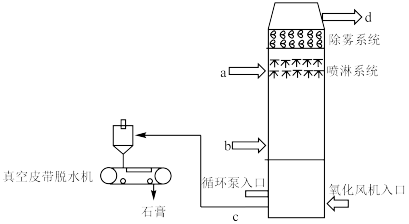
【推荐1】下图是石灰石膏法脱硫的示意图。烟气在脱硫塔内与脱硫剂(石灰石/生石灰浆液)接触混合,继而与鼓入的空气中的氧气发生化学反应,生成石膏(CaSO4·2H2O)。脱硫后的烟气经过除雾器除去雾滴后,排至大气。
1.烟气进口:_____ 。(填a或b)
2.为避免操作不当引起的中间产物CaSO3结垢和堵塞现象,某公司在脱硫剂中加入少量甲酸,效果很好。写出少量甲酸和CaSO3反应的化学方程式:_____ 。
| HCOOH | Ka=1.80×10-4 | |
| H2SO3 | Ka1=1.2×10-2 | Ka2=6.2×10-8 |
| H2CO3 | Ka1=4.2×10-7 | Ka2=4.8×10-11 |
1.烟气进口:
2.为避免操作不当引起的中间产物CaSO3结垢和堵塞现象,某公司在脱硫剂中加入少量甲酸,效果很好。写出少量甲酸和CaSO3反应的化学方程式:
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】H2A(酸):K1=4.3×10-6,K2=2.1×10-9.H2B(酸):K1=1.0×10-4,K2=6.3×10-8,在浓度相同的对应溶液中,用“>”、“<”或“=”填空。
(1)中和同浓度、同体积NaOH溶液时的用量:H2A溶液______ H2B溶液;
(2)c (Na+):Na2A溶液______ Na2B溶液;
(3)pH:H2A溶液______ H2B溶液;
(4)酸分子的浓度:NaHA溶液______ NaHB溶液;
(5)酸根离子的浓度:NaHA溶液______ NaHB溶液;
(1)中和同浓度、同体积NaOH溶液时的用量:H2A溶液
(2)c (Na+):Na2A溶液
(3)pH:H2A溶液
(4)酸分子的浓度:NaHA溶液
(5)酸根离子的浓度:NaHA溶液
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】已知25℃时部分弱电解质的电离平衡常数如下表:
回答下列问题:
(1)物质的量浓度均为0.1mol·L-1的四种溶液:
a.CH3COOH b.Na2CO3 c.NaClO d.NaHCO3
pH由小到大的排列顺序是__________ (用字母表示)。
(2)常温下,0.1mol·L-1的CH3COOH溶液加稀释过程中,下列表达式的数据变大的是________ 。
A.c(H+) B. C.c(H+)·c(OH-) D.
C.c(H+)·c(OH-) D.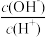
(3)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示:

则HX的电离平衡常数________ CH3COOH的电离平衡常数(填大于、小于或等于),理由是______________________________ 。
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=______ mol·L-1(填精确值),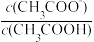 =
=_______ 。
| 化学式 | CH3COOH | H2CO3 | HClO |
| 平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
回答下列问题:
(1)物质的量浓度均为0.1mol·L-1的四种溶液:
a.CH3COOH b.Na2CO3 c.NaClO d.NaHCO3
pH由小到大的排列顺序是
(2)常温下,0.1mol·L-1的CH3COOH溶液加稀释过程中,下列表达式的数据变大的是
A.c(H+) B.
 C.c(H+)·c(OH-) D.
C.c(H+)·c(OH-) D.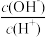
(3)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示:

则HX的电离平衡常数
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=
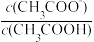 =
=
您最近一年使用:0次



