化学是一门实用性很强的科学,请根据题意填空:
(1)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装___________ (填“浓硫酸”或“浓盐酸”)。
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是___________ (填化学式)。
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质,请完成一定条件下该反应的化学方程式:2NO+2CO 2CO2+
2CO2+__________ 。
(4)“厉害了,我的国”,2017年4月:“天舟一号”成功对接,12月:大型客机C919(如下图)第二次在上海浦东机场试飞成功,实现了我国航空领域的新突破。
请回答下列问题:

①铝合金和碳纤维复合材料是飞机、火箭的常用材料,这主要利用了它们具有的共同性能是___________ (填字母序号)。
A.密度小 强度好 B.密度大 硬度大 C.熔点低 硬度小
②铝的金属活动性比铁的___________ (填“强”或“弱”),空气中,铝比铁具有更好的抗腐蚀性,原因是___________ (用化学反应方程式解释)。
③高温结构陶瓷可用于制造汽车发动机,通常所用的材料是氮化硅(Si3N4),该化合物中硅元素的化合价为___________ 。
(1)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质,请完成一定条件下该反应的化学方程式:2NO+2CO
 2CO2+
2CO2+(4)“厉害了,我的国”,2017年4月:“天舟一号”成功对接,12月:大型客机C919(如下图)第二次在上海浦东机场试飞成功,实现了我国航空领域的新突破。
请回答下列问题:

①铝合金和碳纤维复合材料是飞机、火箭的常用材料,这主要利用了它们具有的共同性能是
A.密度小 强度好 B.密度大 硬度大 C.熔点低 硬度小
②铝的金属活动性比铁的
③高温结构陶瓷可用于制造汽车发动机,通常所用的材料是氮化硅(Si3N4),该化合物中硅元素的化合价为
更新时间:2023/03/12 11:59:19
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】将高温水蒸气通到硫氰化钾的表面,会发生反应: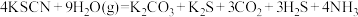 。完成下列填空:
。完成下列填空:
(1)上述反应所涉及的各元素中,简单离子半径最大的是_______ (填写离子符号); 中含有的化学键类型是
中含有的化学键类型是_______ 。
(2)上述反应所涉及的各物质中,属于非电解质的是_______ 。
(3)写出 的电子式
的电子式_______ ,其熔沸点比 低的原因是
低的原因是_______ 。
(4)写出实验室制备并检验 气体的离子方程式:
气体的离子方程式:_______ 、_______ 。
(5) 接触潮湿银器表面时,出现黑色斑点
接触潮湿银器表面时,出现黑色斑点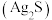 ,其化学反应如下:
,其化学反应如下:
_______ _______
_______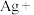 _______
_______ _______
_______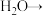 _______
_______ _______
_______
①配平上述反应_____ 。
②每消耗标准状况下 ,转移电子的数目为
,转移电子的数目为_______ 。
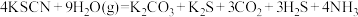 。完成下列填空:
。完成下列填空:(1)上述反应所涉及的各元素中,简单离子半径最大的是
 中含有的化学键类型是
中含有的化学键类型是(2)上述反应所涉及的各物质中,属于非电解质的是
(3)写出
 的电子式
的电子式 低的原因是
低的原因是(4)写出实验室制备并检验
 气体的离子方程式:
气体的离子方程式:(5)
 接触潮湿银器表面时,出现黑色斑点
接触潮湿银器表面时,出现黑色斑点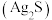 ,其化学反应如下:
,其化学反应如下:_______
 _______
_______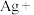 _______
_______ _______
_______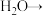 _______
_______ _______
_______
①配平上述反应
②每消耗标准状况下
 ,转移电子的数目为
,转移电子的数目为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】汽车是人们出行的重要交通工具,其中蕴含着大量的化学知识,回答下列问题:
(1)汽车中包含多种材料,制轮胎的丁苯橡胶属于_______ (填“天然”或“合成”)橡胶。
(2)汽车安全气囊启动时发生的反应有: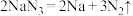 ,用单线桥表示该反应中的电子转移情况:
,用单线桥表示该反应中的电子转移情况:_______ 。
(3)在催化剂作用下,汽车尾气中的 与
与 能转化成两种无污染的气体,写出反应的化学方程式
能转化成两种无污染的气体,写出反应的化学方程式_______ 。
(4)汽车排放的 会加剧温室效应,实验室用
会加剧温室效应,实验室用 溶液吸收
溶液吸收 ,当
,当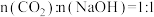 时,所得溶液呈碱性,原因是
时,所得溶液呈碱性,原因是_______ ,
_______ 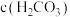 (填“>”或“<”)。
(填“>”或“<”)。
(5)使用燃料电池汽车可解决 的排放,写出
的排放,写出 溶液环境下甲醇燃料电池的负极电极反应式
溶液环境下甲醇燃料电池的负极电极反应式_______ 。
(1)汽车中包含多种材料,制轮胎的丁苯橡胶属于
(2)汽车安全气囊启动时发生的反应有:
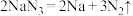 ,用单线桥表示该反应中的电子转移情况:
,用单线桥表示该反应中的电子转移情况:(3)在催化剂作用下,汽车尾气中的
 与
与 能转化成两种无污染的气体,写出反应的化学方程式
能转化成两种无污染的气体,写出反应的化学方程式(4)汽车排放的
 会加剧温室效应,实验室用
会加剧温室效应,实验室用 溶液吸收
溶液吸收 ,当
,当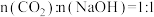 时,所得溶液呈碱性,原因是
时,所得溶液呈碱性,原因是
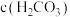 (填“>”或“<”)。
(填“>”或“<”)。(5)使用燃料电池汽车可解决
 的排放,写出
的排放,写出 溶液环境下甲醇燃料电池的负极电极反应式
溶液环境下甲醇燃料电池的负极电极反应式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】钛(Ti)因为具有神奇的性能越来越引起人们的关注。常温下,钛不和非金属、强酸反应;红热时,却可与常见的非金属单质反应。钛是航空、军工、电力等方面的必需原料。地壳中含钛矿石之一称金红石(TiO2)目前大规模生产钛的方法是:
第一步:金红石、碳粉混合,在高温条件下通入氯气制得TiCl4和一种可燃性气体。该反应的化学方程式是______ ,该反应的还原剂是______ 。
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)此反应的化学方程式是______ 。
(2)简述由上述所得产物中获取金属钛的步骤______ 。
第一步:金红石、碳粉混合,在高温条件下通入氯气制得TiCl4和一种可燃性气体。该反应的化学方程式是
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)此反应的化学方程式是
(2)简述由上述所得产物中获取金属钛的步骤
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】浓H2SO4具有①酸性;②强氧化性;③吸水性;④脱水性等性质,根据题意填空(填序号):
(1)将浓硫酸滴到滤纸上,滤纸变黑,是因为浓硫酸具有__________ ;
(2)浓H2SO4与木炭共热生成二氧化碳、二氧化硫和水,该反应体现了浓H2SO4的__________ 。
(3)盛有浓硫酸的烧杯敞口放置一段时间后,质量增加.是因为浓硫酸具有__________ 。
(1)将浓硫酸滴到滤纸上,滤纸变黑,是因为浓硫酸具有
(2)浓H2SO4与木炭共热生成二氧化碳、二氧化硫和水,该反应体现了浓H2SO4的
(3)盛有浓硫酸的烧杯敞口放置一段时间后,质量增加.是因为浓硫酸具有
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】学习化学应该明确“从生活中来,到生活中去”道理。在生产生活中,我们会遇到各种各样的化学反应。请按要求回答下列问题:
(1)写出下列反应的化学方程式。(注意反应条件并配平)
①镁带着火时,不能用CO2灭火剂来灭火的原因是_______
②氯气和石灰乳反应制漂白粉_______
③工业上用硫铁矿(FeS2)制SO2_______
④木炭与浓硫酸在加热下反应_______
(2)请你写出下列反应的离子方程式。
①工业上电解饱和食盐水制取氯气_______
②小苏打在医疗上用来治疗胃酸(盐酸)过多_______
(1)写出下列反应的化学方程式。(注意反应条件并配平)
①镁带着火时,不能用CO2灭火剂来灭火的原因是
②氯气和石灰乳反应制漂白粉
③工业上用硫铁矿(FeS2)制SO2
④木炭与浓硫酸在加热下反应
(2)请你写出下列反应的离子方程式。
①工业上电解饱和食盐水制取氯气
②小苏打在医疗上用来治疗胃酸(盐酸)过多
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】基础知识填空:
(1)酸雨的pH小于______ ;硅酸钠的水溶液俗称______ ;
(2)有以下物质:①Cu ②Al ③ C ④稀硫酸 ⑤浓硫酸 ⑥稀硝酸 ⑦浓硝酸。
加热条件下,①和④______ (填“能”或者“不能”)反应;
常温下,⑤和⑦可盛装在______ (选填①或②)容器中;
写出①与⑥反应的化学方程式______ ;
(3)实验室用MnO2与浓盐酸反应制氯气,在该反应中,氧化剂是______ ,如有1 mol Cl2生成,则被氧化的HCl的物质的量是______ mol,转移的电子数目为______ 。
(1)酸雨的pH小于
(2)有以下物质:①Cu ②Al ③ C ④稀硫酸 ⑤浓硫酸 ⑥稀硝酸 ⑦浓硝酸。
加热条件下,①和④
常温下,⑤和⑦可盛装在
写出①与⑥反应的化学方程式
(3)实验室用MnO2与浓盐酸反应制氯气,在该反应中,氧化剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)用地壳中某主要元素生产的多种产品在现代高科技中占重要位置,足见化学对现代物质文明的重要作用。例如:
①光导纤维的主要成分是____________ ;
②目前应用最多的太阳能电池的光电转化材料是_____ 。
(2)氮化硅Si3N4是一种高温结构材料,粉末状态的Si3N4可以由SiCl4的蒸气和NH3反应制取。粉末状Si3N4对空气和水都不稳定。但将粉末状的Si3N4和适量氧化镁在230×1.01×105Pa和185℃的密闭容器中热处理,可以制得结构十分紧密、对空气和水都相当稳定的固体材料,同时还得到对水不稳定的Mg3N2。
①写出由SiCl4和NH3反应制取Si3N4的化学反应方程式:________________ ;
②在Si3N4和适量氧化镁在230×1.01×105Pa和185℃的密闭容器中热处理的过程中,发生反应,反应过程中有Mg3N2生成。其化学方程式为:_________________ ;
③氮化硅Si3N4是一种高温结构材料,其优点是(只要求写出二种)。
___________________ 、_____________________ 。
①光导纤维的主要成分是
②目前应用最多的太阳能电池的光电转化材料是
(2)氮化硅Si3N4是一种高温结构材料,粉末状态的Si3N4可以由SiCl4的蒸气和NH3反应制取。粉末状Si3N4对空气和水都不稳定。但将粉末状的Si3N4和适量氧化镁在230×1.01×105Pa和185℃的密闭容器中热处理,可以制得结构十分紧密、对空气和水都相当稳定的固体材料,同时还得到对水不稳定的Mg3N2。
①写出由SiCl4和NH3反应制取Si3N4的化学反应方程式:
②在Si3N4和适量氧化镁在230×1.01×105Pa和185℃的密闭容器中热处理的过程中,发生反应,反应过程中有Mg3N2生成。其化学方程式为:
③氮化硅Si3N4是一种高温结构材料,其优点是(只要求写出二种)。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】材料是人类赖以生存和发展的重要物质基础。
(1)试管、烧杯和烧瓶等化学仪器的主要材质是_________ 。
A.玻璃 B.陶瓷
(2)钢铁是目前用量最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为_________ ;
A.O2+2H2O+4e-=4OH- B.Fe-2e-=Fe2+
(3)太阳能电池现已被广泛使用。生产太阳能电池主要用到的是_________ (填字母)。
A.晶体硅 B.石墨 C.金属锂
(4)钢铁是日常生活中使用最为广泛的金属,在潮湿的环境中易发生_________ (填“化学”或“电化学”)腐蚀,在铁制闸门上常嵌入_________ (填“铜块”、“锌块”)来保护闸门防止腐蚀。
(1)试管、烧杯和烧瓶等化学仪器的主要材质是
A.玻璃 B.陶瓷
(2)钢铁是目前用量最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为
A.O2+2H2O+4e-=4OH- B.Fe-2e-=Fe2+
(3)太阳能电池现已被广泛使用。生产太阳能电池主要用到的是
A.晶体硅 B.石墨 C.金属锂
(4)钢铁是日常生活中使用最为广泛的金属,在潮湿的环境中易发生
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】中国高铁对实现“一带一路”的倡议有重要的作用。
(1)高铁上的信息传输系统使用了光导纤维,其主要成分是____ ;乘务员使用的无线通话机的芯片材料是____ 。
(2) 是一种酸性氧化物,能与强碱溶液反应。例如,
是一种酸性氧化物,能与强碱溶液反应。例如, 与NaOH反应可生成
与NaOH反应可生成 。
。 的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。请写出相关反应的化学方程式
的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。请写出相关反应的化学方程式___ 。
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式为_____ 。
(4)氮化硅( )可由石英与焦炭在高温的氮气流中通过以下反应制备:
)可由石英与焦炭在高温的氮气流中通过以下反应制备: ,以及以上反应中的氧化剂
,以及以上反应中的氧化剂____ ,还原剂___ 。
(1)高铁上的信息传输系统使用了光导纤维,其主要成分是
(2)
 是一种酸性氧化物,能与强碱溶液反应。例如,
是一种酸性氧化物,能与强碱溶液反应。例如, 与NaOH反应可生成
与NaOH反应可生成 。
。 的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。请写出相关反应的化学方程式
的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。请写出相关反应的化学方程式(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式为
(4)氮化硅(
 )可由石英与焦炭在高温的氮气流中通过以下反应制备:
)可由石英与焦炭在高温的氮气流中通过以下反应制备: ,以及以上反应中的氧化剂
,以及以上反应中的氧化剂
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】写出下列有关反应的化学方程式:
(1)高温条件下铝粉与氧化铁反应__________________________ ;
(2)乙烯使溴的四氯化碳溶液褪色____________________________ ;
(3)将金属钠放入无水乙醇中_______________________________ 。
(1)高温条件下铝粉与氧化铁反应
(2)乙烯使溴的四氯化碳溶液褪色
(3)将金属钠放入无水乙醇中
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)地球外层空间存在微量臭氧(O3)分子和氧原子,该臭氧层能吸收阻挡太阳强烈有害的紫外线辐射,可是人为的大气污染物会破坏臭氧层,如超音速飞机排放物中的氮氧化物(NO和NO2),它们与O3、O发生如下反应:O3+NO=NO2+O2,NO2+O=NO+O2。这两个反应反复循环,其总反应式为______________ ,由此可见氮氧化物在破坏臭氧层过程中起了________ 的作用。
(2)铝粉是铝热焊剂的主要成分之一。在用99.9%纯度的铝锭制得的铝粉中,常含少量的三氧化二铝和二氧化硅。用气体容量法可以测定铝粉中金属铝(又称活性铝)的含量,其方法是:用盐酸或氢氧化钠溶液与样品作用,通过产生的氢气的体积计算样品中金属铝的含量。在盐酸和氢氧化钠溶液这两种试剂中,选用__________ 较好,原因是________ 。
(3)根据你选用的试剂,写出测定过程的化学方程式_________________ 。
(2)铝粉是铝热焊剂的主要成分之一。在用99.9%纯度的铝锭制得的铝粉中,常含少量的三氧化二铝和二氧化硅。用气体容量法可以测定铝粉中金属铝(又称活性铝)的含量,其方法是:用盐酸或氢氧化钠溶液与样品作用,通过产生的氢气的体积计算样品中金属铝的含量。在盐酸和氢氧化钠溶液这两种试剂中,选用
(3)根据你选用的试剂,写出测定过程的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】已知铝是一种能够和强碱溶液反应生成氢气的一种特殊金属,其反应的化学方程式为. 2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑ ,现向400mLNaOH溶液中投入10.8gAl,二者恰好完全反应,计算:
(1)Al的物质的量为_________ mol。
(2)参加反应的NaOH的物质的量为_______ mol;溶液的物质的量浓度_______ mol•L-1。
(3)生成的H2在标准状况下的体积为______ L;反应中转移的电子数为______ 。
(1)Al的物质的量为
(2)参加反应的NaOH的物质的量为
(3)生成的H2在标准状况下的体积为
您最近一年使用:0次



