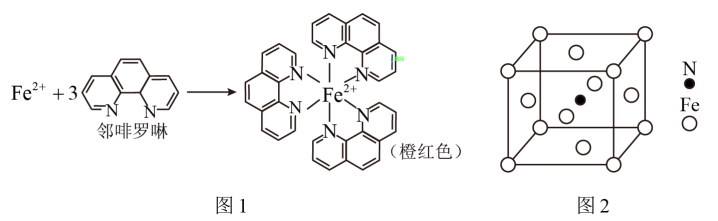
配位化合物在生产生活中有重要应用,请根据要求回答下列问题:
(1)光谱证实单质铝与强碱性溶液反应有[AlOH)4]-生成,则[AlOH)4]-中存在___________ (填序号)。
a.共价键 b.非极性键 c.配位键 d.σ键 e.π键
(2)Co(NH3)5BrSO4可形成两种钴的配合物。已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物的溶液中加BaCl2溶液时,则无明显现象。则第一种配合物的结构式可表示为___________ ,第二种配合物的结构式可表示为___________ 。若在第二种配合物的溶液中滴加AgNO3溶液,则产生的现象是___________ 。(提示:TiCl(H2O)5Cl2这种配合物的结构可表示为[TiCl(H2O)5]Cl2.)
(3)关于[Ti(NH3)5Cl]Cl2的说法中错误的是___________(填字母)。
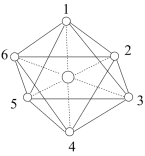
(4)已知CO(NH3)6]3+的立体结构如图,其中1~6处的小圆圈表示NH3分子,且各相邻的NH3分子间的距离相等(图中虚线长度相等)。Co3+位于八面体的中心,若其中两个NH3被Cl取代,所形成的[Co(NH3)4Cl2]+的结构的数目为___________ 。
(5)向盛有硫酸铜水溶液的试管中加氨水。先形成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液。在这个过程中先生成蓝色沉淀,后沉淀溶解,用离子方程式解释原因:___________ 、___________ 。
(1)光谱证实单质铝与强碱性溶液反应有[AlOH)4]-生成,则[AlOH)4]-中存在
a.共价键 b.非极性键 c.配位键 d.σ键 e.π键
(2)Co(NH3)5BrSO4可形成两种钴的配合物。已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀,在第二种配合物的溶液中加BaCl2溶液时,则无明显现象。则第一种配合物的结构式可表示为
(3)关于[Ti(NH3)5Cl]Cl2的说法中错误的是___________(填字母)。
| A.1mol[Ti(NH3)5Cl]Cl2含有σ键的数目为15NA |
| B.中心原子的化合价为+3价 |
| C.中心原子的配位数是6 |
| D.含1mol[Ti(NH3)5Cl]Cl2的水溶液中加入足量AgNO3溶液,产生3mol白色沉淀 |

(5)向盛有硫酸铜水溶液的试管中加氨水。先形成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液。在这个过程中先生成蓝色沉淀,后沉淀溶解,用离子方程式解释原因:
更新时间:2023/03/26 15:46:16
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】某课外兴趣小组进行热致变色实验时,加热0.1mol/L 溶液,未观察到溶液颜色的变化;但在0.1mol/L
溶液,未观察到溶液颜色的变化;但在0.1mol/L  ,溶液中加入适量6mol/L HCl或适量
,溶液中加入适量6mol/L HCl或适量 溶液,加热后溶液颜色逐渐变为蓝色,写出相关反应方程式并注明主要物质的颜色。
溶液,加热后溶液颜色逐渐变为蓝色,写出相关反应方程式并注明主要物质的颜色。___________
 溶液,未观察到溶液颜色的变化;但在0.1mol/L
溶液,未观察到溶液颜色的变化;但在0.1mol/L  ,溶液中加入适量6mol/L HCl或适量
,溶液中加入适量6mol/L HCl或适量 溶液,加热后溶液颜色逐渐变为蓝色,写出相关反应方程式并注明主要物质的颜色。
溶液,加热后溶液颜色逐渐变为蓝色,写出相关反应方程式并注明主要物质的颜色。
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)NaClO溶液在碱性条件下将CN-氧化成无毒的碳酸根离子和N2,该反应离子方程式________________________________ 。
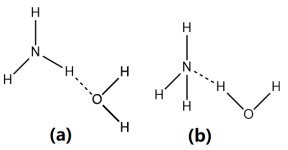
(2)NH3·H2O的电离方程式为NH3·H2O NH4++OH-,试判断溶于水后,形成的合理结构是
NH4++OH-,试判断溶于水后,形成的合理结构是________ 。(填图中的字母)
(3)把CoCl2溶于水后加氨水直到先生成的Co(OH)2沉淀又溶解后,再加氨水,使生成[Co(NH3)6]2+,此时向溶液中通入空气,得到的产物中有一种其组成可用CoCl3·5NH3表示,Co的配位数是6。把分离出的CoCl3·5NH3溶于水后立即加硝酸银溶液,则析出AgCl沉淀。经测定,每1molCoCl3·5NH3只生成2molAgCl,CoCl3·5NH3中Co化合价为__________ ,请写出表示此配合物结构的化学式:______________ 。
(4)H2O、H2S、H2Se熔沸点由低到高的顺序:_________________ 。
(5)HF比HCl热稳定性____ (填“强”或“弱”),原因是:________ 。
(2)NH3·H2O的电离方程式为NH3·H2O
 NH4++OH-,试判断溶于水后,形成的合理结构是
NH4++OH-,试判断溶于水后,形成的合理结构是
(3)把CoCl2溶于水后加氨水直到先生成的Co(OH)2沉淀又溶解后,再加氨水,使生成[Co(NH3)6]2+,此时向溶液中通入空气,得到的产物中有一种其组成可用CoCl3·5NH3表示,Co的配位数是6。把分离出的CoCl3·5NH3溶于水后立即加硝酸银溶液,则析出AgCl沉淀。经测定,每1molCoCl3·5NH3只生成2molAgCl,CoCl3·5NH3中Co化合价为
(4)H2O、H2S、H2Se熔沸点由低到高的顺序:
(5)HF比HCl热稳定性
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据所学物质结构知识,回答下列问题:
(1)氮元素是植物生长所需的元素,常见氮肥有铵盐(NH4+)、尿素 (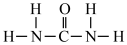 )等,NH4+中H-N-H键角
)等,NH4+中H-N-H键角_______ (填“>”“<”或“=”)。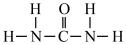 中N-C-N键角。
中N-C-N键角。
(2)硫元素和人类的生存与发展联系密切,在战国时期,我国的炼丹家们就开始了对硫单质及含硫化合物的研究应用。硫单质有多种同素异形体,其中一种单质分子(S8)的结构为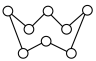 ,其熔点和沸点要比二氧化硫的高很多,主要原因为
,其熔点和沸点要比二氧化硫的高很多,主要原因为___________ 。气态三氧化硫以单分子形式存在,其分子的立体构型为____ 形,实验测得三种氧化物的熔沸点如下,推测固态三氧化硫的分子式为____________ 。
(3)在气体分析中,常用CuCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:2CuCl+2CO+2H2O=Cu2Cl2·2CO·2H2O;Cu2Cl2·2CO·2H2O是一种配合物,其结构如图所示:
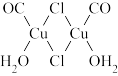
①H2O中氧原子的杂化方式为_____________ ;
②该配合物中,CO作配体时配位原子是C而不是O的原因是______________ 。
(1)氮元素是植物生长所需的元素,常见氮肥有铵盐(NH4+)、尿素 (
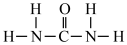 )等,NH4+中H-N-H键角
)等,NH4+中H-N-H键角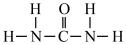 中N-C-N键角。
中N-C-N键角。(2)硫元素和人类的生存与发展联系密切,在战国时期,我国的炼丹家们就开始了对硫单质及含硫化合物的研究应用。硫单质有多种同素异形体,其中一种单质分子(S8)的结构为
 ,其熔点和沸点要比二氧化硫的高很多,主要原因为
,其熔点和沸点要比二氧化硫的高很多,主要原因为| P4O10 | 三氧化硫 | Cl2O7 | |
| 熔点 | 613K | 289K | 182K |
| 沸点 | 633K | 317K | 355K |
(3)在气体分析中,常用CuCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下:2CuCl+2CO+2H2O=Cu2Cl2·2CO·2H2O;Cu2Cl2·2CO·2H2O是一种配合物,其结构如图所示:

①H2O中氧原子的杂化方式为
②该配合物中,CO作配体时配位原子是C而不是O的原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)往硫酸铜溶液中加入氨水,先形成蓝色沉淀,用离子方程式表示为_______ ;继续加氨水,得到深蓝色透明溶液,用离子方程式表示为_______ ;再加入乙醇,得到的深蓝色晶体为_______ ;
(2)[Cu(H2O)4]2+中存在的化学键类型有_______ (填“离子键”或“共价键”或“配位键”)。[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为_______ 。其结构可用示意图表示为_______ 。
(1)往硫酸铜溶液中加入氨水,先形成蓝色沉淀,用离子方程式表示为
(2)[Cu(H2O)4]2+中存在的化学键类型有
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1) 可发生水解反应,机理如下:
可发生水解反应,机理如下:
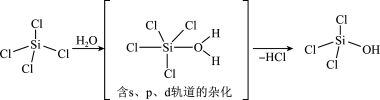
已知中间体 的中心原子
的中心原子 采取的杂化类型为
采取的杂化类型为 ,则该
,则该 原子的价层电子对数为
原子的价层电子对数为_______ ,下列关于该中间体 模型的空间结构推断合理的是
模型的空间结构推断合理的是_______ (填标号)。
a.正四面体 b.三角双锥 c.正八面体
试解释 不易水解的原因:
不易水解的原因:_______ 。
(2) 稀溶液中存在
稀溶液中存在 。已知
。已知 轨道也可以参与杂化,则
轨道也可以参与杂化,则 中
中 的杂化方式为_______(填标号)。
的杂化方式为_______(填标号)。
(1)
 可发生水解反应,机理如下:
可发生水解反应,机理如下:
已知中间体
 的中心原子
的中心原子 采取的杂化类型为
采取的杂化类型为 ,则该
,则该 原子的价层电子对数为
原子的价层电子对数为 模型的空间结构推断合理的是
模型的空间结构推断合理的是a.正四面体 b.三角双锥 c.正八面体
试解释
 不易水解的原因:
不易水解的原因:(2)
 稀溶液中存在
稀溶液中存在 。已知
。已知 轨道也可以参与杂化,则
轨道也可以参与杂化,则 中
中 的杂化方式为_______(填标号)。
的杂化方式为_______(填标号)。A. | B. | C. | D. |
您最近半年使用:0次