(1)NaClO溶液在碱性条件下将CN-氧化成无毒的碳酸根离子和N2,该反应离子方程式________________________________ 。
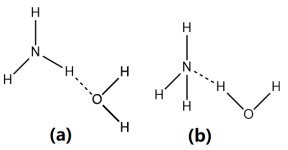
(2)NH3·H2O的电离方程式为NH3·H2O NH4++OH-,试判断溶于水后,形成的合理结构是
NH4++OH-,试判断溶于水后,形成的合理结构是________ 。(填图中的字母)
(3)把CoCl2溶于水后加氨水直到先生成的Co(OH)2沉淀又溶解后,再加氨水,使生成[Co(NH3)6]2+,此时向溶液中通入空气,得到的产物中有一种其组成可用CoCl3·5NH3表示,Co的配位数是6。把分离出的CoCl3·5NH3溶于水后立即加硝酸银溶液,则析出AgCl沉淀。经测定,每1molCoCl3·5NH3只生成2molAgCl,CoCl3·5NH3中Co化合价为__________ ,请写出表示此配合物结构的化学式:______________ 。
(4)H2O、H2S、H2Se熔沸点由低到高的顺序:_________________ 。
(5)HF比HCl热稳定性____ (填“强”或“弱”),原因是:________ 。
(2)NH3·H2O的电离方程式为NH3·H2O
 NH4++OH-,试判断溶于水后,形成的合理结构是
NH4++OH-,试判断溶于水后,形成的合理结构是
(3)把CoCl2溶于水后加氨水直到先生成的Co(OH)2沉淀又溶解后,再加氨水,使生成[Co(NH3)6]2+,此时向溶液中通入空气,得到的产物中有一种其组成可用CoCl3·5NH3表示,Co的配位数是6。把分离出的CoCl3·5NH3溶于水后立即加硝酸银溶液,则析出AgCl沉淀。经测定,每1molCoCl3·5NH3只生成2molAgCl,CoCl3·5NH3中Co化合价为
(4)H2O、H2S、H2Se熔沸点由低到高的顺序:
(5)HF比HCl热稳定性
更新时间:2018-07-24 09:35:38
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】写出下列反应的离子反应方程式
①锌与稀硫酸反应_______ ;
②少量二氧化碳通入澄清石灰水中_______ ;
③硫酸铜溶液和氢氧化钡溶液混合__________ ;
④氢氧化钠溶液与稀硫酸_______ ;
⑤硫酸氢钠溶液与氢氧化钡溶液混合至中性_______ 。
①锌与稀硫酸反应
②少量二氧化碳通入澄清石灰水中
③硫酸铜溶液和氢氧化钡溶液混合
④氢氧化钠溶液与稀硫酸
⑤硫酸氢钠溶液与氢氧化钡溶液混合至中性
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求填空:
(1)向沸腾的蒸馏水中滴加饱和FeCl3溶液可制取Fe(OH)3胶体,用离子方程式表示该方法的原理:______ ;
(2)硫酸铜溶液与氢氧化钡溶液反应的离子方程式为:______ ;
(3)Ca(OH)2溶液与少量NaHCO3溶液混合:_______ ;
(4)+6价铬(Cr)的化合物毒性较大,酸性条件下,常用NaHSO3将废液中的Cr2O 还原为Cr3+,该反应的离子方程式为:
还原为Cr3+,该反应的离子方程式为:______ ;
(5)在酸性条件下,往H2O2与I-的反应液中加入淀粉,淀粉变蓝,用离子方程式表示该方法的原理:_______ 。
(1)向沸腾的蒸馏水中滴加饱和FeCl3溶液可制取Fe(OH)3胶体,用离子方程式表示该方法的原理:
(2)硫酸铜溶液与氢氧化钡溶液反应的离子方程式为:
(3)Ca(OH)2溶液与少量NaHCO3溶液混合:
(4)+6价铬(Cr)的化合物毒性较大,酸性条件下,常用NaHSO3将废液中的Cr2O
 还原为Cr3+,该反应的离子方程式为:
还原为Cr3+,该反应的离子方程式为:(5)在酸性条件下,往H2O2与I-的反应液中加入淀粉,淀粉变蓝,用离子方程式表示该方法的原理:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求填空:
I.现有7种物质:① Na、② FeCl3溶液、③ CH3COOH、④ 熔融的KNO3、⑤ CO2、⑥ Fe(OH)3胶体、⑦ NH4Cl 固体。
(1)能导电的电解质有___________ (填序号)。
(2)属于盐的物质有___________ (填序号)。
(3)区分Fe(OH)3胶体和 FeCl3溶液的常用物理方法是___________ 。
(4)FeCl3在溶液中的电离方程式是___________ 。
II.依据信息书写下列反应的离子方程式。
(5)SO2是一种酸性氧化物,可用过量 NaOH溶液吸收含 SO2的尾气,该反应的离子方程式是___________
(6)市场上出售的抗酸药复方氢氧化铝片主要用于缓解人体胃酸(主要成分是盐酸)过多,相关反应的离子方程式为___________ 。
III.碳酸钠在轻工、建材、纺织、国防、医药等工业中有重要的应用。工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO 等杂质,提纯工艺线路如下:
等杂质,提纯工艺线路如下:

碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:

请回答下列问题:
(7)试剂A是___________ ,“母液”中除了含有Na+、CO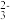 、OH-外,还含有
、OH-外,还含有___________ 等离子,过滤要“趁热”的目的是___________ 。
(8)检验试剂级Na2CO3中Cl-和SO 是否除尽,选用的试剂及加入的先后次序是___________(填字母)。
是否除尽,选用的试剂及加入的先后次序是___________(填字母)。
I.现有7种物质:① Na、② FeCl3溶液、③ CH3COOH、④ 熔融的KNO3、⑤ CO2、⑥ Fe(OH)3胶体、⑦ NH4Cl 固体。
(1)能导电的电解质有
(2)属于盐的物质有
(3)区分Fe(OH)3胶体和 FeCl3溶液的常用物理方法是
(4)FeCl3在溶液中的电离方程式是
II.依据信息书写下列反应的离子方程式。
(5)SO2是一种酸性氧化物,可用过量 NaOH溶液吸收含 SO2的尾气,该反应的离子方程式是
(6)市场上出售的抗酸药复方氢氧化铝片主要用于缓解人体胃酸(主要成分是盐酸)过多,相关反应的离子方程式为
III.碳酸钠在轻工、建材、纺织、国防、医药等工业中有重要的应用。工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO
 等杂质,提纯工艺线路如下:
等杂质,提纯工艺线路如下:
碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:

请回答下列问题:
(7)试剂A是
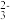 、OH-外,还含有
、OH-外,还含有(8)检验试剂级Na2CO3中Cl-和SO
 是否除尽,选用的试剂及加入的先后次序是___________(填字母)。
是否除尽,选用的试剂及加入的先后次序是___________(填字母)。| A.HCl、BaCl2、AgNO3 | B.AgNO3、HNO3、Ba(NO3)2 |
| C.HNO3、Ba(NO3)2、AgNO3 | D.AgNO3、HCl、BaCl2 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】配合物在许多尖端领域如激光材料、超导材料、抗癌药物的研究、催化剂的研制等方面发挥着越来越大的作用。
(1)三氯化钛( )用于催化聚丙烯的生产等。在浓的
)用于催化聚丙烯的生产等。在浓的 溶液中加入乙醚,并通入
溶液中加入乙醚,并通入 至饱和,可得到配位数为6、组成为
至饱和,可得到配位数为6、组成为 的绿色晶体,该晶体中两配位体的物质的量之比为1∶5,则该配离子的化学式为
的绿色晶体,该晶体中两配位体的物质的量之比为1∶5,则该配离子的化学式为___________ 。
(2)研究表明,对于中心离子为 等阳离子的配合物,配位体给出电子的能力越强,则配位体与中心离子形成的配位键就越强,配合物也就越稳定。预测
等阳离子的配合物,配位体给出电子的能力越强,则配位体与中心离子形成的配位键就越强,配合物也就越稳定。预测 与
与 的稳定性强弱:
的稳定性强弱: 与
与 更
更___________ (填“稳定”或“不稳定”)。
(1)三氯化钛(
 )用于催化聚丙烯的生产等。在浓的
)用于催化聚丙烯的生产等。在浓的 溶液中加入乙醚,并通入
溶液中加入乙醚,并通入 至饱和,可得到配位数为6、组成为
至饱和,可得到配位数为6、组成为 的绿色晶体,该晶体中两配位体的物质的量之比为1∶5,则该配离子的化学式为
的绿色晶体,该晶体中两配位体的物质的量之比为1∶5,则该配离子的化学式为(2)研究表明,对于中心离子为
 等阳离子的配合物,配位体给出电子的能力越强,则配位体与中心离子形成的配位键就越强,配合物也就越稳定。预测
等阳离子的配合物,配位体给出电子的能力越强,则配位体与中心离子形成的配位键就越强,配合物也就越稳定。预测 与
与 的稳定性强弱:
的稳定性强弱: 与
与 更
更
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】第四周期的Fe、Co、Ni、Cu、Zn等许多金属能形成配合物。
(1)NH3是一种很好的配体,氨气分子是____ (填“极性”或“非极性”)分子,NH3的沸点____ (填“高于”“等于”或“低于”)AsH3。
(2)科学家通过X-射线测得胆矾的结构示意图可简单表示如图所示:__________ 。
(3)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4·SO4·H2O晶体。在Cu(NH3)4SO4·H2O晶体中,[Cu(NH3)4]2+为平面正方形结构,则呈正四面体结构的原子团是____ ,该原子团中心原子的杂化轨道类型是____ 。
(4)金属镍粉在CO气流中轻微加热,生成无色、有挥发性的液态Ni(CO)4,其分子呈正四面体构型。Ni(CO)4易溶于____ (填字母)。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(1)NH3是一种很好的配体,氨气分子是
(2)科学家通过X-射线测得胆矾的结构示意图可简单表示如图所示:
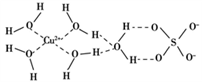
(3)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4·SO4·H2O晶体。在Cu(NH3)4SO4·H2O晶体中,[Cu(NH3)4]2+为平面正方形结构,则呈正四面体结构的原子团是
(4)金属镍粉在CO气流中轻微加热,生成无色、有挥发性的液态Ni(CO)4,其分子呈正四面体构型。Ni(CO)4易溶于
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如图,其中配位键和氢键均采用虚线表示。________________________ 。
(2)Cu2+还能与NH3、Cl-等形成配位数为4的配合物。
①[Cu(NH3)4]2+中存在的化学键类型有__________ (填序号)。
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
②已知[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为_______________ 。
(3)实验证明,用蒸汽密度法测得的H2O的相对分子质量比用化学式计算出来的相对分子质量要大,其原因是_____________________________ 。
(4)向硫酸铜水溶液中逐滴加入氨水直至过量,反应的离子方程式为______________________ 。

(2)Cu2+还能与NH3、Cl-等形成配位数为4的配合物。
①[Cu(NH3)4]2+中存在的化学键类型有
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
②已知[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为
(3)实验证明,用蒸汽密度法测得的H2O的相对分子质量比用化学式计算出来的相对分子质量要大,其原因是
(4)向硫酸铜水溶液中逐滴加入氨水直至过量,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入乙醇,溶液中将析出深蓝色的晶体。
(1)写出该深蓝色晶体的化学式:________________________
(2)写出整个反应过程中的离子方程式:_________________ 、________________ 。
(3)硫酸铜水溶液之所以呈天蓝色是由于铜离子和水分子之间通过配位键形成了水合铜离子,请画出该离子中配位键的结合:__________________ 。
(4)乙醇分子的极性_____ (大于、小于、等于)水分子的极性;乙醇能够和水互溶的原因是___________ 。
(1)写出该深蓝色晶体的化学式:
(2)写出整个反应过程中的离子方程式:
(3)硫酸铜水溶液之所以呈天蓝色是由于铜离子和水分子之间通过配位键形成了水合铜离子,请画出该离子中配位键的结合:
(4)乙醇分子的极性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】地球上的物质不断变化,数10亿年来大气的成分也发生了很大的变化。下表是原始大气和目前空气的主要成分:
用上表所涉及的分子填写下列空白。
(1)含有10个电子的分子有(填化学式,下同)___________ ;
(2)由极性键构成的非极性分子有___________ ;
(3)与 可直接形成配位键的分子有
可直接形成配位键的分子有___________ ;
(4)分子中不含孤电子对的分子有___________ ,它的立体构型为___________ ;
(5)极易溶于水、且水溶液呈碱性的物质的分子是___________ ,它极易溶于水的原因是___________ 。
| 目前空气的成分 |  、 、 、 、 、水蒸气及稀有气体(如He、Ne等) 、水蒸气及稀有气体(如He、Ne等) |
| 原始大气的主要成分 |  、 、 、CO、 、CO、 等 等 |
用上表所涉及的分子填写下列空白。
(1)含有10个电子的分子有(填化学式,下同)
(2)由极性键构成的非极性分子有
(3)与
 可直接形成配位键的分子有
可直接形成配位键的分子有(4)分子中不含孤电子对的分子有
(5)极易溶于水、且水溶液呈碱性的物质的分子是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】工业上常利用铜萃取剂,使溶液中的Cu2+富集进入有机相,再经过进一步的反萃取实现金属铜的沉积、再生,铜萃取剂富集Cu2+的原理如下:
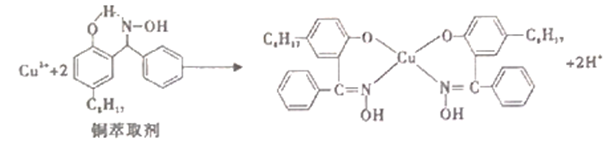
(1)基态铜原子所失去的第一个电子所占据的能层符号是______ , 价铜离 子的简化电子排布式为_________ 。
(2)铜萃取剂中所含 元素的电负性由大到小顺序为______ ,N原子以_____ 杂化轨道与O原子形成σ键。
(3)铜萃取剂与 Cu2+形成的配合物在水相的溶解度______ 有机相的溶解度(填“>”、“<”、“=”),该配合物晶体类型为_____ 。
(4)某学生用硫酸铜溶液与氨水做了一组实 验:CuSO4溶液 蓝色沉淀
蓝色沉淀 沉淀溶解。写出蓝色沉淀溶于氨水的离子方程式
沉淀溶解。写出蓝色沉淀溶于氨水的离子方程式_________ ;沉淀溶解后溶液中的阳离子内存在的化学键类型有________ 。
(5)铜的一种氯化物的晶胞如图所示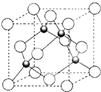 ,该氯化物的化学式
,该氯化物的化学式_____ ,Cu 和Cl之间最短距离为460.0pm,则晶体密度为______ g/cm3。(列式表示)

(1)基态铜原子所失去的第一个电子所占据的能层符号是
(2)铜萃取剂中所含 元素的电负性由大到小顺序为
(3)铜萃取剂与 Cu2+形成的配合物在水相的溶解度
(4)某学生用硫酸铜溶液与氨水做了一组实 验:CuSO4溶液
 蓝色沉淀
蓝色沉淀 沉淀溶解。写出蓝色沉淀溶于氨水的离子方程式
沉淀溶解。写出蓝色沉淀溶于氨水的离子方程式(5)铜的一种氯化物的晶胞如图所示
 ,该氯化物的化学式
,该氯化物的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入乙醇,溶液中将析出深蓝色的晶体。
(1)写出该深蓝色晶体的化学式:________________________
(2)写出整个反应过程中的离子方程式:_________________ 、________________ 。
(3)硫酸铜水溶液之所以呈天蓝色是由于铜离子和水分子之间通过配位键形成了水合铜离子,请画出该离子中配位键的结合:__________________ 。
(4)乙醇分子的极性_____ (大于、小于、等于)水分子的极性;乙醇能够和水互溶的原因是___________ 。
(1)写出该深蓝色晶体的化学式:
(2)写出整个反应过程中的离子方程式:
(3)硫酸铜水溶液之所以呈天蓝色是由于铜离子和水分子之间通过配位键形成了水合铜离子,请画出该离子中配位键的结合:
(4)乙醇分子的极性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】研究物质的结构,用来探寻物质的性质,是我们学习化学的重要方法。回答下列问题:
(1)Fe、Ru、Os在元素周期表中处于同一列,人们已经发现和应用了Ru、Os的四氧化物,Ru、Os体现+8价。量子化学理论预测铁也存在四氧化物,但最终人们发现铁的化合价不是+8而是+6.你预测铁的“四氧化物”分子的结构式为___________ 。
(2)氰酸铵( )是一种铵盐,除氢原子外,各原子均满足8电子稳定结构,且无双键存在,请写出氰酸铵的电子式
)是一种铵盐,除氢原子外,各原子均满足8电子稳定结构,且无双键存在,请写出氰酸铵的电子式___________ 。
(3)抗坏血酸(结构简式如图所示)易溶于水的主要原因___________ 。

(4)氢键的本质是缺电子的氢原子和富电子的原子或原子团之间的一种弱的电性作用。近年来,人们发现了双氢键,双氢键是指带正电的H原子与带负电的H原子之间的一种弱电性相互作用。下列不可能形成双氢键的是___________ 。(已知电负性:H-2.1 Be-1.5 B -2.0 N-3.0 O-3.5 Al-1.5 Si-1.8)
a.Be—H...H—O b.O—H...H—N c.B—H...H—N d.Si—H...H—Al
(5)冰晶石( )主要用作电解氧化铝的助熔剂,也用作研磨产品的耐磨添加剂。
)主要用作电解氧化铝的助熔剂,也用作研磨产品的耐磨添加剂。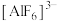 中Al原子处于6个F原子形成的正八面体中心,则中心原子周围的成键电子总数是
中Al原子处于6个F原子形成的正八面体中心,则中心原子周围的成键电子总数是___________ 个。
(1)Fe、Ru、Os在元素周期表中处于同一列,人们已经发现和应用了Ru、Os的四氧化物,Ru、Os体现+8价。量子化学理论预测铁也存在四氧化物,但最终人们发现铁的化合价不是+8而是+6.你预测铁的“四氧化物”分子的结构式为
(2)氰酸铵(
 )是一种铵盐,除氢原子外,各原子均满足8电子稳定结构,且无双键存在,请写出氰酸铵的电子式
)是一种铵盐,除氢原子外,各原子均满足8电子稳定结构,且无双键存在,请写出氰酸铵的电子式(3)抗坏血酸(结构简式如图所示)易溶于水的主要原因

(4)氢键的本质是缺电子的氢原子和富电子的原子或原子团之间的一种弱的电性作用。近年来,人们发现了双氢键,双氢键是指带正电的H原子与带负电的H原子之间的一种弱电性相互作用。下列不可能形成双氢键的是
a.Be—H...H—O b.O—H...H—N c.B—H...H—N d.Si—H...H—Al
(5)冰晶石(
 )主要用作电解氧化铝的助熔剂,也用作研磨产品的耐磨添加剂。
)主要用作电解氧化铝的助熔剂,也用作研磨产品的耐磨添加剂。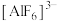 中Al原子处于6个F原子形成的正八面体中心,则中心原子周围的成键电子总数是
中Al原子处于6个F原子形成的正八面体中心,则中心原子周围的成键电子总数是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下列反应曾用于检测司机是否酒后驾驶:2Cr2O +3CH3CH2OH+16H++13H2O―→4[Cr(H2O)6]3++3CH3COOH
+3CH3CH2OH+16H++13H2O―→4[Cr(H2O)6]3++3CH3COOH
(1)CH3COOH中C原子轨道杂化类型为_______________________________ ;
1 mol CH3COOH分子含有σ键的数目为________ 。
(2)与H2O互为等电子体的一种阳离子为________ (填化学式);H2O与CH3CH2OH可以任意比例互溶,除因为它们都是极性分子外,还因为_________________________________________ 。
 +3CH3CH2OH+16H++13H2O―→4[Cr(H2O)6]3++3CH3COOH
+3CH3CH2OH+16H++13H2O―→4[Cr(H2O)6]3++3CH3COOH(1)CH3COOH中C原子轨道杂化类型为
1 mol CH3COOH分子含有σ键的数目为
(2)与H2O互为等电子体的一种阳离子为
您最近一年使用:0次



