“天问一号”着陆火星,“嫦娥五号”采回月壤,探索宇宙离不开化学。镍铼合金是制造喷气发动机的燃烧室、涡轮叶片及排气喷嘴的重要材料。75号元素铼Re,熔点仅次于钨,是稀有金属之一,地壳中铼的含量极低,多伴生于铜、锌、铅等矿物中。
(1)镍原子价电子表示式为___________ ,在元素周期表中,铼与锰在同族,铼在元素周期表中的位置是___________ 。
(2)铼易形成高配位数的化合物如Re2(CO)10,该配合物中___________ (填元素符号)提供孤对电子与铼成键,原因是___________ ,1mol Re2(CO)10中有___________ mol配位键。
(3)锌在潮湿的空气中极易生成一层紧密的碱式碳酸锌[ZnCO3·3Zn(OH)2]薄膜,使其具有抗腐蚀性。碱式碳酸锌中非金属元素的电负性由大到小的顺序为___________ ,CO 的空间构型为
的空间构型为___________ (用文字描述)。与CO 互为等电子体的分子是
互为等电子体的分子是___________ (写一种即可)。
(4)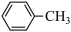 分子中碳原子的杂化类型为
分子中碳原子的杂化类型为___________ ,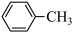 比
比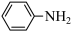 的熔点沸点
的熔点沸点___________ (填“高”或“低”),原因是___________ 。
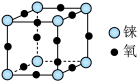
(5)三氧化铼晶胞如图所示,摩尔质量为Mg/mol,晶胞密度为bg/cm3,铼原子填在___________ 个氧原子围成的___________ (填“四面体”“立方体”或“八面体”)空隙中,该晶胞的空间利用率为___________ (铼的原子半径为rRepm,氧原子半径为rOpm,列出计算式)。
(1)镍原子价电子表示式为
(2)铼易形成高配位数的化合物如Re2(CO)10,该配合物中
(3)锌在潮湿的空气中极易生成一层紧密的碱式碳酸锌[ZnCO3·3Zn(OH)2]薄膜,使其具有抗腐蚀性。碱式碳酸锌中非金属元素的电负性由大到小的顺序为
 的空间构型为
的空间构型为 互为等电子体的分子是
互为等电子体的分子是(4)
 分子中碳原子的杂化类型为
分子中碳原子的杂化类型为 比
比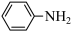 的熔点沸点
的熔点沸点(5)三氧化铼晶胞如图所示,摩尔质量为Mg/mol,晶胞密度为bg/cm3,铼原子填在

2023高三·全国·专题练习 查看更多[1]
(已下线)预测卷01-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)
更新时间:2023-04-12 19:21:26
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】分碳元素是形成单质及化合物种类最多的元素。回答下列问题:
(1)碳能与氢、氮、氧元素构成化合物CO(NH2)2,该分子中各元素电负性由大到小的顺序为_____ ,其中C原子的杂化方式为____ ,该物质易溶于水的主要原因是____ 。
(2)CO是碳元素的常见氧化物,与N2互为等电子体,则CO的结构式为_______ ;CO可以和很多过渡金属形成配合物,如Ni(CO)4,写出基态Ni原子的电子排布式:_______ 。
(3)碳的某种晶体为层状结构,可与熔融金属钾作用。钾原子填充在各层之间,形成间隙化合物,其常见结构的平面投影如图①所示,则其化学式可表示为_______ 。
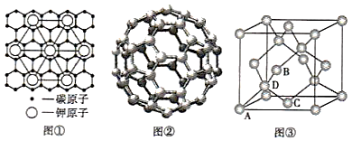
(4)图②为碳的一种同素异形体C60分子,每个C60分子中含有σ键的数目为_______ 。
(5)图③为碳的另一种同素异形体金刚石的晶胞, 晶胞中有4个碳原子填充在四面体空隙中,则四面体空隙填充率为_______ 。
(6)立方氮化硼晶体的结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5 pm。立方氮化硼晶胞的密度是_______ g•cm-3(列出计算式即可,阿伏加德罗常数的值为NA)。
(1)碳能与氢、氮、氧元素构成化合物CO(NH2)2,该分子中各元素电负性由大到小的顺序为
(2)CO是碳元素的常见氧化物,与N2互为等电子体,则CO的结构式为
(3)碳的某种晶体为层状结构,可与熔融金属钾作用。钾原子填充在各层之间,形成间隙化合物,其常见结构的平面投影如图①所示,则其化学式可表示为

(4)图②为碳的一种同素异形体C60分子,每个C60分子中含有σ键的数目为
(5)图③为碳的另一种同素异形体金刚石的晶胞, 晶胞中有4个碳原子填充在四面体空隙中,则四面体空隙填充率为
(6)立方氮化硼晶体的结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5 pm。立方氮化硼晶胞的密度是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】回答下列问题:
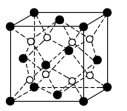
(1)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中Cu原子处于面心,Au原子处于顶点,上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2(见图)的结构相似,该晶体储氢后的化学式应为_______ 。
(2)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一、1 molNH4BF4含有_______ 个配位键。
(3)中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为_______ ,该阴离子中的大Π键可表示为_______ 。
(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。磷化硼是一种超硬耐磨的涂层材料,其晶胞结构如图所示,其中原子坐标参数A为(0,0,0);B为( ,
, ,1);D为(1,1,1)。则C的原子坐标参数为
,1);D为(1,1,1)。则C的原子坐标参数为_______ 。

②晶胞参数,描述晶胞的大小和形状。P原子与B原子的最近距离为a pm,则磷化硼晶体的密度为_______ g·cm-3。(用含a的代数式表示)
③CaTiO3的晶胞如图(a)所示,一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子CH3NH ,其晶胞如图(b)所示。其中Pb2+与图(a)中
,其晶胞如图(b)所示。其中Pb2+与图(a)中_______ 的空间位置相同。

(1)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中Cu原子处于面心,Au原子处于顶点,上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2(见图)的结构相似,该晶体储氢后的化学式应为

(2)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一、1 molNH4BF4含有
(3)中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为
(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。磷化硼是一种超硬耐磨的涂层材料,其晶胞结构如图所示,其中原子坐标参数A为(0,0,0);B为(
 ,
, ,1);D为(1,1,1)。则C的原子坐标参数为
,1);D为(1,1,1)。则C的原子坐标参数为
②晶胞参数,描述晶胞的大小和形状。P原子与B原子的最近距离为a pm,则磷化硼晶体的密度为
③CaTiO3的晶胞如图(a)所示,一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子CH3NH
 ,其晶胞如图(b)所示。其中Pb2+与图(a)中
,其晶胞如图(b)所示。其中Pb2+与图(a)中
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】Ⅰ.尿素[CO(NH2)2]是人工合成的第一种有机物,可用于制有机铁肥,主要代表有[Fe(H2NCONH2)6](NO3)3。
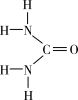
(1)[Fe(H2NCONH2)6](NO3)3中所含元素的电负性由大到小的顺序是______________ 。
(2)尿素中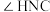
______________ 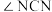 (填“>”“=”“<”),理由是
(填“>”“=”“<”),理由是______________ 。
(3)[Fe(H2NCONH2)6](NO3)3中不存在 的化学键____________ (填序号)。
A.离子键 B.金属键 C.配位键 D. 键 E.
键 E. 键
键
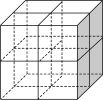
Ⅱ. 是一种贮氢的金属氢化物,可通过氢化镁和镍单质球磨制成。
是一种贮氢的金属氢化物,可通过氢化镁和镍单质球磨制成。 晶胞形状为如图立方体,边长为
晶胞形状为如图立方体,边长为 ,
, 原子占据顶点和面心,
原子占据顶点和面心, 处于八个小立方体的体心。
处于八个小立方体的体心。
(4) 原子的价电子排布式为
原子的价电子排布式为______________ 。
(5) 位于
位于 原子形成的
原子形成的______________ (填“八面体空隙”或“四面体空隙”)。
(6)该晶体的密度为___________  (用含a、
(用含a、 代数式表示)。
代数式表示)。

(1)[Fe(H2NCONH2)6](NO3)3中所含元素的电负性由大到小的顺序是
(2)尿素中
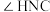
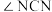 (填“>”“=”“<”),理由是
(填“>”“=”“<”),理由是(3)[Fe(H2NCONH2)6](NO3)3中
A.离子键 B.金属键 C.配位键 D.
 键 E.
键 E. 键
键Ⅱ.
 是一种贮氢的金属氢化物,可通过氢化镁和镍单质球磨制成。
是一种贮氢的金属氢化物,可通过氢化镁和镍单质球磨制成。 晶胞形状为如图立方体,边长为
晶胞形状为如图立方体,边长为 ,
, 原子占据顶点和面心,
原子占据顶点和面心, 处于八个小立方体的体心。
处于八个小立方体的体心。
(4)
 原子的价电子排布式为
原子的价电子排布式为(5)
 位于
位于 原子形成的
原子形成的(6)该晶体的密度为
 (用含a、
(用含a、 代数式表示)。
代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】碳是地球上组成生命的最基本的元素之一。按要求回答:
 碳原子核外有
碳原子核外有________ 种不同空间运动状态的电子
 碳元素能形成多种无机物。石墨与钾可形成石墨夹层离子晶体
碳元素能形成多种无机物。石墨与钾可形成石墨夹层离子晶体 如图
如图 ,其结构为每隔一层碳原子插入一层钾原子,与钾原子层相邻的上下两层碳原子排列方式相同,则与钾最近等距的配位碳原子有
,其结构为每隔一层碳原子插入一层钾原子,与钾原子层相邻的上下两层碳原子排列方式相同,则与钾最近等距的配位碳原子有_________ 个。

 碳也可形成多种有机化合物,下图所示是一种嘌呤和一种吡啶的结构,两种分子中所有原子都在一个平面上。
碳也可形成多种有机化合物,下图所示是一种嘌呤和一种吡啶的结构,两种分子中所有原子都在一个平面上。 吡啶分子中含有
吡啶分子中含有 键数目是
键数目是__________ 。

 嘌呤结构中N原子的杂化方式为
嘌呤结构中N原子的杂化方式为________ 。
 嘌呤中轨道之间的夹角
嘌呤中轨道之间的夹角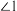 比
比 大,解释原因
大,解释原因___________ 。
 将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代可形成碳的一种新型三维立方晶体结构
将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代可形成碳的一种新型三维立方晶体结构 碳。已知
碳。已知 碳密度为
碳密度为 ,阿伏加 德罗常数为
,阿伏加 德罗常数为 ,则
,则 碳的晶胞参数
碳的晶胞参数
________  写出表达式即可
写出表达式即可 。
。

 碳原子核外有
碳原子核外有 碳元素能形成多种无机物。石墨与钾可形成石墨夹层离子晶体
碳元素能形成多种无机物。石墨与钾可形成石墨夹层离子晶体 如图
如图 ,其结构为每隔一层碳原子插入一层钾原子,与钾原子层相邻的上下两层碳原子排列方式相同,则与钾最近等距的配位碳原子有
,其结构为每隔一层碳原子插入一层钾原子,与钾原子层相邻的上下两层碳原子排列方式相同,则与钾最近等距的配位碳原子有
 碳也可形成多种有机化合物,下图所示是一种嘌呤和一种吡啶的结构,两种分子中所有原子都在一个平面上。
碳也可形成多种有机化合物,下图所示是一种嘌呤和一种吡啶的结构,两种分子中所有原子都在一个平面上。 吡啶分子中含有
吡啶分子中含有 键数目是
键数目是
 嘌呤结构中N原子的杂化方式为
嘌呤结构中N原子的杂化方式为 嘌呤中轨道之间的夹角
嘌呤中轨道之间的夹角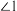 比
比 大,解释原因
大,解释原因 将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代可形成碳的一种新型三维立方晶体结构
将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代可形成碳的一种新型三维立方晶体结构 碳。已知
碳。已知 碳密度为
碳密度为 ,阿伏加 德罗常数为
,阿伏加 德罗常数为 ,则
,则 碳的晶胞参数
碳的晶胞参数
 写出表达式即可
写出表达式即可 。
。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】铀氮化合物是核燃料循环系统中的重要材料。
已知 。回答下列问题:
。回答下列问题:
(1)基态氮原子价电子轨道表示式为___________ 。
(2)反应中断裂的化学键有___________ (填标号)。
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
(3)反应所得的气态产物中属于非极性分子的是___________ (填化学式,下同);氢化物中更易与 形成配离子的是
形成配离子的是___________ ,解释原因___________ 。
(4)基态U原子的外围电子排布式为 ,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是___________(填标号)。
,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是___________(填标号)。
(5) 的空间构型为
的空间构型为___________ ,其结构中存在大π键,可表示为___________ (用 表示,m代表参与形成大
表示,m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数)。
键的电子数)。
(6)某种铀氮化物的晶胞如图。已知晶胞密度为 ,U原子半径为
,U原子半径为 ,N原子半径为
,N原子半径为 ,设
,设 为阿伏加德罗常数的值,则该晶胞的空间利用率为
为阿伏加德罗常数的值,则该晶胞的空间利用率为___________ (用含d、 、
、 、
、 的式子表示)。
的式子表示)。

已知
 。回答下列问题:
。回答下列问题:(1)基态氮原子价电子轨道表示式为
(2)反应中断裂的化学键有
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
(3)反应所得的气态产物中属于非极性分子的是
 形成配离子的是
形成配离子的是(4)基态U原子的外围电子排布式为
 ,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是___________(填标号)。
,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是___________(填标号)。A. | B. | C.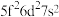 | D. |
 的空间构型为
的空间构型为 表示,m代表参与形成大
表示,m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数)。
键的电子数)。(6)某种铀氮化物的晶胞如图。已知晶胞密度为
 ,U原子半径为
,U原子半径为 ,N原子半径为
,N原子半径为 ,设
,设 为阿伏加德罗常数的值,则该晶胞的空间利用率为
为阿伏加德罗常数的值,则该晶胞的空间利用率为 、
、 、
、 的式子表示)。
的式子表示)。
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】已知X、Y、Z三种元素均为短周期元素,原子序数依次递增,Q、W为前30号元素。5种元素的部分特点:
(1)XF3分子中X的杂化类型为______ ,该分子的空间构型为_______ .
(2)基态Q原子的电子排布式为_____________________ ,第一电离能:X______ Y(填“>” “<”或“=”) .
(3)X、Y、Z电负性由大到小的顺序为____________ (用元素符号表示).
(4)Na在Y2中燃烧产物的电子式为________________ .
(5)Z和X形成的化合物常用作高温耐火材料,化学性质稳定,据此推测它应属于_______ 晶体.

(6)W元素与X元素形成某种化合物的晶胞结构如图所示(黑球代表W原子),若该晶体的密度为ρ g·cm-3,则该晶胞的体积是__________ cm3.
| 元素 | 特点 |
| X | 其气态氢化呈三角锥形,水溶液显碱性 |
| Y | 基态原子核外有三个能级,其中最外层电子数等于次外层电子数的3倍 |
| Z | 元素原子的外围电子层排布式为 |
| Q | 被誉为“太空金属”,也有“生物金属”之称,其基态原子次外层有2个未成对电子 |
| W | 原子M能级层为全充满状态且核外的未成对电子只有一个 |
(2)基态Q原子的电子排布式为
(3)X、Y、Z电负性由大到小的顺序为
(4)Na在Y2中燃烧产物的电子式为
(5)Z和X形成的化合物常用作高温耐火材料,化学性质稳定,据此推测它应属于

(6)W元素与X元素形成某种化合物的晶胞结构如图所示(黑球代表W原子),若该晶体的密度为ρ g·cm-3,则该晶胞的体积是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】合理应用和处理氮的化合物,在生产生活中有重要意义。完成下列填空:
(1)尿素[CO(NH2)2]是一种高效化肥,其分子中各原子的原子半径由大到小顺序为______ ;碳原子核外电子排布式______ ,其最外层______ 种能量不同的电子,有______ 种不同形状的电子云。
(2)氰化钠(NaCN)中,N元素显—3价,则非金属性N______ C(填“<”、“=”或“>”),从原子结构角度解释非金属性强弱的原因______ 。
(3)C3N4是一种硬度可以和金刚石媲美的而在自然界中尚未发现的新的共价化合物,结合所学知识解释它高硬度的性质______ 。
(4)氰化钠属于剧毒物质,可用双氧水或硫代硫酸钠处理。
①用双氧水处理,发生的反应为:NaCN+H2O2+H2O=A+NH3↑,则A的化学式为______ 。
②NaCN与Na2S2O3二者等物质的量反应可得到两种含硫元素的离子,其中一种遇到Fe3+显血红色。写出该反应的离子方程式______ 。
(5)NO2会污染环境,可用Na2CO3溶液吸收NO2并放出CO2。已知9.2gNO2和Na2CO3溶液完全反应时转移电子0.1mol,此反应的离子方程式是______ ;恰好反应后,所得溶液呈弱碱性,则溶液中各离子浓度大小关系是______ 。
(1)尿素[CO(NH2)2]是一种高效化肥,其分子中各原子的原子半径由大到小顺序为
(2)氰化钠(NaCN)中,N元素显—3价,则非金属性N
(3)C3N4是一种硬度可以和金刚石媲美的而在自然界中尚未发现的新的共价化合物,结合所学知识解释它高硬度的性质
(4)氰化钠属于剧毒物质,可用双氧水或硫代硫酸钠处理。
①用双氧水处理,发生的反应为:NaCN+H2O2+H2O=A+NH3↑,则A的化学式为
②NaCN与Na2S2O3二者等物质的量反应可得到两种含硫元素的离子,其中一种遇到Fe3+显血红色。写出该反应的离子方程式
(5)NO2会污染环境,可用Na2CO3溶液吸收NO2并放出CO2。已知9.2gNO2和Na2CO3溶液完全反应时转移电子0.1mol,此反应的离子方程式是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】碳族中的碳、硅、锗及其化合物在多领域有重要用途。
(1)基态 的电子排布式为
的电子排布式为___________ 。
(2)我国科学家研发的“液态阳光”计划是通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。 分子中存在
分子中存在___________ 个 键和
键和___________ 个 键,
键, 分子是
分子是___________ 分子(填“极性”或“非极性”)。
(3)关于 、
、 及其化合物的结构与性质,下列论述
及其化合物的结构与性质,下列论述不正确 的是___________。
(4) 与
与 -甲基咪唑(
-甲基咪唑(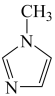 )反应可以得到
)反应可以得到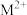 ,其结构如下图所示:
,其结构如下图所示:

 -甲基咪唑中碳原子的杂化轨道类型有
-甲基咪唑中碳原子的杂化轨道类型有___________ 。
(5)汞( )、锗(
)、锗( )、锑(
)、锑( )形成的一种新物质
)形成的一种新物质 为潜在的拓扑绝缘体材料。
为潜在的拓扑绝缘体材料。 的晶体(晶胞为下图
的晶体(晶胞为下图 )可视为
)可视为 晶体(晶胞为下图
晶体(晶胞为下图 )中部分
)中部分 原子被
原子被 和
和 取代后形成。
取代后形成。
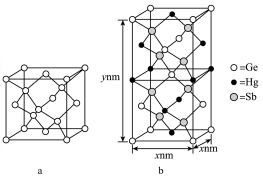
 的最简式的相对分子质量为
的最简式的相对分子质量为 ,阿伏加德罗常数的数值为
,阿伏加德罗常数的数值为 ,则
,则 晶体的密度为
晶体的密度为___________  (列出计算式)。注:
(列出计算式)。注:
(1)基态
 的电子排布式为
的电子排布式为(2)我国科学家研发的“液态阳光”计划是通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。
 分子中存在
分子中存在 键和
键和 键,
键, 分子是
分子是(3)关于
 、
、 及其化合物的结构与性质,下列论述
及其化合物的结构与性质,下列论述A.键能 、 、 ,因此 ,因此 稳定性小于 稳定性小于 |
B. 是与金刚石结构相似的共价晶体,因此 是与金刚石结构相似的共价晶体,因此 具有较高的硬度 具有较高的硬度 |
C. 中 中 的化合价为 的化合价为 , , 中 中 的化合价为 的化合价为 ,因此 ,因此 还原性小于 还原性小于 |
D. 原子间难形成双键和三键而 原子间难形成双键和三键而 原子间可以,是因为 原子间可以,是因为 的原子半径大于 的原子半径大于 ,因此难以形成 ,因此难以形成 键 键 |
 与
与 -甲基咪唑(
-甲基咪唑( )反应可以得到
)反应可以得到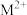 ,其结构如下图所示:
,其结构如下图所示:
 -甲基咪唑中碳原子的杂化轨道类型有
-甲基咪唑中碳原子的杂化轨道类型有(5)汞(
 )、锗(
)、锗( )、锑(
)、锑( )形成的一种新物质
)形成的一种新物质 为潜在的拓扑绝缘体材料。
为潜在的拓扑绝缘体材料。 的晶体(晶胞为下图
的晶体(晶胞为下图 )可视为
)可视为 晶体(晶胞为下图
晶体(晶胞为下图 )中部分
)中部分 原子被
原子被 和
和 取代后形成。
取代后形成。
 的最简式的相对分子质量为
的最简式的相对分子质量为 ,阿伏加德罗常数的数值为
,阿伏加德罗常数的数值为 ,则
,则 晶体的密度为
晶体的密度为 (列出计算式)。注:
(列出计算式)。注:
您最近一年使用:0次
【推荐3】完成下列问题
(1)氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性 (晶体结构如图)。

①关于这两种晶体的说法,不正确的是___________ (填字母)。
a.两种晶体均为分子晶体
b.两种晶体中的B﹣N键均为共价键
c.六方相氮化硼层间作用力小,所以质地软
d.立方相氮化硼含有σ键和π键,所以硬度大
②六方相氮化硼晶体其结构与石墨相似却不导电,原因是___________
(2)石墨的晶胞结构如图所示。已知石墨的密度为ρg·cm-3,C-C键的键长为r cm,NA为阿伏加德罗常数的值,则石墨晶体的层间距d=___________ cm。

(1)氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性 (晶体结构如图)。

①关于这两种晶体的说法,不正确的是
a.两种晶体均为分子晶体
b.两种晶体中的B﹣N键均为共价键
c.六方相氮化硼层间作用力小,所以质地软
d.立方相氮化硼含有σ键和π键,所以硬度大
②六方相氮化硼晶体其结构与石墨相似却不导电,原因是
(2)石墨的晶胞结构如图所示。已知石墨的密度为ρg·cm-3,C-C键的键长为r cm,NA为阿伏加德罗常数的值,则石墨晶体的层间距d=

您最近一年使用:0次



