Ⅰ.尿素[CO(NH2)2]是人工合成的第一种有机物,可用于制有机铁肥,主要代表有[Fe(H2NCONH2)6](NO3)3。
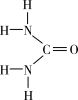
(1)[Fe(H2NCONH2)6](NO3)3中所含元素的电负性由大到小的顺序是______________ 。
(2)尿素中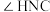
______________ 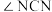 (填“>”“=”“<”),理由是
(填“>”“=”“<”),理由是______________ 。
(3)[Fe(H2NCONH2)6](NO3)3中不存在 的化学键____________ (填序号)。
A.离子键 B.金属键 C.配位键 D. 键 E.
键 E. 键
键
Ⅱ. 是一种贮氢的金属氢化物,可通过氢化镁和镍单质球磨制成。
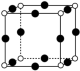
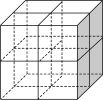
是一种贮氢的金属氢化物,可通过氢化镁和镍单质球磨制成。 晶胞形状为如图立方体,边长为
晶胞形状为如图立方体,边长为 ,
, 原子占据顶点和面心,
原子占据顶点和面心, 处于八个小立方体的体心。
处于八个小立方体的体心。
(4) 原子的价电子排布式为
原子的价电子排布式为______________ 。
(5) 位于
位于 原子形成的
原子形成的______________ (填“八面体空隙”或“四面体空隙”)。
(6)该晶体的密度为___________  (用含a、
(用含a、 代数式表示)。
代数式表示)。

(1)[Fe(H2NCONH2)6](NO3)3中所含元素的电负性由大到小的顺序是
(2)尿素中
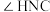
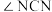 (填“>”“=”“<”),理由是
(填“>”“=”“<”),理由是(3)[Fe(H2NCONH2)6](NO3)3中
A.离子键 B.金属键 C.配位键 D.
 键 E.
键 E. 键
键Ⅱ.
 是一种贮氢的金属氢化物,可通过氢化镁和镍单质球磨制成。
是一种贮氢的金属氢化物,可通过氢化镁和镍单质球磨制成。 晶胞形状为如图立方体,边长为
晶胞形状为如图立方体,边长为 ,
, 原子占据顶点和面心,
原子占据顶点和面心, 处于八个小立方体的体心。
处于八个小立方体的体心。
(4)
 原子的价电子排布式为
原子的价电子排布式为(5)
 位于
位于 原子形成的
原子形成的(6)该晶体的密度为
 (用含a、
(用含a、 代数式表示)。
代数式表示)。
22-23高三上·福建泉州·阶段练习 查看更多[2]
更新时间:2022-12-20 17:10:12
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】2020年1月,南开大学研究团队“高效手性螺环催化剂的发现”获得2019年度国家自然科学技术一等奖,含多种金属元素的催化剂正在刷新合成化学的新高度。
回答下列问题:
(1)形成“刚性”螺环的元素是碳,基态碳原子的价电子轨道表达式是___ 。
(2)如图是一种简单螺环烃,分子中碳原子的杂化方式为___ ,分子中___ (填“含”或“不含”)手性碳原子。
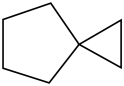
(3)铁及其化合物羰基铁[Fe(CO)5]常用作催化剂。
①1mol Fe(CO)5分子中含有的σ键数目为____ ,写出一种与CO互为等电子体的离子___ 。
②Fe(CO)5是一种浅黄色液体,熔点-20℃,沸点103℃,热稳定性较高,易溶于苯等有机溶剂,不溶于水。Fe(CO)5是___ (填“极性”或“非极性”)分子;配体CO提供孤电子对的原子是C而不是O,原因是____ 。
③如图是某Fe单质的晶胞模型。已知晶体密度为d g·cm-3,则铁原子的半径为___ nm(用含有d、NA的代数式表示)。
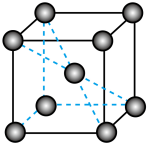
(4)在某些过渡金属的羰基化合物中,中心原子的价电子数与配体提供的电子数之和满足“18e-结构规则”。羰基铁与羰基镍的化学式分别为Fe(CO)5和Ni(CO)4,则羰基铬的化学式是___ 。
回答下列问题:
(1)形成“刚性”螺环的元素是碳,基态碳原子的价电子轨道表达式是
(2)如图是一种简单螺环烃,分子中碳原子的杂化方式为

(3)铁及其化合物羰基铁[Fe(CO)5]常用作催化剂。
①1mol Fe(CO)5分子中含有的σ键数目为
②Fe(CO)5是一种浅黄色液体,熔点-20℃,沸点103℃,热稳定性较高,易溶于苯等有机溶剂,不溶于水。Fe(CO)5是
③如图是某Fe单质的晶胞模型。已知晶体密度为d g·cm-3,则铁原子的半径为

(4)在某些过渡金属的羰基化合物中,中心原子的价电子数与配体提供的电子数之和满足“18e-结构规则”。羰基铁与羰基镍的化学式分别为Fe(CO)5和Ni(CO)4,则羰基铬的化学式是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】江四矿产资源丰富,其中铁、锰、钛、钒、铜、锌、金、银等储量居全国前3位,有亚洲最大的铜矿和中国最大的铜冶炼基地。回答下列问题:
(1)铜原子价层电子排布图______ 。
(2) 是一种常见农药,能防治真菌、细菌和霉菌引起的多种病害。1mol
是一种常见农药,能防治真菌、细菌和霉菌引起的多种病害。1mol  中含有的
中含有的 键数目为
键数目为______ ; 分子与
分子与 形成配合物后
形成配合物后 键角
键角______ (填“变大”“变小”或“不变”)。
(3)Cu与Fe的第二电离能分别为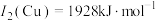 、
、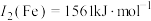 ,
,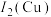 大于
大于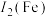 的主要原因是
的主要原因是______ 。
(4) 蒸气状态下以双聚分子形式在(如图),其中Fe的配位数为
蒸气状态下以双聚分子形式在(如图),其中Fe的配位数为______ ,双聚分子中存在配位键,提供空轨道的是______ (填元素符号)原子。______ ;若合金的密度为 ,
, 代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是
代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是______ pm(用含 和
和 的计算式表示,不必化简)。
的计算式表示,不必化简)。
(1)铜原子价层电子排布图
(2)
 是一种常见农药,能防治真菌、细菌和霉菌引起的多种病害。1mol
是一种常见农药,能防治真菌、细菌和霉菌引起的多种病害。1mol  中含有的
中含有的 键数目为
键数目为 分子与
分子与 形成配合物后
形成配合物后 键角
键角(3)Cu与Fe的第二电离能分别为
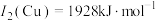 、
、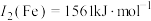 ,
,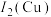 大于
大于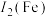 的主要原因是
的主要原因是(4)
 蒸气状态下以双聚分子形式在(如图),其中Fe的配位数为
蒸气状态下以双聚分子形式在(如图),其中Fe的配位数为
 ,
, 代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是
代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是 和
和 的计算式表示,不必化简)。
的计算式表示,不必化简)。
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】Q、R、X、Y、Z是原子序数依次增大的前四周期元素,Q的一种单质是天然存在的最硬的物质,X原子的核外电子有八种运动状态,Y元素的离子半径是第三周期中最小的,Z是第四周期中未成对电子最多的原子。
(1)Z原子的价电子排布式为_________________ 。
(2)Q、R、X、Y四种元素的电负性由大到小的顺序是_______________ 。
(3)杂化轨道理论指出原子中能量相近的s、p或s、p、d轨道之间可以通过杂化形成种类丰富的杂化轨道。RCl3分子中心原子的杂化方式为___________ ,从原子结构的角度解释不存在RCl5分子的原因_______ 。
(4)配合物甲的分子式为ZCl3·4H2O,配位数为6。取1mol甲溶于水,加入足量的AgNO3溶液,得到143.5g白色沉淀。在酸性溶液中,甲发生水合反应转化为乙(ZCl3·6H2O)。乙的配位原子只有一种,配位数为6。
①甲的结构简式为_______________ 。
②甲→乙的化学方程式为______________ 。
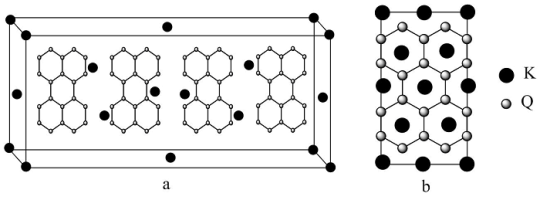
(5)图a是Q的一种同素异形体和钾形成的插层化合物的晶胞图,图b是晶胞沿侧面的投影图。该插层化合物的化学式为______________ 。
(1)Z原子的价电子排布式为
(2)Q、R、X、Y四种元素的电负性由大到小的顺序是
(3)杂化轨道理论指出原子中能量相近的s、p或s、p、d轨道之间可以通过杂化形成种类丰富的杂化轨道。RCl3分子中心原子的杂化方式为
(4)配合物甲的分子式为ZCl3·4H2O,配位数为6。取1mol甲溶于水,加入足量的AgNO3溶液,得到143.5g白色沉淀。在酸性溶液中,甲发生水合反应转化为乙(ZCl3·6H2O)。乙的配位原子只有一种,配位数为6。
①甲的结构简式为
②甲→乙的化学方程式为
(5)图a是Q的一种同素异形体和钾形成的插层化合物的晶胞图,图b是晶胞沿侧面的投影图。该插层化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】已知Mn、Fe、Co是合金中的重要元素,而P、S、Cl是农药中的重要元素。请回答下列问题:
(1)基态锰原子的价电子排布图为_______ ,锰有多种化合价,在+2、+3、+4、+5和+6中,最稳定的化合价是_______ 。
(2)已知PCl3的沸点高于SCl2,原因是:_______ 。
(3)已知P4(白磷)为正四面体结构,与氧气反应生成非极性分子P4O10,其中P在空间的相对位置不变,则P4O10中σ键和π键的数目之比为_______ 。
(4)如图为酞菁钴分子的平面结构,下列说法不正确的是____________ 。

A.电负性:N>C>H B.4个N原子均与Co形成配位键
C.分子中N的杂化轨道类型均为sp2D.第一电离能:N<O
(5)如图是一种由Y(与Sc同族)、Ba、Fe、O组成的晶体,晶胞棱上的球代表Ba,顶点的球代表Y,四方锥中心和八面体中心的球代表Fe,小球代表O。

①该晶体的化学式为_______ 。
②其中Y的配位数为_______ 。
③在氧气气氛中该晶体可被部分氧化,氧原子进入晶格而使晶体呈现深紫色。则被氧化的元素是_______ (填符号),新进入的氧原子在晶胞中的位置是______ 。
(1)基态锰原子的价电子排布图为
(2)已知PCl3的沸点高于SCl2,原因是:
(3)已知P4(白磷)为正四面体结构,与氧气反应生成非极性分子P4O10,其中P在空间的相对位置不变,则P4O10中σ键和π键的数目之比为
(4)如图为酞菁钴分子的平面结构,下列说法不正确的是

A.电负性:N>C>H B.4个N原子均与Co形成配位键
C.分子中N的杂化轨道类型均为sp2D.第一电离能:N<O
(5)如图是一种由Y(与Sc同族)、Ba、Fe、O组成的晶体,晶胞棱上的球代表Ba,顶点的球代表Y,四方锥中心和八面体中心的球代表Fe,小球代表O。

①该晶体的化学式为
②其中Y的配位数为
③在氧气气氛中该晶体可被部分氧化,氧原子进入晶格而使晶体呈现深紫色。则被氧化的元素是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
(1)Y的轨道表示式为________;
(2)X、Y、Z三种元素的原子半径从大到小的顺序是________(用元素符号表示);
(3)XY2的分子中存在________个σ键,分子的空间构形为________,在H-Y、H-Z两种共价键中,键长较长的是________;
(4)W3+的核外电子排布式是________;
(5)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y.此反应的化学方程式是________;
(6)请设计一个实验方案,比较Y、Z单质氧化性的强弱________.
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为56,中子数为30 |
(1)Y的轨道表示式为________;
(2)X、Y、Z三种元素的原子半径从大到小的顺序是________(用元素符号表示);
(3)XY2的分子中存在________个σ键,分子的空间构形为________,在H-Y、H-Z两种共价键中,键长较长的是________;
(4)W3+的核外电子排布式是________;
(5)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y.此反应的化学方程式是________;
(6)请设计一个实验方案,比较Y、Z单质氧化性的强弱________.
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】含硒(Se)化合物在材料药物领域有重要应用。
(1)Se与S同族,基态Se原子的简化电子排布式为___________ ,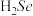 的沸点高于
的沸点高于 ,原因是
,原因是___________ 。
(2)一种含硒的新型 (聚集诱导发光)分子Ⅳ的合成路线如下,下列关于路线中I~Ⅳ的说法正确的有___________。
(聚集诱导发光)分子Ⅳ的合成路线如下,下列关于路线中I~Ⅳ的说法正确的有___________。
(3)硒的两种含氧酸的酸性强弱为
___________  (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠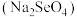 可减轻重金属铊(
可减轻重金属铊( )引起的中毒,
)引起的中毒, 的空间结构为
的空间结构为___________ 。
(4)铊( )与
)与 同族,第一电离能
同族,第一电离能
___________  (填“>”或“<”)。
(填“>”或“<”)。
(5)根据下表中元素的电负性数值判断, 为
为___________ (填“离子化合物”或“共价化合物”,下同), 为
为___________ 。
(6)气态 通常以二聚体
通常以二聚体 的形式存在,其空间结构如图a所示,二聚体中
的形式存在,其空间结构如图a所示,二聚体中 的轨道杂化类型为
的轨道杂化类型为___________ 。 结构如图b所示,若晶胞参数(立方体棱长)为
结构如图b所示,若晶胞参数(立方体棱长)为 ,则晶体密度
,则晶体密度
___________  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
(1)Se与S同族,基态Se原子的简化电子排布式为
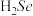 的沸点高于
的沸点高于 ,原因是
,原因是(2)一种含硒的新型
 (聚集诱导发光)分子Ⅳ的合成路线如下,下列关于路线中I~Ⅳ的说法正确的有___________。
(聚集诱导发光)分子Ⅳ的合成路线如下,下列关于路线中I~Ⅳ的说法正确的有___________。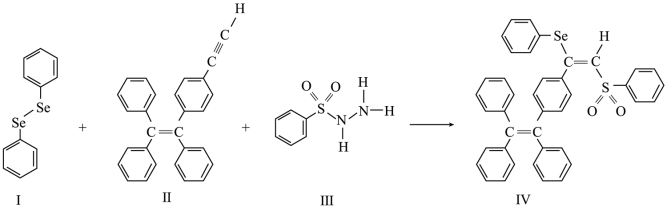
A.Ⅰ中含有两种元素, 键为非极性键 键为非极性键 |
B.Ⅱ中C原子的杂化轨道类型有 与 与 |
| C.Ⅲ中含有的元素中,O的电负性最大 |
D.Ⅳ中 原子的杂化轨道类型为 原子的杂化轨道类型为 |
(3)硒的两种含氧酸的酸性强弱为

 (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠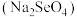 可减轻重金属铊(
可减轻重金属铊( )引起的中毒,
)引起的中毒, 的空间结构为
的空间结构为(4)铊(
 )与
)与 同族,第一电离能
同族,第一电离能
 (填“>”或“<”)。
(填“>”或“<”)。(5)根据下表中元素的电负性数值判断,
 为
为 为
为| 元素 | F |  |  |
| 电负性 | 4.0 | 1.5 | 3.0 |
(6)气态
 通常以二聚体
通常以二聚体 的形式存在,其空间结构如图a所示,二聚体中
的形式存在,其空间结构如图a所示,二聚体中 的轨道杂化类型为
的轨道杂化类型为 结构如图b所示,若晶胞参数(立方体棱长)为
结构如图b所示,若晶胞参数(立方体棱长)为 ,则晶体密度
,则晶体密度
 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
|
|
| 图a | 图b |
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】钛是一种稀有金属,具有密度小、强度高、耐腐蚀等特点,钛和钛的化合物在航天、化工、建筑、日常生活中都有着广泛的用途。已知:阿伏加德罗常数的值为NA。
(1)基态钛原子价电子排布式为_______ ;与钛同周期的元素中,基态原子的未成对电子数与钛相同的还有_______ 种。
(2)钛的一种常见化合物是[Ti(H2O)6]Cl3,1mol该物质中含有σ键的数目为_______ ,配体H2O的VSEPR模型名称是_______ ,其沸点高于H2S,原因是_______ 。
(3)TO2与光气(COCl2)、氯化亚砜(SOCl2)等反应可以制得TiCl4,用于制造虹彩剂、烟雾、颜料等。
①氯化亚砜中心原子的杂化方式为_______ 杂化;
②光气是_______ 分子(填“极性”或“非极性”)。
(4)铁与钛同周期,某离子型铁氧化物晶胞如图所示,它由X、Y组成,则该氧化物的化学式为_______ 。已知该晶体的晶胞参数为a pm,阿伏加德罗常数的值为NA,则该晶体的密度d=_______  (用含a和NA的代数式表示)。
(用含a和NA的代数式表示)。

(1)基态钛原子价电子排布式为
(2)钛的一种常见化合物是[Ti(H2O)6]Cl3,1mol该物质中含有σ键的数目为
(3)TO2与光气(COCl2)、氯化亚砜(SOCl2)等反应可以制得TiCl4,用于制造虹彩剂、烟雾、颜料等。
①氯化亚砜中心原子的杂化方式为
②光气是
(4)铁与钛同周期,某离子型铁氧化物晶胞如图所示,它由X、Y组成,则该氧化物的化学式为
 (用含a和NA的代数式表示)。
(用含a和NA的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】铬同铁、钴、镍、铜等金属形成的合金,用于航空、宇航、电器、仪表及高端科技领域。
(1)铬的基态原子的价电子层排布式是__________________ ;
(2)氯化铬酰(CrO2Cl2)的熔点为-96.5℃,沸点为117℃,固态氯化铬酰属于_______ 晶体。制备CrO2Cl2的反应为K2Cr2O7+3CCl4=2KCl+2CrO2Cl2+3COCl2↑,COCl2分子中σ键和π键的个数比为_____ ,空间构型为_______ ;CCl4的中心原子杂化类型为________ ,其等电子体为___________ (写出一个离子形式);
(3)某镍配合物结构如下图所示。
分子内含有的作用力有_________________ (填序号),其中属于第二周期元素的第一电离能由大到小的顺序是_____________ (填元素符号);
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
(4)向CuSO4溶液中通入氨气得到深蓝色溶液的离子方程式为___________________ ;
(5)CoCl3·4NH3中心原子Co3+配位数为6,向含0.1 mol CoCl3·4NH3的溶液中滴加2 mol·L-1 AgNO3溶液,反应完全共消耗50 mL溶液,则该配合物的化学式为________________ ;
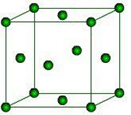
(6)下图是Fe的晶体一种堆积方式,若晶胞的边长为a pm,则晶体的密度为_______ g·cm-3(用含a和NA的表达式表示)。
(1)铬的基态原子的价电子层排布式是
(2)氯化铬酰(CrO2Cl2)的熔点为-96.5℃,沸点为117℃,固态氯化铬酰属于
(3)某镍配合物结构如下图所示。
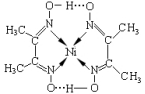
分子内含有的作用力有
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
(4)向CuSO4溶液中通入氨气得到深蓝色溶液的离子方程式为
(5)CoCl3·4NH3中心原子Co3+配位数为6,向含0.1 mol CoCl3·4NH3的溶液中滴加2 mol·L-1 AgNO3溶液,反应完全共消耗50 mL溶液,则该配合物的化学式为
(6)下图是Fe的晶体一种堆积方式,若晶胞的边长为a pm,则晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】回答下列问题:
(1)Li2O是离子晶体,其晶格能可通过图(a)的 Born−Haber循环计算得到。

可知,Li原子的第一电离能为___________ kJ·mol−1,O=O键键能为___________ kJ·mol−1,Li2O晶格能为___________ kJ·mol−1。
(2)Li2O具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为NA,则Li2O的密度为___________ g·cm−3(列出计算式)。
(1)Li2O是离子晶体,其晶格能可通过图(a)的 Born−Haber循环计算得到。

可知,Li原子的第一电离能为
(2)Li2O具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为NA,则Li2O的密度为
您最近一年使用:0次