尾气处理装置(见下图a、b、c)
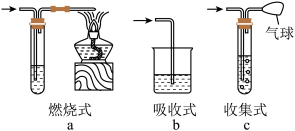
(1)制取Cl2时,尾气的处理可采用________ 装置。
(2)制取CO时,尾气处理可采用________ 装置。
(3)制取H2时,尾气处理可采用________ 装置。

(1)制取Cl2时,尾气的处理可采用
(2)制取CO时,尾气处理可采用
(3)制取H2时,尾气处理可采用
22-23高一下·全国·期中 查看更多[1]
(已下线)专题04 常见气体的实验室制取(知识串讲)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)
更新时间:2023-04-14 13:37:00
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】实验室用MnO2氧化密度为1.19 g·cm-3,溶质质量分数为36.5%的HCl溶液,制备氯气。
(1)该反应的离子方程式为:__________________________________________________ ,该盐酸的物质的量浓度为_______________ mol/L。
(2)生成1molCl2时,转移的电子数目为_______________ 。
(3) 8.7gMnO2与足量浓盐酸反应能使_____________ molHCl被氧化:
(4)浓盐酸在反应中显示出来的性质是___________ .(填字母)
a.还原性b.酸性c.氧化性d.挥发性
(5)用氢氧化钠溶液吸收多余的氯气(用离子方程式表示):_____________________ 。
(1)该反应的离子方程式为:
(2)生成1molCl2时,转移的电子数目为
(3) 8.7gMnO2与足量浓盐酸反应能使
(4)浓盐酸在反应中显示出来的性质是
a.还原性b.酸性c.氧化性d.挥发性
(5)用氢氧化钠溶液吸收多余的氯气(用离子方程式表示):
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】锡(Sn)是第ⅣA族元素,其常见的氯化物为SnCl2和SnCl4。SnCl2常温下为固体,具有强还原性,遇水极易发生水解反应生成难溶于水的Sn(OH)Cl。SnCl4常温下为液体,遇水极易发生水解反应生成难溶于水的SnO2•xH2O。某化学实验小组欲利用如图所示装置制备SnCl4。

回答下列问题:
(1)仪器a的名称为____ ,仪器a中发生反应的化学方程式为___ 。
(2)装置B中盛装的试剂名称为___ ;装置C中盛装的试剂名称为___ ,作用为___ 。
(3)装置连接完成并加入药品后,应先___ (填实验操作),再点燃装置A中的酒精灯,待装置E中充满黄绿色气体,最后点燃装置D中的酒精喷灯,使反应生成的产物汽化后经冷凝管冷凝后进入装置E中。为更好地收集SnCl4,对装置E的改进措施为___ 。
(4)甲同学提出可将装置E中盛有碱石灰的干燥管换成盛有浓NaOH溶液的烧杯并连在装置E的右侧,替换后,将导致的不良后果为____ (用化学方程式表示)。
(5)经测定发现实验所得SnCl4样品中含有极少量的SnCl2,测定样品中Sn2+质量分数的方案如下:取2.00gSnCl4样品置于锥形瓶中,加入适量盐酸溶解,再滴入几滴淀粉溶液作指示剂,用0.01000mol•L-1碘标准液进行滴定,达到滴定终点时(溶液变蓝)消耗标准液的体积为8.40mL,则SnCl4样品中Sn2+的质量分数为____ (保留一位有效数字)。

回答下列问题:
(1)仪器a的名称为
(2)装置B中盛装的试剂名称为
(3)装置连接完成并加入药品后,应先
(4)甲同学提出可将装置E中盛有碱石灰的干燥管换成盛有浓NaOH溶液的烧杯并连在装置E的右侧,替换后,将导致的不良后果为
(5)经测定发现实验所得SnCl4样品中含有极少量的SnCl2,测定样品中Sn2+质量分数的方案如下:取2.00gSnCl4样品置于锥形瓶中,加入适量盐酸溶解,再滴入几滴淀粉溶液作指示剂,用0.01000mol•L-1碘标准液进行滴定,达到滴定终点时(溶液变蓝)消耗标准液的体积为8.40mL,则SnCl4样品中Sn2+的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某兴趣小组设计如下装置进行氯气与金属钠的反应,先将钠预热,在钠熔融成小球时,撤火,并通入氯气发生反应。

(1)实验室制备氯气的化学方程式为_______ 。
(2) 与Na反应会产生大量白烟,白烟的成分是
与Na反应会产生大量白烟,白烟的成分是_______ (填化学式)。
(3)浸有淀粉-KI溶液的棉球变为蓝色,是因为 与KI发生置换反应,该反应的化学方程式为
与KI发生置换反应,该反应的化学方程式为_______ 。
(4)浸有NaOH溶液的棉球的作用是_______ 。若将 通入热的烧碱溶液中,可以得到NaCl、NaClO和
通入热的烧碱溶液中,可以得到NaCl、NaClO和 的混合液。当NaCl和
的混合液。当NaCl和 的物质的量之比为8︰1时,混合液中NaClO和
的物质的量之比为8︰1时,混合液中NaClO和 的物质的量之比为
的物质的量之比为_______ 。

(1)实验室制备氯气的化学方程式为
(2)
 与Na反应会产生大量白烟,白烟的成分是
与Na反应会产生大量白烟,白烟的成分是(3)浸有淀粉-KI溶液的棉球变为蓝色,是因为
 与KI发生置换反应,该反应的化学方程式为
与KI发生置换反应,该反应的化学方程式为(4)浸有NaOH溶液的棉球的作用是
 通入热的烧碱溶液中,可以得到NaCl、NaClO和
通入热的烧碱溶液中,可以得到NaCl、NaClO和 的混合液。当NaCl和
的混合液。当NaCl和 的物质的量之比为8︰1时,混合液中NaClO和
的物质的量之比为8︰1时,混合液中NaClO和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。氯气、漂白液、漂白粉都是生活中常用的含氯消毒剂。家庭中常常使用的消毒剂主要是“84”消毒液,可以说化学让生活更美好。图为“84”消毒液说明书。请回答下列问题:
(1)工业上常用氯气生产84消毒液,请写出反应的离子方程式___________ ,其有效成分为___________ (写化学式)。
(2)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是___________ (用离子方程式表达)。
(3)游泳池水的消毒多用漂粉精,写出漂白精显效的化学方程式___________ 。
(4)Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉、“84”消毒液,主要目的___________。
 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00g/L~60.00g/L | |
| 注意事项 | 不可与其他洗涤剂或消毒液混合使用 | |
| 用法用量 | 稀释后浸泡或洗刷白色衣物、浴缸等1:200水溶液;餐饮具、瓜果等1:100水溶液 |
(1)工业上常用氯气生产84消毒液,请写出反应的离子方程式
(2)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是
(3)游泳池水的消毒多用漂粉精,写出漂白精显效的化学方程式
(4)Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉、“84”消毒液,主要目的___________。
| A.增强漂白能力和消毒作用 |
| B.使它转化为较稳定物质,便于保存和运输 |
| C.使它转化为较易溶于水的物质 |
| D.提高氯的质量分数,有利于漂白、消毒 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下表是生活生产中常见的物质:
(1)分别写出③、⑥的电离方程式__________ ;__________ 。
(2)③与⑥反应的离子方程式:__________ 。
(3)检验⑤的溶液中含有 的方法是:
的方法是:__________ ,有关的离子方程式为__________ 。
(4)常温下,将 通入②中,可以得到一种漂白液,该漂白液的有效成分为
通入②中,可以得到一种漂白液,该漂白液的有效成分为__________ (填名称),检验中②阳离子的方法是__________ (填名称)。
编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
名称 | Na |
|
| 酒精 |
|
|
(2)③与⑥反应的离子方程式:
(3)检验⑤的溶液中含有
 的方法是:
的方法是:(4)常温下,将
 通入②中,可以得到一种漂白液,该漂白液的有效成分为
通入②中,可以得到一种漂白液,该漂白液的有效成分为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应的化学方程式_____________ 漂白粉的有效成分是__________ (填化学式)。
(2)实验室制取氨气的化学方程式:__________________________________
(3)1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是______________ ;
(4)实验室制Fe(OH)2一般看不到白色的Fe(OH)2沉淀,原因___________________ 现象是:_________________________ 。反应的化学方程式:__________________________________
(5)碳酸钠水解反应的离子方程式(第一步):_________________________ 。
(6)铅蓄电池的负极反应式:_________________________ 。
(7)硫酸钡的沉淀溶解平衡:__________________________________ 。
(2)实验室制取氨气的化学方程式:
(3)1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是
(4)实验室制Fe(OH)2一般看不到白色的Fe(OH)2沉淀,原因
(5)碳酸钠水解反应的离子方程式(第一步):
(6)铅蓄电池的负极反应式:
(7)硫酸钡的沉淀溶解平衡:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】长颈漏斗的作用是_______ 。


您最近一年使用:0次
【推荐2】磷及其化合物有重要的用途,回答下列问题:
(1)工业上将磷酸钙、石英砂和碳粉混和在电弧炉中焙烧来制取白磷,配平方程式:
______  +
+______  +
+______ 
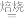
______ 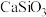 +
+______  +
+______  。
。
(2)白磷易自燃,保存的方法是__________________ ,白磷有毒,皮肤上沾有少量的白磷,可以用硫酸铜溶液处理,发生的反应是: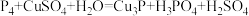 ,该反应的氧化剂是
,该反应的氧化剂是________________________ (填化学式)。
(3) 俗称为膦,电子式为:
俗称为膦,电子式为:________________________ ,沸点比较:
__________  (填”“高于”或“低于”)。
(填”“高于”或“低于”)。
(4)P2O5是常见的气体干燥剂,下列气体能用它干燥的是_______________ 。
A B
B C SO2 D CO2
C SO2 D CO2
也可以发生反应: ,该反应中
,该反应中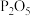 表现的性质是
表现的性质是_________ 。
(1)工业上将磷酸钙、石英砂和碳粉混和在电弧炉中焙烧来制取白磷,配平方程式:
 +
+ +
+
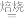
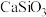 +
+ +
+ 。
。(2)白磷易自燃,保存的方法是
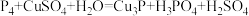 ,该反应的氧化剂是
,该反应的氧化剂是(3)
 俗称为膦,电子式为:
俗称为膦,电子式为:
 (填”“高于”或“低于”)。
(填”“高于”或“低于”)。(4)P2O5是常见的气体干燥剂,下列气体能用它干燥的是
A
 B
B C SO2 D CO2
C SO2 D CO2也可以发生反应:
 ,该反应中
,该反应中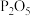 表现的性质是
表现的性质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列填空
(1)下列说法中,符合安全要求的是_______ (填序号)。
①在通风橱内做铜与氯气反应的实验
②实验中剩余的过氧化钠粉末用纸包裹好后,放入垃圾桶内
③闻氯气的气味时,用手轻轻在瓶口扇动,仅使极少量的氯气飘进鼻孔
④为了节约时间,锌与稀硫酸反应一开始有氢气放出,就直接做氢气点燃实验
(2)在进行钠的有关实验中,取用金属钠要用_______ ,用_______ 擦去表面的煤油,用_______ 切割绿豆粒大小的金属钠。若将金属钠投入硫酸铜溶液中,写出反应的化学方程式_______ 。
(3)将Na2O2投入紫色石蕊试液中,现象是_______
(4)向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。写出此过程中的化学方程式:_______ ;证明有Fe(OH)3胶体生成的最简单方法是_______ ;
(1)下列说法中,符合安全要求的是
①在通风橱内做铜与氯气反应的实验
②实验中剩余的过氧化钠粉末用纸包裹好后,放入垃圾桶内
③闻氯气的气味时,用手轻轻在瓶口扇动,仅使极少量的氯气飘进鼻孔
④为了节约时间,锌与稀硫酸反应一开始有氢气放出,就直接做氢气点燃实验
(2)在进行钠的有关实验中,取用金属钠要用
(3)将Na2O2投入紫色石蕊试液中,现象是
(4)向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。写出此过程中的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室常用下图所示装置制取NH3。

(1)NH4Cl和Ca(OH)2加热制取NH3的化学方程式是_______ 。
(2)图中方框内收集NH3的装置可选用“①”或“②”中的_______ 。
(3)若干燥NH3,不能选用浓硫酸,用化学方程式表示其原因:_______ 。

(1)NH4Cl和Ca(OH)2加热制取NH3的化学方程式是
(2)图中方框内收集NH3的装置可选用“①”或“②”中的
(3)若干燥NH3,不能选用浓硫酸,用化学方程式表示其原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(一)我国利用海水制盐具有悠久的历史。目前,从海水中制得的氯化钠除食用外,还是重要的工业原料,从海水中生产金属钠流程如下。

请回答:
(1)③中反应的化学方程式是_____________________ 。
(2)若为了得到精盐,除去粗盐中含有杂质泥沙、Mg2+、Ca2+、SO42-等,则制备精盐的正确的操作顺序是________ (填字母)。
a.将粗盐溶解 b.过滤 c.蒸发 d.加入过量的碳酸钠溶液 e.加入过量的氯化钡溶液f. 加入过量的氢氧化钠溶液 g. 加入盐酸,调溶液的pH略大于7
(3)在(2)中d操作的目的是______________________ 。
(4)若要制备2.3吨金属钠,理论上需要含质量分数为90%氯化钠的粗盐的质量是___ 吨。
(二)甲、乙、丙三位同学分别用如下三套实验装置及化学药品(其中碱石灰为固体氢氧化钠和生石灰的混合物)制取氨气。请你参与探究,并回答下列问题:

(1)三位同学制取氨气的化学方程式是:_________________ 。
(2)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨气(实验操作都正确),你认为没有收集到氨气的同学是______ (填“甲”、“乙”或“丙”)。
(3)为确定试管内是否已收集满氨气,应将湿润的红色石蕊试纸置于收集气体的试管口处,若观察到____________________ ,则说明氨气已收集满。
(4)三位同学都认为他们的实验装置还可用于加热碳酸氢铵固体来制取纯净的氨气,你判断能够达到实验目的的同学是______ (填“甲”、“乙”或“丙”)。

请回答:
(1)③中反应的化学方程式是
(2)若为了得到精盐,除去粗盐中含有杂质泥沙、Mg2+、Ca2+、SO42-等,则制备精盐的正确的操作顺序是
a.将粗盐溶解 b.过滤 c.蒸发 d.加入过量的碳酸钠溶液 e.加入过量的氯化钡溶液f. 加入过量的氢氧化钠溶液 g. 加入盐酸,调溶液的pH略大于7
(3)在(2)中d操作的目的是
(4)若要制备2.3吨金属钠,理论上需要含质量分数为90%氯化钠的粗盐的质量是
(二)甲、乙、丙三位同学分别用如下三套实验装置及化学药品(其中碱石灰为固体氢氧化钠和生石灰的混合物)制取氨气。请你参与探究,并回答下列问题:

(1)三位同学制取氨气的化学方程式是:
(2)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨气(实验操作都正确),你认为没有收集到氨气的同学是
(3)为确定试管内是否已收集满氨气,应将湿润的红色石蕊试纸置于收集气体的试管口处,若观察到
(4)三位同学都认为他们的实验装置还可用于加热碳酸氢铵固体来制取纯净的氨气,你判断能够达到实验目的的同学是
您最近一年使用:0次








