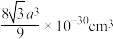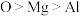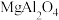X、Y、Z、W、P五种元素,其核电荷数依次增大。X基态原子核外只有三个能级,且各能级电子数相等;Z原子的核外电子有8种运动状态;Z与W元素位于同一族;P原子核外有4个能层,最外层只有1个电子,其余各层均排满电子。下列说法正确的是
| A.Z、Y、X元素的第一电离能依次减小 |
B.Y基态原子的轨道表示式: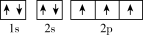 |
C.P原子的价层电子排布为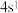 |
| D.P单质分别与Z、W单质反应,产物中P的化合价一定相同 |
2023·湖南怀化·二模 查看更多[4]
湖南省怀化市2023届高三下学期二模仿真考试化学试题江苏省扬州中学2023届高三下学期考前练习化学试题(已下线)考点41 原子结构与性质(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)原子结构与性质
更新时间:2023-04-23 11:18:48
|
相似题推荐
【推荐1】短周期主族元素X、Y、Z、W的原子序数依次增大。Z原子2p轨道上有3个未成对电子。甲、乙、丙、丁、戊是这四种元素之间形成的化合物,75%的甲溶液常用于消毒,戊是Z和X组成的10电子分子,常温下己溶液显中性,它们有如下转化关系:
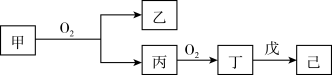
则下列说法中错误的是

则下列说法中错误的是
| A.四种元素原子半径由大到小的顺序为:Y>Z>W>X |
| B.W的氢化物中的某种具有漂白性 |
| C.己溶液中阴离子浓度之和等于阳离子浓度之和 |
| D.W的氢化物沸点一定比Y的氢化物沸点高 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】短周期主族元素W、X、Y、Z的原子序数依次增大,四种元素可以组成一种分子簇,其分子结构如图所示(球大小表示原子半径的相对大小),W、X位于不同周期,X原子的最外层电子数是次外层电子数的3倍,Z的族序数等于其周期数,下列说法中一定正确的是
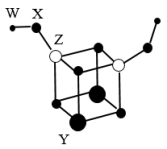

| A.X可以分别与W、Y可形成化合物W2X2、Y2X2 |
| B.工业上获得Y、Z单质均可采用电解它们的熔融氯化物 |
| C.简单离子半径: Z>Y>X>W |
| D.相同条件下,Y单质的沸点比Z单质的低 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】W、X、Y、Z、R为原子序数依次增大的短周期主族元素,W元素的一种核素可用于鉴定文物年代,X元素的一种单质可作为饮用水消毒剂,Y元素的简单离子是同周期元素的简单离子中半径最小的,Z 元素和 W 元素同主族,R元素可形成黄绿色气体单质。下列说法错误的是
| A.W元素和X元素形成的化合物WX属于极性分子 |
| B.X元素与Y元素可形成阴阳离子个数比为1:2的化合物 |
| C.制造日常生活中所使用的计算机芯片需要消耗大量单质Z |
| D.X元素和R元素形成的某种化合物可用于自来水的消毒 |
您最近一年使用:0次
【推荐1】砷化镓(GaAs)作为第二代半导体材料的代表,是目前研究最成熟、生产量最大的半导体材料。GaAs晶胞结构如图所示,晶胞边长为apm,下列说法正确的是
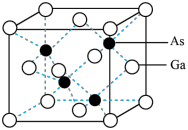

| A.GaAs属于离子晶体 |
B.基态砷原子价电子排布图为 |
| C.As的配位数为4 |
D.该晶体密度为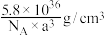 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】从微粒结构角度分析,下列说法正确的是
| A.OF2与H2O的立体构型同为V形,因氧与氢的电负性差大于氧与氟的电负性差,而且OF2中氧原子上有两对孤电子对,抵消了F-O键中共用电子对偏向F而产生的极性,所以水分子的极性比OF2的极性小 |
| B.过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般d0或d10排布无颜色,d1~d9排布有颜色。据此判断[Co(H2O)6]2+和[Mn(H2O)6]2+中只有一种有颜色 |
C.三氧化硫有单分子气体和三聚分子固体(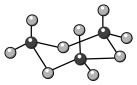 )两种存在形式,两种形式中S原子的杂化轨道类型相同 )两种存在形式,两种形式中S原子的杂化轨道类型相同 |
D.南京理工大学化工学院胡炳成教授团队成功合成世界首个全氮阴离子盐,其局部结构如图所示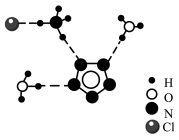 ,其中两种阳离子中心原子的杂化轨道类型相同,阴离子N ,其中两种阳离子中心原子的杂化轨道类型相同,阴离子N 中所有的氮原子在同一平面内 中所有的氮原子在同一平面内 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列说法不正确 的是
| A.某外围电子排布为4f75d16s2基态原子,该元素位于周期表中第六周期第ⅢB族 |
| B.在元素周期表中,s区,d区和ds区的元素都是金属元素 |
C.当碳原子的核外电子排布由 转变为 转变为 时,释放能量,由激发态转化成基态 时,释放能量,由激发态转化成基态 |
| D.非金属元素形成的共价化合物中,原子的最外层电子数不一定是2或8 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】下列有关化学用语表述或性质比较正确的是
A.基态氧原子核外价电子排布轨道表示式 |
| B.基态氧原子核外有8种空间运动状态的电子 |
C.用原子轨道描述氢分子中化学键的形成: |
| D.第三周期的元素中,第一电离能介于Mg和S之间只有1种元素 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】CoxNi(1-x)Fe2O4在磁性材料和催化剂领域具有广泛的应用前景,Co3+可以形成配合物[Co(NH2—CH2—CH2—NH2)(NH3)2Cl2]Cl。下列说法不正确的是
A.第四周期中不成对电子数目最多的基态原子的价电子轨道表示式为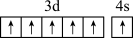 |
| B.CoxNi(1-x)Fe2O4中Co、Ni的化合价都是+2,则Fe的化合价是+3 |
| C.乙二胺与三甲胺[N(CH3)3]均属于胺,乙二胺的沸点比三甲胺高的原因是乙二胺分子间可以形成氢键,而三甲胺却形成了分子内氢键 |
| D.该配合物中Co3+的配位数是6 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】X、Y、Z、W、Q均为短周期元素、在元素周期表中的相对位置如图所示;Q的最高价氧化物的水化物是一种二元酸。
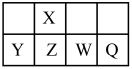
下列说法正确的是

下列说法正确的是
| A.第一电离能:W>Q>Z | B.X与氢元素能组成直线型分子 |
| C.X、Z元素形成的单质晶体类型一定相同 | D.Q元素的两种常见氧化物分子里键角相同 |
您最近一年使用:0次
【推荐2】离子化合物 由四种原子序数依次增大的短周期主族元素W、X、Y、Z组成,其中阴、阳离子均由两种元素组成且均呈正四面体形。四种元素的原子序数之和为21,且W、Z元素的基态原子核外均只有1个未成对电子。下列说法错误的是
由四种原子序数依次增大的短周期主族元素W、X、Y、Z组成,其中阴、阳离子均由两种元素组成且均呈正四面体形。四种元素的原子序数之和为21,且W、Z元素的基态原子核外均只有1个未成对电子。下列说法错误的是
 由四种原子序数依次增大的短周期主族元素W、X、Y、Z组成,其中阴、阳离子均由两种元素组成且均呈正四面体形。四种元素的原子序数之和为21,且W、Z元素的基态原子核外均只有1个未成对电子。下列说法错误的是
由四种原子序数依次增大的短周期主族元素W、X、Y、Z组成,其中阴、阳离子均由两种元素组成且均呈正四面体形。四种元素的原子序数之和为21,且W、Z元素的基态原子核外均只有1个未成对电子。下列说法错误的是| A.第一电离能:Y>Z>X | B.原子半径:X>Y>Z |
C.键角: | D. 的化学式: 的化学式: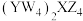 |
您最近一年使用:0次

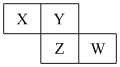
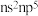
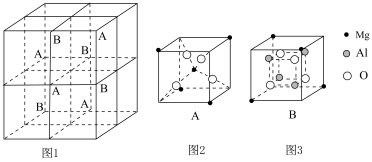
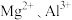 和
和 在小立方体中的分布如图2、图3所示。已知
在小立方体中的分布如图2、图3所示。已知 之间的最小间距为
之间的最小间距为 。下列说法错误的是
。下列说法错误的是