硫是重要的非金属元素,也是人类较早认识的化学元素之一。人们对硫元素的利用,其本质就是通过各种化学反应,实现含硫元素的物质之间的转化。
(1)硫可以形成分子式为 、
、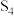 、
、 、
、 的单质,其中
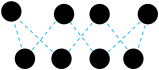
的单质,其中 的分子球棍模型如图所示。下列有关说法正确的是_______。
的分子球棍模型如图所示。下列有关说法正确的是_______。
(2)将 气体通入
气体通入 溶液中,没有看到明显现象,再遇入一种气体(或加入一种物质)后,可产生一种沉淀,该气体(或物质)不可能是_______。
溶液中,没有看到明显现象,再遇入一种气体(或加入一种物质)后,可产生一种沉淀,该气体(或物质)不可能是_______。
(3)用如图所示实验装置(部分夹持仪器已略去)探究铜丝与过量浓硫酸的反应。
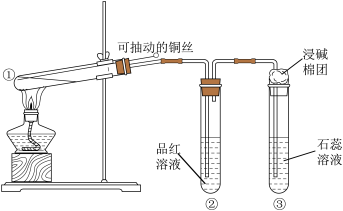
下列实验或说法不合理的是_______。
(4)工业上制备硫酸铜是利用废铜屑经灼烧后,在加热情况下跟稀硫酸反应,有关的化学方程式是_______ 。不采用铜跟浓硫酸反应来制取硫酸铜的原因是_______ 。
(5)在 溶液中滴加少量
溶液中滴加少量 溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移的方向和数目
溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移的方向和数目_______ 。
_______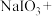 _______
_______ _______
_______ _______
_______ _______
_______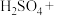 _______
_______
(6)中华人民共和国国家标准(G2762022)规定葡萄酒中 最大使用量为0.25 g⋅L-1,取300.00 mL葡萄酒,通过适当的方法使所含
最大使用量为0.25 g⋅L-1,取300.00 mL葡萄酒,通过适当的方法使所含 全部逸出并用
全部逸出并用 将其全部氧化为
将其全部氧化为 ,消耗浓度为0.0900 mol•L-1NaOH标准溶液25mL,该葡萄酒中
,消耗浓度为0.0900 mol•L-1NaOH标准溶液25mL,该葡萄酒中 含量为
含量为_______ g·L-1。
(7)同学们继续设计实验探究亚硫酸与次氯酸的酸性强弱:甲同学查阅资料得知 为难溶于水的白色沉淀,因此设计了实验方案为:将
为难溶于水的白色沉淀,因此设计了实验方案为:将 通入漂白粉溶液中,若观察到有白色沉淀生成,说明发生反应
通入漂白粉溶液中,若观察到有白色沉淀生成,说明发生反应
 ,则证明亚硫酸性强于次氯酸。乙同学分为甲同学方案的反应原理是错误的,理由是
,则证明亚硫酸性强于次氯酸。乙同学分为甲同学方案的反应原理是错误的,理由是_______ 。
(1)硫可以形成分子式为
 、
、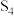 、
、 、
、 的单质,其中
的单质,其中 的分子球棍模型如图所示。下列有关说法正确的是_______。
的分子球棍模型如图所示。下列有关说法正确的是_______。
A.1 mol  单质中含有的S—S键个数为 单质中含有的S—S键个数为 |
B. 、 、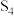 、 、 、 、 互为同位素 互为同位素 |
C.硫的单质在足量的空气中完全燃烧可生成 |
D. 的摩尔质量为32 g/mol 的摩尔质量为32 g/mol |
 气体通入
气体通入 溶液中,没有看到明显现象,再遇入一种气体(或加入一种物质)后,可产生一种沉淀,该气体(或物质)不可能是_______。
溶液中,没有看到明显现象,再遇入一种气体(或加入一种物质)后,可产生一种沉淀,该气体(或物质)不可能是_______。A. | B. | C. | D. |

下列实验或说法不合理的是_______。
A.上下移动①中铜丝可控制 的量 的量 |
B.②中品红溶液是验证 的生成 的生成 |
| C.③中石蕊溶液先变红后褪色 |
D.为确认 生成,向①中加水,观察颜色 生成,向①中加水,观察颜色 |
(5)在
 溶液中滴加少量
溶液中滴加少量 溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移的方向和数目
溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移的方向和数目_______
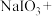 _______
_______ _______
_______ _______
_______ _______
_______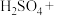 _______
_______
(6)中华人民共和国国家标准(G2762022)规定葡萄酒中
 最大使用量为0.25 g⋅L-1,取300.00 mL葡萄酒,通过适当的方法使所含
最大使用量为0.25 g⋅L-1,取300.00 mL葡萄酒,通过适当的方法使所含 全部逸出并用
全部逸出并用 将其全部氧化为
将其全部氧化为 ,消耗浓度为0.0900 mol•L-1NaOH标准溶液25mL,该葡萄酒中
,消耗浓度为0.0900 mol•L-1NaOH标准溶液25mL,该葡萄酒中 含量为
含量为(7)同学们继续设计实验探究亚硫酸与次氯酸的酸性强弱:甲同学查阅资料得知
 为难溶于水的白色沉淀,因此设计了实验方案为:将
为难溶于水的白色沉淀,因此设计了实验方案为:将 通入漂白粉溶液中,若观察到有白色沉淀生成,说明发生反应
通入漂白粉溶液中,若观察到有白色沉淀生成,说明发生反应
 ,则证明亚硫酸性强于次氯酸。乙同学分为甲同学方案的反应原理是错误的,理由是
,则证明亚硫酸性强于次氯酸。乙同学分为甲同学方案的反应原理是错误的,理由是
22-23高一下·上海宝山·期中 查看更多[2]
更新时间:2023-04-15 17:46:34
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】钪的价格昂贵,在地壳里的含量只有0.0005%。从铝土矿生产Al2O3的副产品“赤泥”(主要成分为Al2O3、Fe2O3、TiO2、Sc2O3)中回收钪,同时生产聚合硫酸铁铝[AlFe(OH)6-2n(SO4)n]具有极其重要的工业价值,一种工艺流程如下:
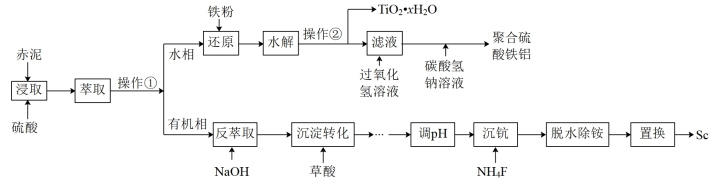
已知:钪离子可以在不同pH下生成[Sc(OH)n] 3-n(n=1~6)。
“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O 分解得到ScF3,某固体样品质量与温度的关系如图所示。加热至 380-400℃产生白烟,400℃以上质量不再改变。则a=_______ (填数字)。
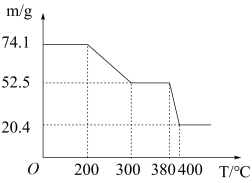

已知:钪离子可以在不同pH下生成[Sc(OH)n] 3-n(n=1~6)。
“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O 分解得到ScF3,某固体样品质量与温度的关系如图所示。加热至 380-400℃产生白烟,400℃以上质量不再改变。则a=

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】胆矾(CuSO4·5H2O)易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的CuO(杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:
结晶水测定:称量干燥坩埚的质量为m1,加入胆矾后总质量为m2,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为m3.根据实验数据,胆矾分子中结晶水的个数为_______ (写表达式)。
结晶水测定:称量干燥坩埚的质量为m1,加入胆矾后总质量为m2,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为m3.根据实验数据,胆矾分子中结晶水的个数为
您最近一年使用:0次
【推荐1】回答下列问题:
(1)在S2-、Fe3+、Fe2+、Mg2+、S、I-、H+中,只有氧化性的是___________ ,只有还原性的是___________ ,既有氧化性又有还原性的是___________ 。
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3 N2O3+H2O
N2O3+H2O
②N2O4+H2O HNO3+HNO2
HNO3+HNO2
③NH3+NO HNO2+H2O
HNO2+H2O
其中你认为一定不可能实现的是___________ (填序号)。
(3)下列三个氧化还原反应中:
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2NaClO3+4HCl(浓)=2NaCl+2ClO2↑+Cl2↑+2H2O
双线桥标出反应②的电子转移方向和数目:___________ ;反应③中的还原产物___________ ;
若溶质中Cl-与I-共存,为了氧化I-而Cl-不被氧化,除单质外,还可选用上述反应中的___________ 做氧化剂。
(1)在S2-、Fe3+、Fe2+、Mg2+、S、I-、H+中,只有氧化性的是
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3
 N2O3+H2O
N2O3+H2O②N2O4+H2O
 HNO3+HNO2
HNO3+HNO2③NH3+NO
 HNO2+H2O
HNO2+H2O其中你认为一定不可能实现的是
(3)下列三个氧化还原反应中:
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2NaClO3+4HCl(浓)=2NaCl+2ClO2↑+Cl2↑+2H2O
双线桥标出反应②的电子转移方向和数目:
若溶质中Cl-与I-共存,为了氧化I-而Cl-不被氧化,除单质外,还可选用上述反应中的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)酸碱质子理论认为,能电离出质子的物质都是酸,能结合质子的物质是碱,用一个离子方程式说明CO 与AlO
与AlO 的碱性强弱
的碱性强弱____ 。
(2)高铁酸盐(K2FeO4)是公认的绿色消毒净水剂,请简要解释其原理____ 。
(1)酸碱质子理论认为,能电离出质子的物质都是酸,能结合质子的物质是碱,用一个离子方程式说明CO
 与AlO
与AlO 的碱性强弱
的碱性强弱(2)高铁酸盐(K2FeO4)是公认的绿色消毒净水剂,请简要解释其原理
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】阅读下面两条科普信息,回答有关问题:
一个体重50kg的健康人身体中含铁2g,这2g铁在人体中不是以金属单质的形式存在,而是以Fe2+和Fe3+的形式存在,亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
在新生代的海水里有一种铁细菌,它们提取海水中的亚铁离子,利用酶为催化剂把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉积下来形成铁矿:该反应的另一种反应物是CO2,反应后CO2转变成有机物(用甲醛CH2O表示)。
(1)这两则科普信息分别介绍了人体内和海水中的亚铁离子与铁离子(或者铁的高价化合物)相互转化的事实,方法和途径。这说明维生素C具有_______ 性,铁离子具有_______ 性,第二则则信息中CO2是_______ 剂。
(2)铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+离子。制取铁酸钠的化学方程式如下:Fe(NO3)3+NaOH+Cl2→Na2FeO4+NaNO3+NaCl+H2O
配平上述反应_______ ,并分析_____ 元素被氧化,当生成3mol还原产物时,转移电子的总数为_______ 。
一个体重50kg的健康人身体中含铁2g,这2g铁在人体中不是以金属单质的形式存在,而是以Fe2+和Fe3+的形式存在,亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
在新生代的海水里有一种铁细菌,它们提取海水中的亚铁离子,利用酶为催化剂把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉积下来形成铁矿:该反应的另一种反应物是CO2,反应后CO2转变成有机物(用甲醛CH2O表示)。
(1)这两则科普信息分别介绍了人体内和海水中的亚铁离子与铁离子(或者铁的高价化合物)相互转化的事实,方法和途径。这说明维生素C具有
(2)铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+离子。制取铁酸钠的化学方程式如下:Fe(NO3)3+NaOH+Cl2→Na2FeO4+NaNO3+NaCl+H2O
配平上述反应
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】元素在周期表中的位置反映了元素的原子结构和元素的性质。如图是元素周期表的一部分。回答下列问题:
(1)N在元素周期表中的位置为第__________ 周期__________ 族。根据元素周期律,预测酸性强弱:
______ (填“>”或“<”) 。
。
(2)S的最高化合价和最低化合价的代数和为_______ ,Se与 的反应比S与
的反应比S与 的反应
的反应______ (填“难”或“易”)。
(3) 具有较强的氧化性,
具有较强的氧化性, 具有较强的还原性,将
具有较强的还原性,将 气体通入溴水后,溶液中主要存在的离子是
气体通入溴水后,溶液中主要存在的离子是________ (填离子符号)。
(4)下列说法错误的是___________ (填序号)。
①C、N、O、F的原子半径随着原子序数的增大而减小
②Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
③由元素周期律可直接推断出酸性:
④HF、HCl、HBr、HI的稳定性逐渐减弱
| C | N | O | F | ||
| Si | P | S | Cl | ||
| Ge | As | Se | Br | ||
| Sn | Sb | Te | I | ||
| Pb | Bi | Po | At |

 。
。(2)S的最高化合价和最低化合价的代数和为
 的反应比S与
的反应比S与 的反应
的反应(3)
 具有较强的氧化性,
具有较强的氧化性, 具有较强的还原性,将
具有较强的还原性,将 气体通入溴水后,溶液中主要存在的离子是
气体通入溴水后,溶液中主要存在的离子是(4)下列说法错误的是
①C、N、O、F的原子半径随着原子序数的增大而减小
②Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
③由元素周期律可直接推断出酸性:

④HF、HCl、HBr、HI的稳定性逐渐减弱
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】非金属元素在生产生活中扮演着重要角色。请根据题意填空;
(1)氨是一种极易溶于水的气体,其水溶液能使酚酞溶液变_______ (填“红”或“蓝”);
(2)SO2有一定的还原性,在葡萄酒的酿制过程中,添加适量的SO2,除可杀菌外,还可防止葡萄酒中的一些成分被_______ (填“氧化”或“还原”),起到保质作用;
(3)玻璃中的成分SiO2能与NaOH溶液反应: ,实验室中盛放NaOH溶液应选用带
,实验室中盛放NaOH溶液应选用带_______ (填“玻璃塞”或“橡胶塞”)的试剂瓶。
(1)氨是一种极易溶于水的气体,其水溶液能使酚酞溶液变
(2)SO2有一定的还原性,在葡萄酒的酿制过程中,添加适量的SO2,除可杀菌外,还可防止葡萄酒中的一些成分被
(3)玻璃中的成分SiO2能与NaOH溶液反应:
 ,实验室中盛放NaOH溶液应选用带
,实验室中盛放NaOH溶液应选用带
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】为了探究三种气态氧化物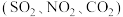 的性质,某同学设计了一组实验:用三只集气瓶收集满二氧化硫或二氧化氮气体,然后将其倒置在水槽中。分别缓慢通入适量
的性质,某同学设计了一组实验:用三只集气瓶收集满二氧化硫或二氧化氮气体,然后将其倒置在水槽中。分别缓慢通入适量 或
或 ,如图D、E、F所示。一段时间后,D、E装置的集气瓶中充满溶液,F装置的集气瓶中还有气体剩余。(假设瓶内液体不扩散):
,如图D、E、F所示。一段时间后,D、E装置的集气瓶中充满溶液,F装置的集气瓶中还有气体剩余。(假设瓶内液体不扩散):
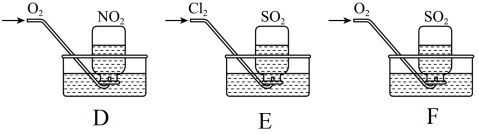
(1)通入氧气前D烧杯中发生反应的化学方程式:_______ 。
(2)写出通入 后装置E中反应的离子方程式:
后装置E中反应的离子方程式:_______ 。
(3)在F的水槽里滴加几滴紫色石蕊试液,将收集满二氧化硫的集气瓶倒置在水槽中,观察到的现象是_______ ,写出通入 后装置F中反应的化学方程式
后装置F中反应的化学方程式_______ 。
(4)假设该实验条件为标况,则装置D的集气瓶中最终所得溶液溶质的物质的量浓度为_______  。
。
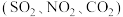 的性质,某同学设计了一组实验:用三只集气瓶收集满二氧化硫或二氧化氮气体,然后将其倒置在水槽中。分别缓慢通入适量
的性质,某同学设计了一组实验:用三只集气瓶收集满二氧化硫或二氧化氮气体,然后将其倒置在水槽中。分别缓慢通入适量 或
或 ,如图D、E、F所示。一段时间后,D、E装置的集气瓶中充满溶液,F装置的集气瓶中还有气体剩余。(假设瓶内液体不扩散):
,如图D、E、F所示。一段时间后,D、E装置的集气瓶中充满溶液,F装置的集气瓶中还有气体剩余。(假设瓶内液体不扩散):
(1)通入氧气前D烧杯中发生反应的化学方程式:
(2)写出通入
 后装置E中反应的离子方程式:
后装置E中反应的离子方程式:(3)在F的水槽里滴加几滴紫色石蕊试液,将收集满二氧化硫的集气瓶倒置在水槽中,观察到的现象是
 后装置F中反应的化学方程式
后装置F中反应的化学方程式(4)假设该实验条件为标况,则装置D的集气瓶中最终所得溶液溶质的物质的量浓度为
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某些化学反应可表示为: .请回答下列问题:
.请回答下列问题:
(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式_______
(2)若气体D能使湿润的红色石蕊试纸变蓝,写出该反应的化学方程式_______
(3)若A是金属单质,C是遇空气会变为红棕色的无色气体,写出该反应的离子方程式_______
(4)若C、D均为能使澄清石灰水变浑浊的气体,且D可以使品红褪色,则A与B反应的化学方程式为_______
 .请回答下列问题:
.请回答下列问题:(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式
(2)若气体D能使湿润的红色石蕊试纸变蓝,写出该反应的化学方程式
(3)若A是金属单质,C是遇空气会变为红棕色的无色气体,写出该反应的离子方程式
(4)若C、D均为能使澄清石灰水变浑浊的气体,且D可以使品红褪色,则A与B反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某化学学习小组设计通过以下步骤用铜丝和硫酸制取胆矾晶体:

(1)固体A为___ 色;胆矾的化学式为___ 。
(2)为加快反应②,可采取的实验方法是___ (写出一种即可)。
(3)操作①、操作②的具体实验操作名称是___ 。
(4)有同学提出可以将反应①和反应②合并,也就是将铜丝与浓硫酸直接混合加热即可得到蓝色溶液。该同学所提方案不足之处是__ (写出一种即可)。

(1)固体A为
(2)为加快反应②,可采取的实验方法是
(3)操作①、操作②的具体实验操作名称是
(4)有同学提出可以将反应①和反应②合并,也就是将铜丝与浓硫酸直接混合加热即可得到蓝色溶液。该同学所提方案不足之处是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.从以下试剂中选择合适的试剂实现转化的方程式。
试剂清单:①浓H2SO4 ②Na2S溶液 ③酸性KMnO4溶液 ④H2SO3溶液 ⑤木炭
(1)S(+4)→S(+6)离子方程式_______ 。
(2)S(+6)→S(+4)化学方程式_______ 。
II.下列溶液或用品中:
①澄清石灰水;②H2S溶液;③酸性KMnO4溶液;④溴水;⑤Ba(NO3)2溶液;⑥品红溶液;⑦湿润的蓝色石蕊试纸。不能区别SO2和CO2气体的是________ 。
A.①⑤⑦ B.①⑤ C.①⑦ D.②③④⑤⑥
若将过量的SO2通入澄清石灰水中,写出反应的离子方程式_______
III.工业上常用纯碱液来吸收NOx,有关反应的化学方程式为2NO2+Na2CO3=NaNO2+NaNO3+CO2、NO2+NO+Na2CO3=2NaNO2+CO2,现有aLNO2和bLNO的混合气体(气体体积已经换算成标准状况下)恰好被200mLNa2CO3溶液完全吸收,则a、b应满足的关系为_______ 。Na2CO3溶液的物质的量浓度为_______ mol·L-1。
试剂清单:①浓H2SO4 ②Na2S溶液 ③酸性KMnO4溶液 ④H2SO3溶液 ⑤木炭
(1)S(+4)→S(+6)离子方程式
(2)S(+6)→S(+4)化学方程式
II.下列溶液或用品中:
①澄清石灰水;②H2S溶液;③酸性KMnO4溶液;④溴水;⑤Ba(NO3)2溶液;⑥品红溶液;⑦湿润的蓝色石蕊试纸。不能区别SO2和CO2气体的是
A.①⑤⑦ B.①⑤ C.①⑦ D.②③④⑤⑥
若将过量的SO2通入澄清石灰水中,写出反应的离子方程式
III.工业上常用纯碱液来吸收NOx,有关反应的化学方程式为2NO2+Na2CO3=NaNO2+NaNO3+CO2、NO2+NO+Na2CO3=2NaNO2+CO2,现有aLNO2和bLNO的混合气体(气体体积已经换算成标准状况下)恰好被200mLNa2CO3溶液完全吸收,则a、b应满足的关系为
您最近一年使用:0次



