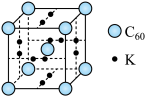
科学家把C60和K掺杂在一起制造出的化合物具有超导性能,其晶胞如图所示。该化合物中的K原子和C60分子的个数比为______ 。

2023高三·全国·专题练习 查看更多[1]
(已下线)04 常考题空4 晶体化学式及粒子数确定 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
更新时间:2023-04-25 15:07:05
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图表示两种晶体的微观结构:
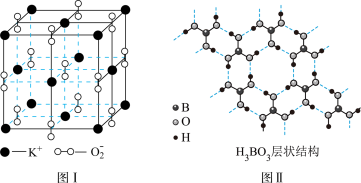
试回答下列有关问题:
(1)高温下,超氧化钾晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。图I为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则晶体中,与每个K+距离最近的K+有_________ 个,0价氧原子与-2价氧原子的数目比为_________ ;
(2)正硼酸(H3BO3)是一种片层结构的白色晶体,层内的H3BO3分子通过氢键相连(如图II)。下列有关说法正确的有_________ 。
①正硼酸晶体属于原子晶体
②H3BO3分子的稳定性与氢键有关
③在H3BO3分子中各原子未能都满足8e-稳定结构
④含1molH3BO3的晶体中有3mol氢键
⑤含1molH3BO3的晶体中有3mol极性共价键
⑥晶体中每个B与相邻的3个O共平面

试回答下列有关问题:
(1)高温下,超氧化钾晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。图I为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则晶体中,与每个K+距离最近的K+有
(2)正硼酸(H3BO3)是一种片层结构的白色晶体,层内的H3BO3分子通过氢键相连(如图II)。下列有关说法正确的有
①正硼酸晶体属于原子晶体
②H3BO3分子的稳定性与氢键有关
③在H3BO3分子中各原子未能都满足8e-稳定结构
④含1molH3BO3的晶体中有3mol氢键
⑤含1molH3BO3的晶体中有3mol极性共价键
⑥晶体中每个B与相邻的3个O共平面
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
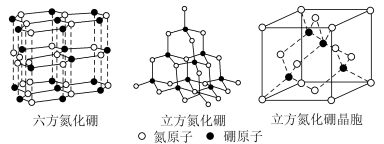
【推荐2】六方氮化硼的结构与石墨类似,B-N共价单键的键长理论值为158 pm,而六方氮化硼层内B、N原子间距的实测值为145 pm,造成这一差值的原因是___________ 。高温高压下,六方氮化硼可转化为立方氮化硼,立方氮化硼的结构与金刚石类似,已知晶胞参数中边长为a=362pm,则立方氮化硼的密度是___________ g/cm3

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)Fe基态原子核外电子排布式为_____________________ 。
(2)H、N、O的电负性从小到大的顺序是___________________ 。
(3)与 互为等电子体的一种分子为
互为等电子体的一种分子为______________ (填化学式)。
氨基(-NH2)中氮原子的杂化类型为_________________ 。
(4)1mol乙酸分子中含有σ键的数目为____________________ 。
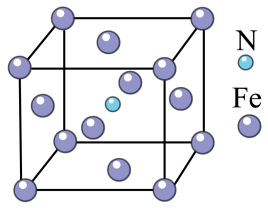
(5)Fe与N形成的某化合物晶胞如图所示,则该晶体的化学式为_______________ 。
(2)H、N、O的电负性从小到大的顺序是
(3)与
 互为等电子体的一种分子为
互为等电子体的一种分子为氨基(-NH2)中氮原子的杂化类型为
(4)1mol乙酸分子中含有σ键的数目为
(5)Fe与N形成的某化合物晶胞如图所示,则该晶体的化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】锌是一种重要的金属,锌及其化合物有着广泛的应用。
(1)葡萄糖酸锌[CH2OH(CHOH4COO)2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式______________________ ;葡萄糖[CH2OH(CHOH)4CHO]分子中碳原子杂化方式是_________________________ 。
(2)Zn2+也能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子空间构型为______ ;在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在下图中
表示[Zn(NH3)4]2+中Zn2+与N之间的化学键_______ 。

(3)下图表示锌与某种元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为_______ ;该化合物的晶体熔点比干冰高得多,原因是_____ 。
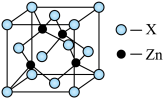
(1)葡萄糖酸锌[CH2OH(CHOH4COO)2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式
(2)Zn2+也能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子空间构型为
表示[Zn(NH3)4]2+中Zn2+与N之间的化学键

(3)下图表示锌与某种元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)Cu的价电子排布图______ ,钾的最高能层符号______ 。
(2)NH3在水中的溶解度大于H2S在水中的溶解度其原因是______ 。
(3)用“>、<、=”来比较下列晶体的熔沸点。
CaO______ MgO HF______ HCl Si______ SiC K______ Ti
(4)某金属晶体堆积方式为面心立方堆积,其配位数为______ ;一个该金属晶胞中含有______ 个该金属原子。
(5)NH3与NH4+的键角大小,NH3______ NH4+(用“>、<、=”比较),原因是______ 。
(2)NH3在水中的溶解度大于H2S在水中的溶解度其原因是
(3)用“>、<、=”来比较下列晶体的熔沸点。
CaO
(4)某金属晶体堆积方式为面心立方堆积,其配位数为
(5)NH3与NH4+的键角大小,NH3
您最近一年使用:0次

 的结构为体心立方堆积,晶胞参数为a pm,
的结构为体心立方堆积,晶胞参数为a pm, 

