磷酸铁锂( )是一种重要的锂离子电池正极材料。
)是一种重要的锂离子电池正极材料。
(1) 的晶胞结构示意图如图-1所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。
的晶胞结构示意图如图-1所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。
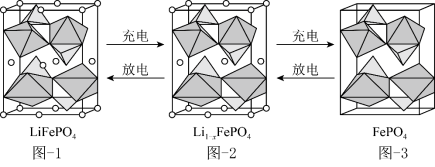
①图-1、图-2中小球表示的是___________ (填微粒符号)。
②图-1中每个晶胞中含有 的单元数有
的单元数有___________ 个。
(2)利用钛铁矿(主要成分为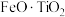 ,含有少量MgO、CaO、
,含有少量MgO、CaO、 等杂质)制备磷酸铁和锂离子电池正极材料(
等杂质)制备磷酸铁和锂离子电池正极材料( )的部分工业流程如图4所示:
)的部分工业流程如图4所示:
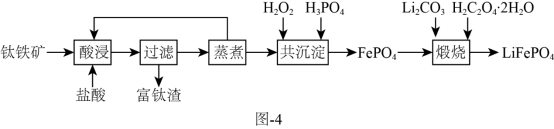
①基态 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为___________ 。
②磷酸根离子的空间构型为___________ 。
③1mol 分子中含有的σ键的数目为
分子中含有的σ键的数目为___________ 。
④煅烧得到 的化学方程式为
的化学方程式为___________ 。
⑤制备 的过程中,理论上所需17%双氧水与
的过程中,理论上所需17%双氧水与 的质量比为
的质量比为___________ 。
 )是一种重要的锂离子电池正极材料。
)是一种重要的锂离子电池正极材料。(1)
 的晶胞结构示意图如图-1所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。
的晶胞结构示意图如图-1所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。
①图-1、图-2中小球表示的是
②图-1中每个晶胞中含有
 的单元数有
的单元数有(2)利用钛铁矿(主要成分为
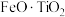 ,含有少量MgO、CaO、
,含有少量MgO、CaO、 等杂质)制备磷酸铁和锂离子电池正极材料(
等杂质)制备磷酸铁和锂离子电池正极材料( )的部分工业流程如图4所示:
)的部分工业流程如图4所示:
①基态
 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为②磷酸根离子的空间构型为
③1mol
 分子中含有的σ键的数目为
分子中含有的σ键的数目为④煅烧得到
 的化学方程式为
的化学方程式为⑤制备
 的过程中,理论上所需17%双氧水与
的过程中,理论上所需17%双氧水与 的质量比为
的质量比为
22-23高二下·全国·单元测试 查看更多[2]
(已下线)专题突破卷06 物质结构与性质?-2024年高考化学一轮复习考点通关卷(新教材新高考)第三章 晶体结构与性质(B卷·能力提升练)-2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修2)
更新时间:2023-04-28 13:38:00
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】CoP、FeS2、NiS2等物质对电化学氢析出反应有良好的催化活性和稳定性。请回答下列问题:
(1)基态Co原子价层电子的电子排布图(轨道表达式)为________________ ,基态P原子的电子占据最高能级的电子云轮廓图为_______ 。
(2)PH3的沸点_____ (填“高于”或“低于”)NH3,原因是______________ 。
(3)下图为白磷(P4)的晶胞示意图,晶胞的边长为a nm,设阿伏加 德罗常数的数值为NA,其晶体密度的计算表达式为______ g·cm-3。

(1)基态Co原子价层电子的电子排布图(轨道表达式)为
(2)PH3的沸点
(3)下图为白磷(P4)的晶胞示意图,晶胞的边长为a nm,设阿伏加 德罗常数的数值为NA,其晶体密度的计算表达式为

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】硫和碳及其化合物广泛存在于自然界中,并被人们广泛利用。回答下列问题:
(1)当基态原子的电子吸收能量后,电子会发生____ ,某处于激发态的S原子,其中1个3s电子跃迁到3p轨道中,该激发态S原子的核外电子排布式为__________ 。硫所在周期中,第一电离能最大的元素是___________ 。(填元素符号)
(2)写出一个与CO2具有相同空间结构和键合形式的分子的电子式__________________ 。
(3)H2S中S原子的杂化类型是__________ ;H2S的VSEPR模型名称为_________ ;H2S的键角约为94°,H2O的键角为105°,其原因是___________________________ 。
(4)科学家通过X射线推测胆矾结构示意图1如下:


其中含有________ 个配位键,___________ 个氢键。
(5)已知Zn和Hg同属IIB族元素,火山喷出的岩浆是一种复杂的混合物,冷却时,许多矿物相继析出,其中所含的ZnS矿物先于HgS矿物析出,原因是_________________________________ 。
(6)碳的另一种同素异形体—石墨,其晶体结构如上图2所示,虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数为____ 个,已知石墨的密度为pg·cm-1,C-C键长为rcm,阿伏伽德罗常数的值为NA,计算石墨晶体的层间距为____ cm。
(1)当基态原子的电子吸收能量后,电子会发生
(2)写出一个与CO2具有相同空间结构和键合形式的分子的电子式
(3)H2S中S原子的杂化类型是
(4)科学家通过X射线推测胆矾结构示意图1如下:


其中含有
(5)已知Zn和Hg同属IIB族元素,火山喷出的岩浆是一种复杂的混合物,冷却时,许多矿物相继析出,其中所含的ZnS矿物先于HgS矿物析出,原因是
(6)碳的另一种同素异形体—石墨,其晶体结构如上图2所示,虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:
(1)基态P原子的价电子排布式为___ 。
(2)磷的一种同素异形体——白磷(P4)的空间构型为___ ,其键角为__ ,推测其在CS2中的溶解度___ (填“大于”或“小于”)在水中的溶解度。
(3)膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试用价层电子对互斥理论分析PH3的键角小于NH3的原因:___ 。
(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A、B的化学式分别为___ 、__ ,A的中心原子杂化轨道类型为___ 。

(5)第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素是__ (填元素符号)。
(6)氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如下表所示。试从结构的角度分析它们熔点不同的原因:__ 。
(1)基态P原子的价电子排布式为
(2)磷的一种同素异形体——白磷(P4)的空间构型为
(3)膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试用价层电子对互斥理论分析PH3的键角小于NH3的原因:
(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A、B的化学式分别为

(5)第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素是
(6)氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如下表所示。试从结构的角度分析它们熔点不同的原因:
| 物质 | BN | AlN | GaN |
| 熔点/℃ | 3000 | 2200 | 1700 |
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】[化学——选修3:物质结构与性质]
技术人员晒制蓝图时,用K3Fe(C2O4)3]·H2O(三草酸合铁酸钾)作感光剂,再以K3[Fe(CN)6]氰合铁酸钾)溶液作显影剂。请回答以下问题:
(1)铁元素在周期表中位置为___________ ,Fe3+的基态价电子排布图为___________ 。
(2)在上述两种钾盐中第一电离能最大的元素为___________ ,电负性最小的元素为___________ 。
(3)H2C2O4分子中碳原子的杂化类型是___________ ,与C2O42-互为等电子体的分子的化学式为___________ (写一种)。
(4)在分析化学中F-常用于Fe3+的掩蔽剂,因为生成的FeF63-十分稳定,但Fe3+却不能与I-形成配合物,其原因是______________________ (用离子方程式来表示)。
(5)已知C60分子结构和C60晶胞如右图所示:
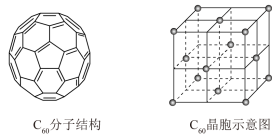
①1个C60分子中含有π键的数目为___________ 。
②晶胞中C60的配位数为___________ 。
③已知C60晶胞参数为apm,则该晶胞密度的表达式是___________ g·cm-3(NA代表阿伏伽德罗常数)。
技术人员晒制蓝图时,用K3Fe(C2O4)3]·H2O(三草酸合铁酸钾)作感光剂,再以K3[Fe(CN)6]氰合铁酸钾)溶液作显影剂。请回答以下问题:
(1)铁元素在周期表中位置为
(2)在上述两种钾盐中第一电离能最大的元素为
(3)H2C2O4分子中碳原子的杂化类型是
(4)在分析化学中F-常用于Fe3+的掩蔽剂,因为生成的FeF63-十分稳定,但Fe3+却不能与I-形成配合物,其原因是
(5)已知C60分子结构和C60晶胞如右图所示:

①1个C60分子中含有π键的数目为
②晶胞中C60的配位数为
③已知C60晶胞参数为apm,则该晶胞密度的表达式是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】2019年诺贝尔化学奖授予约翰•古德伊纳夫、斯坦利•惠廷厄姆和吉野彰三位科学家,以表彰他们在锂电池领域所做出的巨大贡献。请回答下列问题:
(1)LiCoO2、LiFePO4常用作锂离子电池的正极材料。基态Co原子核外电子排布式为___ ,基态磷原子中,电子占据的最高能层符号为___ ,该能层能量最高的电子云在空间有___ 个伸展方向,原子轨道呈___ 形。
(2)[CO(NO )4]2-中Co2+的配位数为4,配体中N原子的杂化方式为
)4]2-中Co2+的配位数为4,配体中N原子的杂化方式为___ ,该配离子中各元素的第一电离能由小到大的顺序为___ (填元素符号),1mol该配离子中含σ键数目为___ NA。
(3)MnCl2可与NH3反应生成[Mn(NH3)6]Cl2,新生成的化学键为___ 键。NH3分子的空间构型为___ ,其中N原子的杂化轨道类型为___ 。
(4)钴蓝晶体结构如图,该立方晶胞由4个I型和4个II型小立方体构成,共化学式为___ ,晶体中Al3+占据O2-形成的___ (填“四面体空隙”或“八面体空隙”)。NA为阿伏加德罗常数得值,钴蓝晶体的密度为___ g•cm-3(列计算式)。

(1)LiCoO2、LiFePO4常用作锂离子电池的正极材料。基态Co原子核外电子排布式为
(2)[CO(NO
 )4]2-中Co2+的配位数为4,配体中N原子的杂化方式为
)4]2-中Co2+的配位数为4,配体中N原子的杂化方式为(3)MnCl2可与NH3反应生成[Mn(NH3)6]Cl2,新生成的化学键为
(4)钴蓝晶体结构如图,该立方晶胞由4个I型和4个II型小立方体构成,共化学式为

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】晶体世界丰富多彩,复杂多样,各类晶体具有不同的结构特点,决定着他具有不同的性质和用途,回答下列问题:
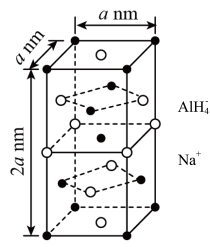
(1)氢化铝钠(NaAlH4)是一种新型轻质储氢材料,其晶胞结构如图所示,为长方体。NaAlH4晶体中,与AlH 紧邻且等距的Na+有
紧邻且等距的Na+有_____ 个;NaAlH4晶体的密度为_____ g•cm-3(用含a、NA的代数式表示)。
(2)氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方晶格的八面体空隙中,晶胞结构如图所示。
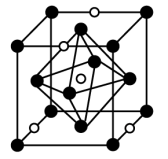
氮化钼的化学式为_____ ,Mo原子周围与之等距离的Mo原子个数为_____ 。
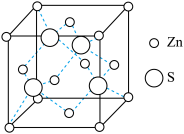
(3)ZnS的晶胞结构如图所示:晶体中S2-填充在Zn2+围成的四面体空隙中,则四面体空隙的填充率为_____ ;已知ZnS的晶胞密度是ag/cm3,则Zn2+与S2-的最短距离为_____ pm(用含a、NA的代数式表示)。
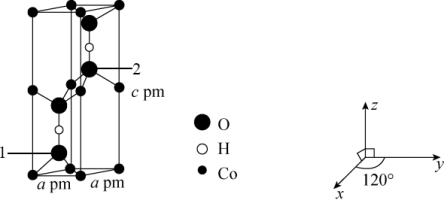
(4)已知Co可形成晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可表示晶胞中各原子的位置,称作原子的分数坐标,已知晶胞含对称中心,其中1号O原子的分数坐标为(0.6667,0.3333,0.1077),2号O原子的分数坐标为_____ 。
(1)氢化铝钠(NaAlH4)是一种新型轻质储氢材料,其晶胞结构如图所示,为长方体。NaAlH4晶体中,与AlH
 紧邻且等距的Na+有
紧邻且等距的Na+有
(2)氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方晶格的八面体空隙中,晶胞结构如图所示。

氮化钼的化学式为
(3)ZnS的晶胞结构如图所示:晶体中S2-填充在Zn2+围成的四面体空隙中,则四面体空隙的填充率为

(4)已知Co可形成晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可表示晶胞中各原子的位置,称作原子的分数坐标,已知晶胞含对称中心,其中1号O原子的分数坐标为(0.6667,0.3333,0.1077),2号O原子的分数坐标为

您最近一年使用:0次



