名校
解题方法
1 . 下列有关晶体的说法中一定正确的是
①原子晶体中只存在非极性共价键;
②稀有气体形成的晶体属于原子晶体;
③SO2与S都属于分子晶体,且SO2的摩尔质量比S的摩尔质量大,所以SO2熔沸点高于S;
④MgCO3与CaCO3都是离子晶体,且Mg2+半径比Ca2+半径小,所以MgCO3的分解温度更高;
⑤分子晶体的堆积均为分子密堆积;
⑥金属晶体和离子晶体都能导电;
⑦离子晶体和金属晶体中均存在阳离子,但金属晶体中却不存在离子键;
⑧依据构成粒子的堆积方式可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体
①原子晶体中只存在非极性共价键;
②稀有气体形成的晶体属于原子晶体;
③SO2与S都属于分子晶体,且SO2的摩尔质量比S的摩尔质量大,所以SO2熔沸点高于S;
④MgCO3与CaCO3都是离子晶体,且Mg2+半径比Ca2+半径小,所以MgCO3的分解温度更高;
⑤分子晶体的堆积均为分子密堆积;
⑥金属晶体和离子晶体都能导电;
⑦离子晶体和金属晶体中均存在阳离子,但金属晶体中却不存在离子键;
⑧依据构成粒子的堆积方式可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体
| A.①③⑦ | B.只有⑦ | C.②④⑤⑦ | D.⑤⑥⑧ |
您最近半年使用:0次
名校
2 . 汽车安全气囊中的填充物有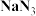 (叠氮酸钠)、
(叠氮酸钠)、 等物质。
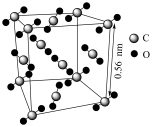
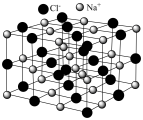
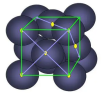
等物质。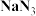 的内部结构为
的内部结构为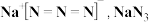 遇撞击时能生成金属钠和
遇撞击时能生成金属钠和 。
。
1.上述六种物质中能真实表示物质组成的是___________ 。
2.上述六种物质中属于非电解质的是___________ 。
3.汽车安全气囊填充物的三种物质中所涉及的5种元素中,原子半径最大的是___________ (填写元素符号)。
4.钠离子的结构示意图是___________ 。
5. 所属的晶体类型是
所属的晶体类型是___________ 晶体, 中含
中含___________  键。
键。
6.下列选项中可表示干冰内部结构的是___________。
7.写出叠氮酸钠分解的化学方程式___________ 。
8.某品牌汽车设计安全气囊受撞击时需产生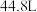 气体(已换算至标准状况下的体积),则该安全气囊中需填充的
气体(已换算至标准状况下的体积),则该安全气囊中需填充的 质量是
质量是___________  。
。
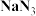 (叠氮酸钠)、
(叠氮酸钠)、 等物质。
等物质。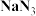 的内部结构为
的内部结构为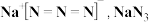 遇撞击时能生成金属钠和
遇撞击时能生成金属钠和 。
。1.上述六种物质中能真实表示物质组成的是
2.上述六种物质中属于非电解质的是
3.汽车安全气囊填充物的三种物质中所涉及的5种元素中,原子半径最大的是
4.钠离子的结构示意图是
5.
 所属的晶体类型是
所属的晶体类型是 中含
中含 键。
键。6.下列选项中可表示干冰内部结构的是___________。
|
|
|
|
| A | B | C | D |
| A.A | B.B | C.C | D.D |
8.某品牌汽车设计安全气囊受撞击时需产生
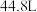 气体(已换算至标准状况下的体积),则该安全气囊中需填充的
气体(已换算至标准状况下的体积),则该安全气囊中需填充的 质量是
质量是 。
。
您最近半年使用:0次
名校
3 . 按要求填空:
(1)用系统命名法命名: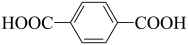 的苯环上的碳原子的杂化方式为
的苯环上的碳原子的杂化方式为___________ ,羧基上碳原子的杂化方式为___________ ,最多有___________ 个原子共平面。
(3)正硝酸钠( )为白色晶体,是一种重要的化工原料。
)为白色晶体,是一种重要的化工原料。
① 阴离子的空间构型为
阴离子的空间构型为___________ ,其中心原子杂化方式为___________ 。
②写出一种与 的阴离子互为等电子体的阴离子或分子
的阴离子互为等电子体的阴离子或分子___________ (填化学式)。
(4) 的电子式为
的电子式为___________ ; 中H-N-H键角比
中H-N-H键角比 中H-N-H键角
中H-N-H键角_________ (填“大”或“小”),理由是_____________ 。
(5)若硝酸的结构表示为 ,已知硝酸与水分子可形成一水合二硝酸结晶水合物(
,已知硝酸与水分子可形成一水合二硝酸结晶水合物(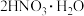 ),水分子以三个氢键与两个硝酸分子结合,请写出一水合二硝酸的结构式
),水分子以三个氢键与两个硝酸分子结合,请写出一水合二硝酸的结构式______ (氢键用“…”表示)。
(6)已知NaCl和MgO的晶体结构相似,熔点较高的是____________________ (填化学式),原因是______________________ 。
(1)用系统命名法命名:
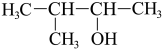

 的苯环上的碳原子的杂化方式为
的苯环上的碳原子的杂化方式为(3)正硝酸钠(
 )为白色晶体,是一种重要的化工原料。
)为白色晶体,是一种重要的化工原料。①
 阴离子的空间构型为
阴离子的空间构型为②写出一种与
 的阴离子互为等电子体的阴离子或分子
的阴离子互为等电子体的阴离子或分子(4)
 的电子式为
的电子式为 中H-N-H键角比
中H-N-H键角比 中H-N-H键角
中H-N-H键角(5)若硝酸的结构表示为
 ,已知硝酸与水分子可形成一水合二硝酸结晶水合物(
,已知硝酸与水分子可形成一水合二硝酸结晶水合物(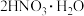 ),水分子以三个氢键与两个硝酸分子结合,请写出一水合二硝酸的结构式
),水分子以三个氢键与两个硝酸分子结合,请写出一水合二硝酸的结构式(6)已知NaCl和MgO的晶体结构相似,熔点较高的是
您最近半年使用:0次
名校
解题方法
4 . 物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
| 选项 | 性质差异 | 结构因素 |
| A | 酸性:三氟乙酸>三氯乙酸 | 电负性差异 |
| B | 熔点:SiO2>干冰 | 晶体类型差异 |
| C | 溶解性:I2在CCl4中的溶解度大于在水中的溶解度 | 相似相溶 |
| D | 稳定性:H2O的分解温度(3000℃)远大于H2S(900℃) | 有无氢键 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
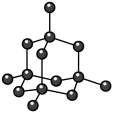
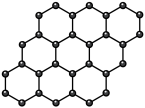
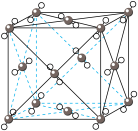
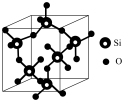
5 . 观察下列模型,判断下列说法错误的是
金刚石 | 碳化硅 | 二氧化硅 | 石墨烯 | 干冰 |
|
|
|
|
|
| A.原子数相同的金刚石和碳化硅,共价键个数之比为1∶2 |
B. 晶体中Si和Si-O键个数比为1∶4 晶体中Si和Si-O键个数比为1∶4 |
| C.石墨烯中碳原子和六元环个数比为2∶1 |
| D.干冰晶体堆积属于分子密堆积 |
您最近半年使用:0次
名校
6 . 共价键、离子键和范德华力都是微观粒子之间的不同作用力,下列物质:① ;②SiO₂;③石墨; ④金刚石; ⑤CaCl₂; ⑥白磷, 其中含有两种作用力的组合是
;②SiO₂;③石墨; ④金刚石; ⑤CaCl₂; ⑥白磷, 其中含有两种作用力的组合是
 ;②SiO₂;③石墨; ④金刚石; ⑤CaCl₂; ⑥白磷, 其中含有两种作用力的组合是
;②SiO₂;③石墨; ④金刚石; ⑤CaCl₂; ⑥白磷, 其中含有两种作用力的组合是| A.①③⑤⑥ | B.①③⑥ | C.②④⑥ | D.①②③⑥ |
您最近半年使用:0次
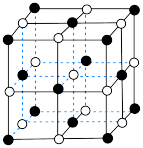
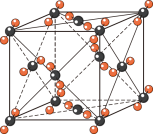
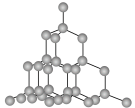
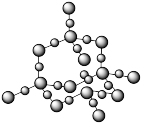
7 . 以下是四种物质的晶体结构示意图。其中属于离子晶体的是
| A |  | C | D |

| 
|  | 
|
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
8 . 氟及其化合物用途非常广泛。回答下列问题:
(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过____________ 方法区分晶体、准晶体和非晶体。
(2)基态铜原子价层电子排布图为______ 。
(3)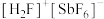 (氟锑酸)是一种超强酸,存在
(氟锑酸)是一种超强酸,存在 ,该离子的空间构型为
,该离子的空间构型为______ ,与 具有相同空间构型和成键方式的分子和阴离子分别是
具有相同空间构型和成键方式的分子和阴离子分别是______ (各举一例)。
(4) (氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。
(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。 中中心原子的杂化类型是
中中心原子的杂化类型是______ ;氟化铵中存在______ (填字母)。
A.离子键 B.σ键 C.π键 D.氢键
(5) 被广泛用作高压电气设备的绝缘介质。
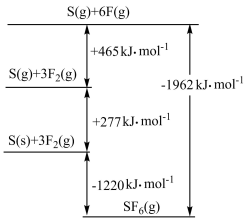
被广泛用作高压电气设备的绝缘介质。 是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则
是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则 键的键能为
键的键能为______ kJ·mol ,
, 键的键能为
键的键能为______ kJ·mol 。
。 。
。
①CuF的熔点比CuCl的高,原因是____________ 。
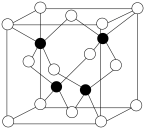
②已知 为阿伏加德罗常数的值,CuF的晶胞结构如图所示,则CuF的晶胞参数
为阿伏加德罗常数的值,CuF的晶胞结构如图所示,则CuF的晶胞参数
______ nm(列出计算式)。
(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)基态铜原子价层电子排布图为
(3)
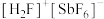 (氟锑酸)是一种超强酸,存在
(氟锑酸)是一种超强酸,存在 ,该离子的空间构型为
,该离子的空间构型为 具有相同空间构型和成键方式的分子和阴离子分别是
具有相同空间构型和成键方式的分子和阴离子分别是(4)
 (氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。
(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。 中中心原子的杂化类型是
中中心原子的杂化类型是A.离子键 B.σ键 C.π键 D.氢键
(5)
 被广泛用作高压电气设备的绝缘介质。
被广泛用作高压电气设备的绝缘介质。 是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则
是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则 键的键能为
键的键能为 ,
, 键的键能为
键的键能为 。
。
 。
。①CuF的熔点比CuCl的高,原因是
②已知
 为阿伏加德罗常数的值,CuF的晶胞结构如图所示,则CuF的晶胞参数
为阿伏加德罗常数的值,CuF的晶胞结构如图所示,则CuF的晶胞参数
您最近半年使用:0次
9 . 下列说法正确的是
| A.CO2、HClO、P4分子中所有原子均满足最外层8电子稳定结构 |
| B.离子晶体中可能存在共价键,而分子晶体中一定存在共价键 |
| C.氨气很稳定(很高温度才会部分分解),并不是氨气中含有大量的氢键所致 |
| D.金刚石、石英和C60均为空间网状结构的共价晶体,加热熔化时需破坏共价键 |
您最近半年使用:0次
10 . 等离子电视曾风靡一时,等离子电视和液晶电视都属于平板电视。下列说法不正确的是
| A.等离子体是由电子、阳离子和电中性粒子组成的整体上呈电中性的气态物质 |
| B.等离子体具有良好的导电性和流动性,等离子体通过电场时,所有粒子的运动方向都发生改变 |
| C.液晶是介于液态和晶态之间的物质状态 |
| D.液晶既具有液体的流动性,又表现出类似晶体的各向异性 |
您最近半年使用:0次