解题方法
1 . 2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯( )与四氟乙烯(
)与四氟乙烯( )的共聚物(ETFE)制成。回答下列问题:
)的共聚物(ETFE)制成。回答下列问题:
(1)图 、
、 、
、 分别表示
分别表示 、
、 、
、 和
和 的逐级电离能
的逐级电离能 变化趋势(纵坐标的标度不同)。第一电离能的变化图是
变化趋势(纵坐标的标度不同)。第一电离能的变化图是___________ (填标号);第三电离能的变化图是___________ (填标号)。 后,科学家合成了
后,科学家合成了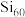 、
、 ,三者结构相似。下列说法正确的是
,三者结构相似。下列说法正确的是___________ (填序号) 、
、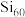 、
、 都属于共价晶体
都属于共价晶体
B.由于 键能小于
键能小于 ,故
,故 的稳定性弱于
的稳定性弱于
C.由于 键长小于
键长小于 键,所以
键,所以 熔沸点低于
熔沸点低于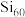
(3) 分子的空间结构为
分子的空间结构为___________ ; 的熔、沸点
的熔、沸点___________ (填“高于”或“低于”) ,原因是
,原因是___________ 。
(4) (二氟氮烯)分子中,氮原子的杂化类型为
(二氟氮烯)分子中,氮原子的杂化类型为 ,则
,则 的结构式为
的结构式为___________ 。
(5)晶体硅的结构和金刚石结构相似,碳化硅( )也是一种具有类似于金刚石结构的晶体,其中碳原子核硅原子的位置是交替的。在①金刚石,②晶体硅,③碳化硅这三种晶体中,它们的熔点从高到低的顺序是___________
)也是一种具有类似于金刚石结构的晶体,其中碳原子核硅原子的位置是交替的。在①金刚石,②晶体硅,③碳化硅这三种晶体中,它们的熔点从高到低的顺序是___________
 )与四氟乙烯(
)与四氟乙烯( )的共聚物(ETFE)制成。回答下列问题:
)的共聚物(ETFE)制成。回答下列问题:(1)图
 、
、 、
、 分别表示
分别表示 、
、 、
、 和
和 的逐级电离能
的逐级电离能 变化趋势(纵坐标的标度不同)。第一电离能的变化图是
变化趋势(纵坐标的标度不同)。第一电离能的变化图是
 后,科学家合成了
后,科学家合成了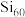 、
、 ,三者结构相似。下列说法正确的是
,三者结构相似。下列说法正确的是
 、
、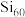 、
、 都属于共价晶体
都属于共价晶体B.由于
 键能小于
键能小于 ,故
,故 的稳定性弱于
的稳定性弱于
C.由于
 键长小于
键长小于 键,所以
键,所以 熔沸点低于
熔沸点低于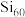
(3)
 分子的空间结构为
分子的空间结构为 的熔、沸点
的熔、沸点 ,原因是
,原因是(4)
 (二氟氮烯)分子中,氮原子的杂化类型为
(二氟氮烯)分子中,氮原子的杂化类型为 ,则
,则 的结构式为
的结构式为(5)晶体硅的结构和金刚石结构相似,碳化硅(
 )也是一种具有类似于金刚石结构的晶体,其中碳原子核硅原子的位置是交替的。在①金刚石,②晶体硅,③碳化硅这三种晶体中,它们的熔点从高到低的顺序是___________
)也是一种具有类似于金刚石结构的晶体,其中碳原子核硅原子的位置是交替的。在①金刚石,②晶体硅,③碳化硅这三种晶体中,它们的熔点从高到低的顺序是___________| A.①③② | B.③②① | C.③①② | D.②①③ |
您最近一年使用:0次
2 . W、X、Y、Z、M是原子序数依次增大的五种短周期主族元素,它们组成的一种新材料的结构如图所示。

A.第一电离能: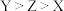 |
B.简单离子半径: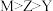 |
C.氧化物对应水化物的酸性: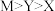 |
D. 分别与 分别与 形成的化合物的晶体类型不相同 形成的化合物的晶体类型不相同 |
您最近一年使用:0次
名校
3 . 下列有关物质结构与性质的说法错误的是
| A.简单氢化物分子间形成的氢键越多,物质的熔、沸点越高 |
| B.超分子具有分子识别和自组装的重要特征 |
C.通过X射线衍射实验可区分晶体 和非晶体 和非晶体 |
| D.离子晶体中阴、阳离子有配位数说明离子键有饱和性 |
您最近一年使用:0次
2024-05-12更新
|
80次组卷
|
2卷引用:河南省漯河市高级中学2023-2024学年高三下学期5月月考化学试题
4 . 有关X、Y、Z、W四种元素的描述如下: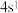
①基态 的离子结构示意图为
的离子结构示意图为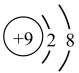
②基态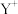 的轨道表示式为
的轨道表示式为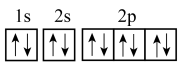
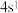
④基态W原子有3个电子层,其电子式为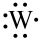
| A.金属性:Z<Y | B.X与W的最高正价相同 |
| C.YX的熔点高于YW的 | D.上述四种元素对应的单质的晶体类型有3种 |
您最近一年使用:0次
5 . 下列晶体中,与 的晶体类型和化学键类型完全相同的是
的晶体类型和化学键类型完全相同的是
 的晶体类型和化学键类型完全相同的是
的晶体类型和化学键类型完全相同的是| A.KCl | B.Cu | C. | D. |
您最近一年使用:0次
6 . 下列对一些实验事实的解释错误的是
| 选项 | 实验事实 | 解释 |
| A | 水加热到较高温度难以分解 | 水分子中共价键键能较大 |
| B | 石墨棒作为原电池的电极材料 | 石墨晶体能导电 |
| C |  的沸点高于 的沸点高于 | H-N键的键长比H-P键的键长短 |
| D | 用X射线实验区分玻璃和水晶 | 水晶的衍射图上有明锐的衍射峰 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
| 选项 | 性质差异 | 结构因素 |
| A | 酸性:三氟乙酸>三氯乙酸 | 电负性差异 |
| B | 熔点:SiO2>干冰 | 晶体类型差异 |
| C | 溶解性:I2在CCl4中的溶解度大于在水中的溶解度 | 相似相溶 |
| D | 稳定性:H2O的分解温度(3000℃)远大于H2S(900℃) | 有无氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-27更新
|
179次组卷
|
2卷引用:河南省濮阳市第一高级中学2023-2024学年高二下学期第一次月考化学(B)试题
名校
8 . 我国科研工作者发现了一种在低压条件下高效电催化还原 的新方法,其总反应为
的新方法,其总反应为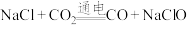 。下列说法错误的是
。下列说法错误的是
 的新方法,其总反应为
的新方法,其总反应为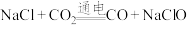 。下列说法错误的是
。下列说法错误的是A. 的晶体类型是离子晶体 的晶体类型是离子晶体 |
B. 的键角为 的键角为 |
C.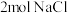 中含有氯化钠分子的数目为 中含有氯化钠分子的数目为 |
| D.该反应中存在共价键、离子键的断裂与形成 |
您最近一年使用:0次
9 . 现有部分前四周期元素的性质或原子结构如下表:
(1)B单质分子中,含有___________ 个 键和
键和___________ 个 键,元素B的气态氢化物的空间型为
键,元素B的气态氢化物的空间型为___________ 。
(2)C单质的熔点___________ A单质的熔点(填“高于”或“低于”),其原因是:___________
(3)写出元素D基态原子的电子排布式:___________ 。
| 元素编号 | 元素性质或原子结构 |
| A | 第三周期中的半导体材料 |
| B | L层s电子数比p电子数少1 |
| C | 第三周期主族元素中其第一电离能最大 |
| D | 前四周期呀中其未成对电子数最多 |
 键和
键和 键,元素B的气态氢化物的空间型为
键,元素B的气态氢化物的空间型为(2)C单质的熔点
(3)写出元素D基态原子的电子排布式:
您最近一年使用:0次
解题方法
10 . 化学与人类生产、生活密切相关,下列说法中错误的是
| A.亚硝酸钠有毒,不能用作食品添加剂 |
| B.储氢合金是一类能够大量吸收氢气,并与氢气结合成金属氢化物的材料 |
| C.电阻率低、热导率高的石墨烯可用于制作超级导电材料 |
| D.液晶既有液体的流动性,又有类似晶体的各向异性 |
您最近一年使用:0次



