[化学——选修3:物质结构与性质]
技术人员晒制蓝图时,用K3Fe(C2O4)3]·H2O(三草酸合铁酸钾)作感光剂,再以K3[Fe(CN)6]氰合铁酸钾)溶液作显影剂。请回答以下问题:
(1)铁元素在周期表中位置为___________ ,Fe3+的基态价电子排布图为___________ 。
(2)在上述两种钾盐中第一电离能最大的元素为___________ ,电负性最小的元素为___________ 。
(3)H2C2O4分子中碳原子的杂化类型是___________ ,与C2O42-互为等电子体的分子的化学式为___________ (写一种)。
(4)在分析化学中F-常用于Fe3+的掩蔽剂,因为生成的FeF63-十分稳定,但Fe3+却不能与I-形成配合物,其原因是______________________ (用离子方程式来表示)。
(5)已知C60分子结构和C60晶胞如右图所示:
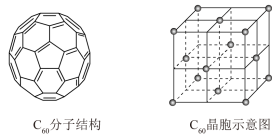
①1个C60分子中含有π键的数目为___________ 。
②晶胞中C60的配位数为___________ 。
③已知C60晶胞参数为apm,则该晶胞密度的表达式是___________ g·cm-3(NA代表阿伏伽德罗常数)。
技术人员晒制蓝图时,用K3Fe(C2O4)3]·H2O(三草酸合铁酸钾)作感光剂,再以K3[Fe(CN)6]氰合铁酸钾)溶液作显影剂。请回答以下问题:
(1)铁元素在周期表中位置为
(2)在上述两种钾盐中第一电离能最大的元素为
(3)H2C2O4分子中碳原子的杂化类型是
(4)在分析化学中F-常用于Fe3+的掩蔽剂,因为生成的FeF63-十分稳定,但Fe3+却不能与I-形成配合物,其原因是
(5)已知C60分子结构和C60晶胞如右图所示:

①1个C60分子中含有π键的数目为
②晶胞中C60的配位数为
③已知C60晶胞参数为apm,则该晶胞密度的表达式是
更新时间:2019-02-17 16:45:05
|
相似题推荐
填空题
|
较难
(0.4)
名校
【推荐1】水合肼 在储氢领域有广阔的应用前景,其水溶液呈弱碱性。
在储氢领域有广阔的应用前景,其水溶液呈弱碱性。
(1) 分子有顺式、反式和交互式三种比较稳定的空间构型。下列结构能表示
分子有顺式、反式和交互式三种比较稳定的空间构型。下列结构能表示 分子交互式的是
分子交互式的是_______ (填序号)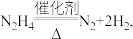 肼的理论储氢密度
肼的理论储氢密度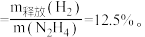 测得肼实际分解时产生的气体中含
测得肼实际分解时产生的气体中含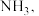 肼实际储氢密度小于理论值的原因是
肼实际储氢密度小于理论值的原因是_______ (用化学方程式表示)。
(3)水合肼制氢过程中涉及肼在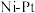 催化剂表面分解,如图所示。
催化剂表面分解,如图所示。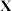 的结构简式为
的结构简式为_______ 。
②催化剂表面存在 和
和 两种活性位点,两种活性位点分别带不同电性的电荷。肼中的氢原子吸附于
两种活性位点,两种活性位点分别带不同电性的电荷。肼中的氢原子吸附于_______ (填“ ”或“
”或“ ”)活性位点。已知:
”)活性位点。已知: 键、
键、 键的键能分别是
键的键能分别是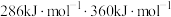 。肼在该催化剂表面反应断裂的化学键不是
。肼在该催化剂表面反应断裂的化学键不是 键,而是
键,而是 键,原因是
键,原因是_______ 。
③催化剂存在下,不同浓度的 分解时,测得
分解时,测得 随时间的变化如下图所示。当
随时间的变化如下图所示。当 浓度从
浓度从 增加到
增加到 时,反应速率加快;从
时,反应速率加快;从 增加到
增加到 时,反应速率几乎不变。其原因是
时,反应速率几乎不变。其原因是_______ 。
 在储氢领域有广阔的应用前景,其水溶液呈弱碱性。
在储氢领域有广阔的应用前景,其水溶液呈弱碱性。(1)
 分子有顺式、反式和交互式三种比较稳定的空间构型。下列结构能表示
分子有顺式、反式和交互式三种比较稳定的空间构型。下列结构能表示 分子交互式的是
分子交互式的是
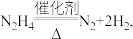 肼的理论储氢密度
肼的理论储氢密度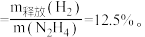 测得肼实际分解时产生的气体中含
测得肼实际分解时产生的气体中含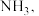 肼实际储氢密度小于理论值的原因是
肼实际储氢密度小于理论值的原因是(3)水合肼制氢过程中涉及肼在
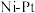 催化剂表面分解,如图所示。
催化剂表面分解,如图所示。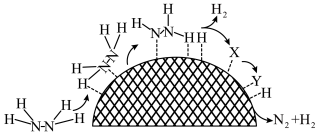
 的结构简式为
的结构简式为②催化剂表面存在
 和
和 两种活性位点,两种活性位点分别带不同电性的电荷。肼中的氢原子吸附于
两种活性位点,两种活性位点分别带不同电性的电荷。肼中的氢原子吸附于 ”或“
”或“ ”)活性位点。已知:
”)活性位点。已知: 键、
键、 键的键能分别是
键的键能分别是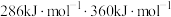 。肼在该催化剂表面反应断裂的化学键不是
。肼在该催化剂表面反应断裂的化学键不是 键,而是
键,而是 键,原因是
键,原因是③催化剂存在下,不同浓度的
 分解时,测得
分解时,测得 随时间的变化如下图所示。当
随时间的变化如下图所示。当 浓度从
浓度从 增加到
增加到 时,反应速率加快;从
时,反应速率加快;从 增加到
增加到 时,反应速率几乎不变。其原因是
时,反应速率几乎不变。其原因是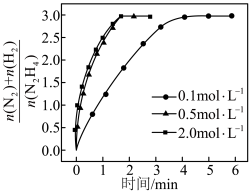
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】将氟气通入氢氧化钠溶液中,可得OF2.OF2是一种无色、几乎无味的剧毒气体,主要用于氧化氟化反应、火箭工程助燃剂等。请回答下列问题:
(1)OF2中O的化合价为_______ ,OF2中O原子的杂化轨道类型是_______ ,OF2分子的空间构型为_______ 。
(2)与H2O分子相比,OF2分子的键角更_______ (填“大”或“小”)。
(3)与H2O分子相比,OF2分子的极性更_______ (填“大” 或“小”),原因是_______ ;
(4)OF2 在常温下就能与干燥空气反应生成二氧化氮和无色气体氟化氮,该反应的化学方程式为(已知反应中N2与O2的物质的量之比为4:1)_______ 。
(1)OF2中O的化合价为
(2)与H2O分子相比,OF2分子的键角更
(3)与H2O分子相比,OF2分子的极性更
(4)OF2 在常温下就能与干燥空气反应生成二氧化氮和无色气体氟化氮,该反应的化学方程式为(已知反应中N2与O2的物质的量之比为4:1)
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】(1)前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差2。
回答下列问题:
①D2+的价层电子排布图为____ 。
②四种元素中第一电离能最小的是____ (填元素符号,下同),电负性最大的是____ 。
(2)Ge的最高价氯化物分子式是______ 。该元素可能的性质或应用有__________________ 。
A.是一种活泼的金属元素
B.其电负性大于硫
C.其单质可作为半导体材料
D.其最高价氯化物的沸点低于其溴化物的沸点
回答下列问题:
①D2+的价层电子排布图为
②四种元素中第一电离能最小的是
(2)Ge的最高价氯化物分子式是
A.是一种活泼的金属元素
B.其电负性大于硫
C.其单质可作为半导体材料
D.其最高价氯化物的沸点低于其溴化物的沸点
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】立方氮化硼CBN( Cubic Boron Nitrde)的硬度仅次于金刚石而远远高于其它材料,因此它与金刚石统称为超硬材料,具有优异的耐磨性。其晶体结构如下图所示:
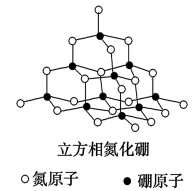
(1)基态氮原子的价电子层排布式是_____________ ,在氮和硼原子所在的周期中,第一电离能小于氮原子的有_____ 种元素的原子。
(2)氮原子和硼原子形成的化学键类型有_____________________ 。
(3)硼原子的杂化类型是_______ ,与硼原子紧相连的4个氮原子的空间构型是________ ,键角是_______ 。
(4)晶胞如图所示,该晶体属于______ 晶体。

(5)晶体中所连接的最小环上是六元环,每个硼原子被_____ 个六元环共用,六元环最多有_____ 个原子在同一平面上。若晶胞边长为apm,立方氮化硼的密度是ρg/cm3,则NA的表达式是____ (用a和ρ表示)。

(1)基态氮原子的价电子层排布式是
(2)氮原子和硼原子形成的化学键类型有
(3)硼原子的杂化类型是
(4)晶胞如图所示,该晶体属于

(5)晶体中所连接的最小环上是六元环,每个硼原子被
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(1)Ni原子的核外电子排布式为____________ ;
(2)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO______ FeO(填“<”或“>”);
(3)NiO晶胞中Ni和O的配位数分别为________ 、_________ ;
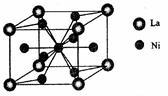
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为_________ ;
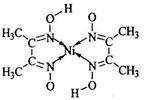
(5)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如右上图所示。
①该结构中,碳碳之间的共价键类型是σ键,碳氮之间的共价键类型是________ ,氮镍之间形成的化学键是______ ;
②该结构中,氧氢之间除共价键外还可存在__________ ;
③该结构中,碳原子的杂化轨道类型有______________ 。
(1)Ni原子的核外电子排布式为
(2)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO
(3)NiO晶胞中Ni和O的配位数分别为
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为


(5)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如右上图所示。
①该结构中,碳碳之间的共价键类型是σ键,碳氮之间的共价键类型是
②该结构中,氧氢之间除共价键外还可存在
③该结构中,碳原子的杂化轨道类型有
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】根据物质结构有关性质和特点,回答以下问题:
(1)过渡元素Co 基态原子价电子轨道表达式为_______________________________ 。第四电离能I4 (Co) < I4 (Fe) ,其原因是__________________________________________ 。
(2)磷的氯化物有两种:PCl3和PCl5 ,PCl3中磷原子的杂化类型为__________ ,PCl3的立体构型为__________ ,其中PCl3的沸点________ (填“大于”或“小于”)PCl5,原因是__________ 。
(3)酞菁铟是有机分子酞菁与金属铟形成的复杂分子,结构简式如下图所示,该分子中存在的化学键为___________ (填选项字母)
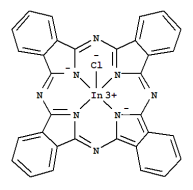
a.σ键 b.π键 c.离子键 d.配位键
(4)氯有多种含氧酸,其电离平衡常数如下:
从物质结构的角度解释以上含氧酸 Ka 依次减小的原因________________________ 。
(5)钴的一种化合物的晶胞结构如下图所示:
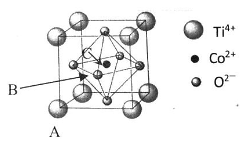
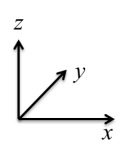
①已知A点的原子坐标参数为(0,0,0),C 点为(1/2,1/2,1/2),则B点的原子坐标参数为___________ 。
②已知晶胞参数 a = 0.5485 nm,则该晶体的密度为_______________ g/cm3。(列出计算表达式即可)
(1)过渡元素Co 基态原子价电子轨道表达式为
(2)磷的氯化物有两种:PCl3和PCl5 ,PCl3中磷原子的杂化类型为
(3)酞菁铟是有机分子酞菁与金属铟形成的复杂分子,结构简式如下图所示,该分子中存在的化学键为

a.σ键 b.π键 c.离子键 d.配位键
(4)氯有多种含氧酸,其电离平衡常数如下:
| 化学式 | HClO4 | HClO3 | HClO2 | HClO |
| Ka | 1×1010 | 1×10 | 1×10‾2 | 4×10‾8 |
从物质结构的角度解释以上含氧酸 Ka 依次减小的原因
(5)钴的一种化合物的晶胞结构如下图所示:


①已知A点的原子坐标参数为(0,0,0),C 点为(1/2,1/2,1/2),则B点的原子坐标参数为
②已知晶胞参数 a = 0.5485 nm,则该晶体的密度为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】铁及其化合物在有机化学中应用广泛,例如有机合成中,常用铁和盐酸将硝基(﹣NO2)还原为氨基(﹣NH2);在苯的溴代反应中用溴化铁作催化剂。
(1)N的原子结构示意图为_______ ,Fe基态原子核外电子排布式为_______ 。
(2)H、N、O 的电负性从小到大的顺序是_______ 。
(3)与NO2+互为等电子体的一种分子为_____ (填化学式),氨基(﹣NH2)中氮原子的杂化类型为_____ 。
(4)1mol苯分子中含有σ键的物质的量为______ 。
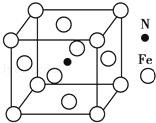
(5)Fe 与 N 形成的某化合物晶胞如图所示,则该晶体的化学式为_______ 。
(1)N的原子结构示意图为
(2)H、N、O 的电负性从小到大的顺序是
(3)与NO2+互为等电子体的一种分子为
(4)1mol苯分子中含有σ键的物质的量为
(5)Fe 与 N 形成的某化合物晶胞如图所示,则该晶体的化学式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】已知元素镓和砷的单质及其化合物在工业生产上有重要的用途。回答下列问题:
(1)砷元素基态原子的电子排布式为_______________________ 。
(2)砷与氢元素可形成化合物砷化氢,该化合物的空间构型为_____________ ,其中砷原子的杂化方式为__________ 。
(3)根据等电子原理,写出由短周期元素组成且与砷化氢互为等电子体的一种离子的化学式________ 。
(4)已知由元素砷与镓元素组成的化合物A为第三代半导体。已知化合物A的晶胞结构与金刚石相似,其中砷原子位于立方体内,镓原子位于立方体顶点和面心,请写出化合物A的化学式____________ ;
(5)已知铝与镓元素位于同一主族,金属铝属立方晶系,其晶胞边长为405 pm,密度是2.70g·cm-3,通过计算确定铝原子在三维空间中堆积方式________________ (已知NA=6.02×1023,1pm=10-10cm,4053=6.64×107);晶胞中距离最近的铝原子可看作是接触的,列式计算铝的原子半径r(A1)=______ pm.(只列出计算式即可)
(1)砷元素基态原子的电子排布式为
(2)砷与氢元素可形成化合物砷化氢,该化合物的空间构型为
(3)根据等电子原理,写出由短周期元素组成且与砷化氢互为等电子体的一种离子的化学式
(4)已知由元素砷与镓元素组成的化合物A为第三代半导体。已知化合物A的晶胞结构与金刚石相似,其中砷原子位于立方体内,镓原子位于立方体顶点和面心,请写出化合物A的化学式
(5)已知铝与镓元素位于同一主族,金属铝属立方晶系,其晶胞边长为405 pm,密度是2.70g·cm-3,通过计算确定铝原子在三维空间中堆积方式
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】氟是卤族元素中原子半径最小的元素,氟的化合物种类繁多,用途广泛。回答下列问题:
(1)基态氟原子价电子的电子排布图(轨道表达式)为___________ ,其电子占据的最高能级的电子云轮廓图为___________ 。
(2)NaF和MgF2均为离子晶体,其熔沸点如下表:
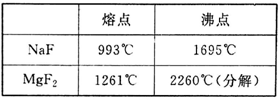
Na+、Mg2+、F-的离子半径大小顺序为___________ ,MgF2熔沸点比NaF高的原因是___________ 。
(3)氟虫腈是一种广谱性杀虫剂,其结构简式如下图甲:
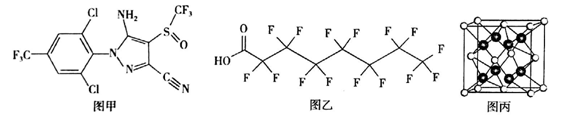
氟虫腈中碳原子的杂化方式为___________ ,氟虫腈晶体中存在___________ (填标号)。
a.离子键 b.π键 c.非极性键 d.氢键 e.极性键
(4)全氟辛酸(如上图乙)主要用作表面活性剂、乳化剂。全氟辛酸结构中,与每个碳原子(除羧基碳外)相连的F、C的空间构型为___________ ,构成该物质的C、O、F的第一电离能强弱为___________ 。
(5)PbF2具有萤石结构晶胞如上图两所示。每个Pb2+周围等距且紧邻的F-有___________ 个。已知晶胞参数为anm,阿伏伽德罗常数的值为NA,则PbF2的密度为________ g/cm3。
(1)基态氟原子价电子的电子排布图(轨道表达式)为
(2)NaF和MgF2均为离子晶体,其熔沸点如下表:

Na+、Mg2+、F-的离子半径大小顺序为
(3)氟虫腈是一种广谱性杀虫剂,其结构简式如下图甲:

氟虫腈中碳原子的杂化方式为
a.离子键 b.π键 c.非极性键 d.氢键 e.极性键
(4)全氟辛酸(如上图乙)主要用作表面活性剂、乳化剂。全氟辛酸结构中,与每个碳原子(除羧基碳外)相连的F、C的空间构型为
(5)PbF2具有萤石结构晶胞如上图两所示。每个Pb2+周围等距且紧邻的F-有
您最近一年使用:0次



