将氟气通入氢氧化钠溶液中,可得OF2.OF2是一种无色、几乎无味的剧毒气体,主要用于氧化氟化反应、火箭工程助燃剂等。请回答下列问题:
(1)OF2中O的化合价为_______ ,OF2中O原子的杂化轨道类型是_______ ,OF2分子的空间构型为_______ 。
(2)与H2O分子相比,OF2分子的键角更_______ (填“大”或“小”)。
(3)与H2O分子相比,OF2分子的极性更_______ (填“大” 或“小”),原因是_______ ;
(4)OF2 在常温下就能与干燥空气反应生成二氧化氮和无色气体氟化氮,该反应的化学方程式为(已知反应中N2与O2的物质的量之比为4:1)_______ 。
(1)OF2中O的化合价为
(2)与H2O分子相比,OF2分子的键角更
(3)与H2O分子相比,OF2分子的极性更
(4)OF2 在常温下就能与干燥空气反应生成二氧化氮和无色气体氟化氮,该反应的化学方程式为(已知反应中N2与O2的物质的量之比为4:1)
更新时间:2023-11-22 10:38:01
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】草酸(H2C2O4,二元弱酸)与草酸盐在实验和工业生产中都起着重要的作用。
(1)Na2C2O4溶液显碱性,请用离子方程式解释原因_______ 。
(2)KMnO4能与硫酸酸化的Na2C2O4溶液反应生成Mn2+和CO2,该反应的离子方程式为_____ 。
(3)常温下,pH=3的H2C2O4溶液的物质的量浓度为c1,水电离出的c(H+)为c3;pH=4的H2C2O4溶液的物质的量浓度为c2,水电离出的c(H+)为c4。则c1_______ 10c2(填“>”“<”或“=”,下同);10c3_______ c4。
(4)常温下,用0.1000mol·L-1NaOH溶液滴定20.00mL某未知浓度的H2C2O4溶液,滴定曲线如图,c点所示溶液中:2c( )+2c(
)+2c( )+2c(H2C2O4)=c(Na+)
)+2c(H2C2O4)=c(Na+)

①该草酸溶液的物质的量浓度为______________ (列出计算式,并得出计算结果)。
②a点所示溶液中各离子的浓度由大到小的顺序为_______ 。
(1)Na2C2O4溶液显碱性,请用离子方程式解释原因
(2)KMnO4能与硫酸酸化的Na2C2O4溶液反应生成Mn2+和CO2,该反应的离子方程式为
(3)常温下,pH=3的H2C2O4溶液的物质的量浓度为c1,水电离出的c(H+)为c3;pH=4的H2C2O4溶液的物质的量浓度为c2,水电离出的c(H+)为c4。则c1
(4)常温下,用0.1000mol·L-1NaOH溶液滴定20.00mL某未知浓度的H2C2O4溶液,滴定曲线如图,c点所示溶液中:2c(
 )+2c(
)+2c( )+2c(H2C2O4)=c(Na+)
)+2c(H2C2O4)=c(Na+)
①该草酸溶液的物质的量浓度为
②a点所示溶液中各离子的浓度由大到小的顺序为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)直链聚磷酸是由n个磷酸分子通过分子间脱水形成的,常用于制取阻燃剂聚磷酸铵。
①写出磷酸主要的电离方程式_____________________ 。
②直链低聚磷酸铵的化学式可表示为(NH4)(n+2)PnOx,x=_________ (用n表示)。
(2)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式。
□H2PO2-+□Ag+ + □________ = □PO43-+ □Ag +□
(3)由工业白磷(含少量砷、铁、镁等)制备高纯白磷(熔点44℃,沸点280℃),主要生产流程如下

①除砷过程在75℃下进行,其合理的原因是_______ (填字母)。
a.温度不宜过高,防止硝酸分解 b.适当提高温度,加快化学反应速率
c.使白磷熔化,并溶于水 d.降低白磷的毒性
②硝酸氧化除砷时被还原为NO,若氧化产物为等物质的量的亚砷酸与砷酸,则化学反应方程式为_______________
(1)直链聚磷酸是由n个磷酸分子通过分子间脱水形成的,常用于制取阻燃剂聚磷酸铵。
①写出磷酸主要的电离方程式
②直链低聚磷酸铵的化学式可表示为(NH4)(n+2)PnOx,x=
(2)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式。
□H2PO2-+□Ag+ + □
(3)由工业白磷(含少量砷、铁、镁等)制备高纯白磷(熔点44℃,沸点280℃),主要生产流程如下

①除砷过程在75℃下进行,其合理的原因是
a.温度不宜过高,防止硝酸分解 b.适当提高温度,加快化学反应速率
c.使白磷熔化,并溶于水 d.降低白磷的毒性
②硝酸氧化除砷时被还原为NO,若氧化产物为等物质的量的亚砷酸与砷酸,则化学反应方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】铁和钴是两种重要的过渡元素。
(1)钴位于元素周期表的第______ 族,其基态原子中未成对电子个数为________ 。
(2)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中Fe3+的核外电子排布式为_________________________________ ,所含非金属元素的电负性由大到小的顺序是_____________________________ 。
(3)尿素[CO(NH2)2]分子中,碳原子为_______ 杂化,分子中σ键与π键的数目之比为_________ 。
(4)FeO晶体与NaCl晶体结构相似,比较FeO与NaCl的晶格能大小,还需知道的数据是________________________________________ 。
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为___________________ 。
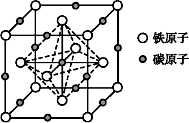
(6)奥氏体是碳溶解在r-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如图所示,则该物质的化学式为____________ 。若晶体密度为d g·cm-3,则晶胞中最近的两个碳原子的距离为___________________ pm(阿伏伽德罗常数的值用NA表示,写出简化后的计算式即可)。
(1)钴位于元素周期表的第
(2)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中Fe3+的核外电子排布式为
(3)尿素[CO(NH2)2]分子中,碳原子为
(4)FeO晶体与NaCl晶体结构相似,比较FeO与NaCl的晶格能大小,还需知道的数据是
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为
(6)奥氏体是碳溶解在r-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如图所示,则该物质的化学式为

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】卤素钙钛矿已经被广泛应用于太阳能电池、发光二极体等领域,其中合成二维/三维(2D/3D)的钙钛矿异质结是提升器件稳定性和转换效率的一个策略,近期化学工作者在气相合成的单晶三维钙钛矿CsPbBr3上合成外延生长的水平和垂直的二维钙钛矿(PEA)2PbBr4(PEA+代表 )异质结。回答下列问题:
)异质结。回答下列问题:
(1)基态Br原子的价电子排布式为___ 。
(2)PEA+中N的价层电子对数为___ ,杂化轨道类型为___ ,PEA+中涉及元素的电负性由大到小的顺序为___ ,1molPEA+中存在___ molσ键。
(3)已知铅卤化合物中存在正四面体构型的[PbCl4]2-、[PbBr4]2-、[PbI4]2-,三者中半径最小的配体为___ 。已知[Pb2I6]2-中每个Pb均采用四配位模式,则[Pb2I6]2-的结构式为___ 。
(4)Br2和碱金属单质形成的MBr熔点如表:
等量NaBr、KBr、RbBr、CsBr同时开始加热优先导电的是____ (填化学式),熔点呈现表中趋势的原因是____ 。
(5)已知三维立方钙钛矿CsPbBr3中三种离子在晶胞(a)中占据正方体顶点、面心、体心位置,图(b)显示的是三种离子在xz面、yz面、xy面上的位置:

若晶胞边长为apm,阿伏加德罗常数的值为NA,晶体的密度为___ g·cm-3 (写出表达式)。
②上述晶胞沿体对角线方向的投影图为___ (填标号)。
A. B.
B. C.
C. D.
D.
 )异质结。回答下列问题:
)异质结。回答下列问题:(1)基态Br原子的价电子排布式为
(2)PEA+中N的价层电子对数为
(3)已知铅卤化合物中存在正四面体构型的[PbCl4]2-、[PbBr4]2-、[PbI4]2-,三者中半径最小的配体为
(4)Br2和碱金属单质形成的MBr熔点如表:
| MBr | NaBr | KBr | RbBr | CsBr |
| 熔点/℃ | 747 | 734 | 693 | 636 |
等量NaBr、KBr、RbBr、CsBr同时开始加热优先导电的是
(5)已知三维立方钙钛矿CsPbBr3中三种离子在晶胞(a)中占据正方体顶点、面心、体心位置,图(b)显示的是三种离子在xz面、yz面、xy面上的位置:

若晶胞边长为apm,阿伏加德罗常数的值为NA,晶体的密度为
②上述晶胞沿体对角线方向的投影图为
A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】氨硼烷是一种特殊的化合物,分子式为 。氨硼烷在催化剂作用下水解释放氢气
。氨硼烷在催化剂作用下水解释放氢气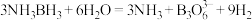 。
。 的结构如图。回答下列问题:
的结构如图。回答下列问题:_______
(2)写出 分子的电子式
分子的电子式_______
(3) 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(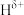 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(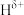 )。上述化学反应中,所含元素电负性由小到大的顺序为
)。上述化学反应中,所含元素电负性由小到大的顺序为_______ (填元素符号)
(4)有机碱离子 是
是 的等电子体,该离子与
的等电子体,该离子与 、
、 组成的光电材料,其晶胞如图所示:
组成的光电材料,其晶胞如图所示: 离子与
离子与 离子间的作用力为
离子间的作用力为_______ , 的配位数是
的配位数是_______ 。若晶胞参数为a pm,该晶体密度为ρ g⋅cm ,阿伏加德罗常数
,阿伏加德罗常数 可表示为
可表示为_______ mol (列出计算式)。
(列出计算式)。
 。氨硼烷在催化剂作用下水解释放氢气
。氨硼烷在催化剂作用下水解释放氢气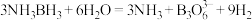 。
。 的结构如图。回答下列问题:
的结构如图。回答下列问题: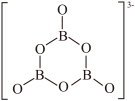
(2)写出
 分子的电子式
分子的电子式(3)
 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(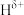 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(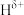 )。上述化学反应中,所含元素电负性由小到大的顺序为
)。上述化学反应中,所含元素电负性由小到大的顺序为(4)有机碱离子
 是
是 的等电子体,该离子与
的等电子体,该离子与 、
、 组成的光电材料,其晶胞如图所示:
组成的光电材料,其晶胞如图所示: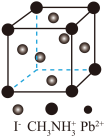
 离子与
离子与 离子间的作用力为
离子间的作用力为 的配位数是
的配位数是 ,阿伏加德罗常数
,阿伏加德罗常数 可表示为
可表示为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:
(1)基态P原子的价电子排布式为___ 。
(2)磷的一种同素异形体——白磷(P4)的空间构型为___ ,其键角为__ ,推测其在CS2中的溶解度___ (填“大于”或“小于”)在水中的溶解度。
(3)膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试用价层电子对互斥理论分析PH3的键角小于NH3的原因:___ 。
(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A、B的化学式分别为___ 、__ ,A的中心原子杂化轨道类型为___ 。

(5)第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素是__ (填元素符号)。
(6)氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如下表所示。试从结构的角度分析它们熔点不同的原因:__ 。
(1)基态P原子的价电子排布式为
(2)磷的一种同素异形体——白磷(P4)的空间构型为
(3)膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试用价层电子对互斥理论分析PH3的键角小于NH3的原因:
(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A、B的化学式分别为

(5)第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素是
(6)氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如下表所示。试从结构的角度分析它们熔点不同的原因:
| 物质 | BN | AlN | GaN |
| 熔点/℃ | 3000 | 2200 | 1700 |
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】Ⅰ.A,B,C分别代表三种不同的短周期元素,A原子的最外层电子排布为ns1,B原子的价电子排布为ns2np2,C原子的最外层电子数是其电子层数的3倍。
(1)若A原子的最外层电子排布为1s1,则按原子轨道的重迭方式判断,A与C形成的化合物中的共价键类型属于__ 键,A与C所形成的化合物的熔沸点明显高于A与C的同主族元素所形成的化合物的熔沸点,其原因是__ ;
(2)当n=2时,B与C形成的晶体属于__ 晶体,当n=3时,B与C形成的晶体中,B原子的杂化方式为__ ,微粒间的作用力是__ ;
Ⅱ.元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同.第四周期过渡元素的明显特征是形成多种多样的配合物。
(3)CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5]、羰基镍[Ni(CO)4],CO分子中C原子上有一对孤对电子,C,O原子都符合8电子稳定结构,CO的结构式为__ ,与CO互为等电子体的离子为__ (填化学式)。
(4)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,镓的基态原子的电子排布式是_______________ ,Ga的第一电离能却明显低于Zn,原因是_____________________ 。
(5)用价层电子对互斥理论预测H2Se和BBr3的立体结构,两个结论都正确的是__ 。
a.直线形;三角锥形 b.V形;三角锥形 c.直线形;平面三角形 d.V形;平面三角形
(1)若A原子的最外层电子排布为1s1,则按原子轨道的重迭方式判断,A与C形成的化合物中的共价键类型属于
(2)当n=2时,B与C形成的晶体属于
Ⅱ.元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同.第四周期过渡元素的明显特征是形成多种多样的配合物。
(3)CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5]、羰基镍[Ni(CO)4],CO分子中C原子上有一对孤对电子,C,O原子都符合8电子稳定结构,CO的结构式为
(4)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的,镓的基态原子的电子排布式是
(5)用价层电子对互斥理论预测H2Se和BBr3的立体结构,两个结论都正确的是
a.直线形;三角锥形 b.V形;三角锥形 c.直线形;平面三角形 d.V形;平面三角形
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】(1)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇的结构简式为 。请回答下列问题:
。请回答下列问题:
①基态镍原子的价电子排布式为________ 。
② 键,烯丙醇分子中碳原子的杂化类型是
键,烯丙醇分子中碳原子的杂化类型是__________ 。
(2)乙炔是有机合成的一种重要原料。实验室可用 与水反应得到乙炔。
与水反应得到乙炔。
①将乙炔通入 溶液中生成
溶液中生成 红棕色沉淀。基态
红棕色沉淀。基态 的核外电子排布式为
的核外电子排布式为____ 。
②乙炔与 反应可得丙烯腈(
反应可得丙烯腈( ),丙烯腈分子中碳原子的的杂化轨道类型是
),丙烯腈分子中碳原子的的杂化轨道类型是_______ ,分子中含有 键的数目为
键的数目为___________ 。
 。请回答下列问题:
。请回答下列问题:①基态镍原子的价电子排布式为
②
 键,烯丙醇分子中碳原子的杂化类型是
键,烯丙醇分子中碳原子的杂化类型是(2)乙炔是有机合成的一种重要原料。实验室可用
 与水反应得到乙炔。
与水反应得到乙炔。①将乙炔通入
 溶液中生成
溶液中生成 红棕色沉淀。基态
红棕色沉淀。基态 的核外电子排布式为
的核外电子排布式为②乙炔与
 反应可得丙烯腈(
反应可得丙烯腈( ),丙烯腈分子中碳原子的的杂化轨道类型是
),丙烯腈分子中碳原子的的杂化轨道类型是 键的数目为
键的数目为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】(1)下面列出了几组物质,请将正确的序号填写在空格上。
同位素__________ ,同系物__________ ,同素异形体__________ ,同分异构体__________ 。
①金刚石与“足球烯” ;②
;② 与
与 ; ③氧气
; ③氧气 与臭氧
与臭氧 ;④
;④  和
和 ;⑤
;⑤ 和CH3CH2CH2CH2CH3;⑥
和CH3CH2CH2CH2CH3;⑥ 和CH3CH2CH2CH2CH3
和CH3CH2CH2CH2CH3
请用下列几种物质的序号填空:
①Ar ②CO2 ③Na2O2 ④KOH ⑤MgBr2 ⑥NH4Cl ⑦H2SO4
只存在共价键的是__________ ,只存在离子键的是______________ ,既存在离子键又存在极性共价键的是____________ ,既存在离子键又存在非极性共价键的是___________ 。
(3)已知一定条件下,金刚石转化为石墨释放出能量,则等质量的金刚石比石墨具有的能量____ (填“高”、“低”),故金刚石比石墨稳定性_____ (填“强”、“弱”),等质量的金刚石和石墨充分燃烧均生成二氧化碳,______ 放出热量多
同位素
①金刚石与“足球烯”
 ;②
;② 与
与 ; ③氧气
; ③氧气 与臭氧
与臭氧 ;④
;④  和
和 ;⑤
;⑤ 和CH3CH2CH2CH2CH3;⑥
和CH3CH2CH2CH2CH3;⑥ 和CH3CH2CH2CH2CH3
和CH3CH2CH2CH2CH3请用下列几种物质的序号填空:
①Ar ②CO2 ③Na2O2 ④KOH ⑤MgBr2 ⑥NH4Cl ⑦H2SO4
只存在共价键的是
(3)已知一定条件下,金刚石转化为石墨释放出能量,则等质量的金刚石比石墨具有的能量
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】煤作为主要的能源物质,在国民生产和生活中起重要作用,但直接排放煤燃烧产生的烟气会引起严重的环境问题,将烟气通过装有石灰石(主要成分:CaCO3)浆液的脱硫装置可以除去其中的 SO2气体,最终生成硫酸钙。硫酸钙可在如图所示的循环燃烧装置的燃料反应器中与甲烷反应,气体产物分离出水后得到几乎不含杂质的二氧化碳,从而有利于 CO2的回收利用,达到减少碳排放的目的。
请回答下列问题:
(1)煤燃烧产生的烟气直接排放在空气中,不会引发的环境问题是(______ )
A. 温室效应 B. 酸雨 C. 粉层污染 D. 水体富营养化
(2)在烟气脱硫的过程中,所用的石灰石浆液在进入脱硫装置前,需通过一段时间的CO2,以增加脱硫效率;脱硫时控制浆液的pH值,此时浆液含有的Ca(HSO3)2可以快速被氧化为CaSO4。
①从分子结构看,CO2是由_____ 共价键构成的_____ 分子(选填:“极性”或“非极性”)。它与石灰石浆液反应的属于 _________ 反应。(选填“化合”、“分解”、“置换”、“复分解”),固体的CO2被称为干冰,其受热很容易_______ 。(填一种物理现象)
②Ca(HSO3)2从晶体类型看属于_____ 晶体,它溶于蒸馏水的电离方程式为______________________ ,它与足量氧气反应生成硫酸氢钙的化学方程式是_________________ 。用单线桥表示出反应物中电子转移的数目和方向:____________________ 。
③回收的CO2与酚羟基的钠盐在一定条件下反应,生成有机物M,其化学式为C7H5O3Na,M经过稀硫酸酸化后得到一种药物中间体N,N的结构简式为:
M的结构简式为________________ 除苯基外,药物中间体N所含的官能团还有______________ (填写“中文名称”)N在一定条件下可以经过自身缩聚形成一种高分子化合物,试写出形成高分子的化学反应:__________________ 。分子中无 -O-O- ,醛基与苯环直接相连的N的同分异构体共有_______ 种。

请回答下列问题:
(1)煤燃烧产生的烟气直接排放在空气中,不会引发的环境问题是(
A. 温室效应 B. 酸雨 C. 粉层污染 D. 水体富营养化
(2)在烟气脱硫的过程中,所用的石灰石浆液在进入脱硫装置前,需通过一段时间的CO2,以增加脱硫效率;脱硫时控制浆液的pH值,此时浆液含有的Ca(HSO3)2可以快速被氧化为CaSO4。
①从分子结构看,CO2是由
②Ca(HSO3)2从晶体类型看属于
③回收的CO2与酚羟基的钠盐在一定条件下反应,生成有机物M,其化学式为C7H5O3Na,M经过稀硫酸酸化后得到一种药物中间体N,N的结构简式为:

M的结构简式为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】
(1)①NH3分子的空间构型是_______________ ;
②化合物NF3为______ 分子(填“极性”或“非极性”),若其沸点为-129 ℃,则其晶体类型为_______ 。
(2)已知尿素的结构式为: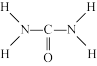 ,
,
①基态氮原子的价电子排布图是_________________ 。
②其中C、N、O三种元素的电负性由大到小顺序是________________________ 。
③尿素分子中C和N原子的杂化方式分别是____________ 、_______________ 。
(3)①肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。N2H4分子的电子式为___________ 。
②肼可用作火箭燃料, 肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在____________ (填标号)
a.离子键 b.共价键 c.配位键 d.范德华力
(1)①NH3分子的空间构型是
②化合物NF3为
(2)已知尿素的结构式为:
 ,
,①基态氮原子的价电子排布图是
②其中C、N、O三种元素的电负性由大到小顺序是
③尿素分子中C和N原子的杂化方式分别是
(3)①肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。N2H4分子的电子式为
②肼可用作火箭燃料, 肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在
a.离子键 b.共价键 c.配位键 d.范德华力
您最近一年使用:0次



