几种短周期主族元素在周期表中的位置如表,请回答下列问题:

(1)实验室可用dj2洗涤残留在试管中j单质,写出dj2的电子式___________ 。
(2)e、f、g三种元素简单气态氢化物的稳定性由弱到强的顺序为___________ (用化学式表示)。
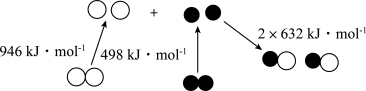
(3)1molf元素的单质和1molg元素的单质完全反应生成fg,其能量变化如图所示,会___________ (填“吸收”或“放出”)___________ kJ能量。
(4)f的简单气态氢化物是一种优良的小分子储氢载体,实验室制备该氢化物的化学方程式是:___________ 。
(5)用如图装置证明酸性: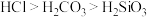 ,则溶液b为
,则溶液b为___________ 。下列事实不能用于比较C与Cl两元素非金属性相对强弱的是___________ (填序号)。
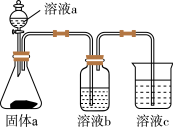
A.最高正化合价Cl>C
B.Cl的氢化物比C的简单氢化物稳定
C.Cl的氢化物比C的简单氢化物沸点高
D.最高价氧化物对应的水化物的酸性: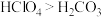

(1)实验室可用dj2洗涤残留在试管中j单质,写出dj2的电子式
(2)e、f、g三种元素简单气态氢化物的稳定性由弱到强的顺序为
(3)1molf元素的单质和1molg元素的单质完全反应生成fg,其能量变化如图所示,会

(4)f的简单气态氢化物是一种优良的小分子储氢载体,实验室制备该氢化物的化学方程式是:
(5)用如图装置证明酸性:
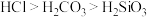 ,则溶液b为
,则溶液b为
A.最高正化合价Cl>C
B.Cl的氢化物比C的简单氢化物稳定
C.Cl的氢化物比C的简单氢化物沸点高
D.最高价氧化物对应的水化物的酸性:
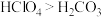
更新时间:2023-05-01 22:13:40
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】莽草酸能够通过抑制血小板聚集、防止脑血栓的形成,下图是合成莽草酸的路线(部分反应条件和步骤已略去),回答下列问题。___________ ,该物质可发生加聚反应,其产物的结构简式为___________ 。
(2)物质D中含氧官能团的名称为___________ 。
(3)莽草酸的化学式为___________ ,莽草酸与足量NaOH溶液反应的化学方程式为___________ 。
(4)一定条件下莽草酸与酸R可生成酯(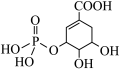 ),根据酯化反应原理可知酸R为
),根据酯化反应原理可知酸R为___________ (写化学式)。
(5)A与 发生加成反应的产物M与G互为同系物,G的相对分子质量比M大28.则符合条件的G有
发生加成反应的产物M与G互为同系物,G的相对分子质量比M大28.则符合条件的G有___________ 种。

已知:在有机化学中也可用键线式表示有机物的结构,如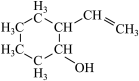 可简写为
可简写为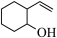
(2)物质D中含氧官能团的名称为
(3)莽草酸的化学式为
(4)一定条件下莽草酸与酸R可生成酯(
 ),根据酯化反应原理可知酸R为
),根据酯化反应原理可知酸R为(5)A与
 发生加成反应的产物M与G互为同系物,G的相对分子质量比M大28.则符合条件的G有
发生加成反应的产物M与G互为同系物,G的相对分子质量比M大28.则符合条件的G有
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】现有部分短周期元素的原子结构如下表:
(1)写出X的元素符号:___________ ,元素Y位于元素周期表第___________ 周期第___________ 族,请写出YW2的电子式___________ 。
(2)Z元素原子的质量数为___________ ,用电子式表示Z2W2的形成过程___________ 。
(3)X和Z两种元素的最高价氧化物对应的水化物相互反应的离子方程式___________ 。
| 元素符号 | 元素原子结构 |
| X | 原子结构示意图为 |
| Y | 最外层电子数是次外层电子数的2倍 |
| Z | 原子核内含有12个中子,且其离子的结构示意图为 |
| W | W2-离子结构与Ne电子结构相同 |
(2)Z元素原子的质量数为
(3)X和Z两种元素的最高价氧化物对应的水化物相互反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】我国科学家合成了一种新化合物,结构式如图所示。已知M、X、Y、Z、W、Q均为前20号主族元素,且原子序数依次增大,其中Q与M、Z与Y同主族;Z元素原子中的质子数是Y元素原子中的质子数的2倍。
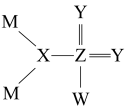
回答下列问题:
(1)写出W的离子结构示意图_______ 。
(2)Z、Q两种元素最简单离子半径的大小顺序为_______ (用离子符号表示)。
(3)X元素与氢原子按个数比1∶2形成的含18个电子的化合物的电子式为_______ 。写出实验室制取该元素简单氢化物的化学方程式_______ 。
(4)Q元素单质与金属钠性质相似,则Q的过氧化物与水反应的离子方程式_______ 。
(5)比较Z、W原子的得电子能力强弱。
方法一:比较Z、W两种元素最高价氧化物对应水化物的酸性强弱_______ (用化学式回答);
方法二:比较单质的氧化性强弱,设计实验证明(请简述试剂、操作、现象、结论):_______ 。

回答下列问题:
(1)写出W的离子结构示意图
(2)Z、Q两种元素最简单离子半径的大小顺序为
(3)X元素与氢原子按个数比1∶2形成的含18个电子的化合物的电子式为
(4)Q元素单质与金属钠性质相似,则Q的过氧化物与水反应的离子方程式
(5)比较Z、W原子的得电子能力强弱。
方法一:比较Z、W两种元素最高价氧化物对应水化物的酸性强弱
方法二:比较单质的氧化性强弱,设计实验证明(请简述试剂、操作、现象、结论):
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐1】工业合成氨反应为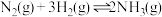 ,氨在工农业生产中应用广泛。
,氨在工农业生产中应用广泛。
(1)已知:键能是1mol化学键完全断裂形成气态原子所需要吸收的能量,部分化学键的键能如表格所示。计算每合成2mol 需要
需要_______ (填“放出”或“吸收”)kJ的热量。
(2)实验室中模拟合成氨过程,将1mol 和2.7mol
和2.7mol 置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是
置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是_______ (填序号)。
a.反应不再进行,已经停止 b.单位时间内生成nmol 的同时,生成3nmol
的同时,生成3nmol
c.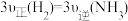 d.
d. 、
、 和
和 的物质的量浓度之比为1:3:2
的物质的量浓度之比为1:3:2
e.混合气体的压强不再改变 f.混合气体的密度不再改变
若10min时测得氢气浓度为1.2 mol∙L−1,则用氨气表示的0~10min内的平均化学反应速率为_______ ;10min时的体系总压强与初始时的总压强之比为_______ 。
(3)工业合成氨过程中,按一定投料比将原料气以及催化剂置于反应容器中,测得在不同温度和压强下达到化学平衡状态时的氨的平衡含量(%)如表格所示:
实际生产时,通常采用铁触媒作为催化剂、在400~500℃和10~30MPa的条件下合成氨。结合所学知识以及上述表格数据分析,工业上采用400~500℃反应的原因是_______ 。
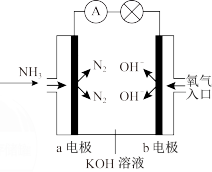
(4)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池的工作原理如图所示。a电极的电极反应式是_______ 。
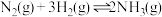 ,氨在工农业生产中应用广泛。
,氨在工农业生产中应用广泛。| 化学键 | H−H | N−H | N≡N |
键能( ) ) | 436 | 391 | 945.6 |
 需要
需要(2)实验室中模拟合成氨过程,将1mol
 和2.7mol
和2.7mol 置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是
置于恒温、体积为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是a.反应不再进行,已经停止 b.单位时间内生成nmol
 的同时,生成3nmol
的同时,生成3nmol
c.
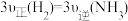 d.
d. 、
、 和
和 的物质的量浓度之比为1:3:2
的物质的量浓度之比为1:3:2e.混合气体的压强不再改变 f.混合气体的密度不再改变
若10min时测得氢气浓度为1.2 mol∙L−1,则用氨气表示的0~10min内的平均化学反应速率为
(3)工业合成氨过程中,按一定投料比将原料气以及催化剂置于反应容器中,测得在不同温度和压强下达到化学平衡状态时的氨的平衡含量(%)如表格所示:
| 压强(MPa) 氨的平衡 含量(%) 温度(摄氏度) | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
(4)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池的工作原理如图所示。a电极的电极反应式是

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】I.理论上讲,任何自发的氧化还原反应都可以设计成原电池。某同学利用“Cu+2Ag+=2Ag+Cu2+”反应设制一个化学电池,如图所示,已知该电池在外电路中,电流从a极流向b极。请回答下列问题:
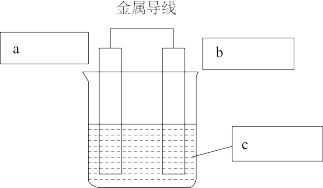
(1)b极是电池的____ 极,材料是____ ,写出该电极的反应式____ 。
(2)a可以为____ 。
(3)c溶液是___ 。
A.CuSO4溶液 B.AgNO3溶液 C.酒精溶液
(4)若该反应过程中有0.2mol电子发生转移,则生成Ag为___ 克。
II.已知12g石墨转变为12g金刚石需吸收能量。
(5)①上述变化属于____ (填“物理”或“化学”)变化。
②常温常压下,石墨与金刚石更稳定的是____ 。
(6)如图是反应H2(g)+I2(g) 2HI(g)过程中的能量变化图。由图可知,反应物断键
2HI(g)过程中的能量变化图。由图可知,反应物断键____ (填“>”、“<”或“=”)生成物的总键能。


(1)b极是电池的
(2)a可以为
| A.铜 | B.银 | C.铁 | D.石墨 |
A.CuSO4溶液 B.AgNO3溶液 C.酒精溶液
(4)若该反应过程中有0.2mol电子发生转移,则生成Ag为
II.已知12g石墨转变为12g金刚石需吸收能量。
(5)①上述变化属于
②常温常压下,石墨与金刚石更稳定的是
(6)如图是反应H2(g)+I2(g)
 2HI(g)过程中的能量变化图。由图可知,反应物断键
2HI(g)过程中的能量变化图。由图可知,反应物断键
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】甲醇(CH3OH)是一种无色液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
(1)已知:2CH3OH(g)+O2(g)⇌2CO2(g)+4H2(g)的能量变化如图所示,下列说法正确的是_____ 。(填字母)
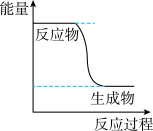
a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学反应不仅有新物质生成,同时也一定伴随能量变化
d.2mol甲醇和1mol氧气的总键能大于2mol二氧化碳和4mol氢气的总键能
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.4mol/L。则4min内平均反应速率v(H2)=_____ ,CH3OH的转化率为______ 。(转化率=某反应物转化浓度与该反应物起始浓度的百分比)
(3)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、氧气和KOH溶液构成。该燃料电池的总反应为CH3OH+O2+KOH=K2CO3+H2O(未配平)。回答下列问题:
①该电池的正极反应物为______ 。
②负极的电极反应式为_____ 。
(1)已知:2CH3OH(g)+O2(g)⇌2CO2(g)+4H2(g)的能量变化如图所示,下列说法正确的是

a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学反应不仅有新物质生成,同时也一定伴随能量变化
d.2mol甲醇和1mol氧气的总键能大于2mol二氧化碳和4mol氢气的总键能
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.4mol/L。则4min内平均反应速率v(H2)=
(3)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、氧气和KOH溶液构成。该燃料电池的总反应为CH3OH+O2+KOH=K2CO3+H2O(未配平)。回答下列问题:
①该电池的正极反应物为
②负极的电极反应式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是元素周期表短周期的一部分
(1)①-⑦元素中金属性最强的元素位于周期表中的位置为______________________ 。
(2)③与⑤形成的化合物溶于水会剧烈反应生成白色沉淀和气体A,请写出该反应的化学方程式__________ 。
(3)④所形成的单质与水反应的化学方程式为_____________ 。
(4)②、③、⑦的最高价含氧酸的酸性由弱到强的顺序是__________________ (用化学式表示);④所在族的各元素与氢气化合所形成的气态氢化物稳定性由强到弱的顺序是(用化学式表示)__________________ 。
(5)表中元素⑥的最高价氧化物与少量的KOH溶液反应的离子方程式为_____________ 。
| ① | ||||||||
| ② | ③ | ④ | ||||||
| ⑤ | ⑥ | ⑦ | ⑧ | |||||
(2)③与⑤形成的化合物溶于水会剧烈反应生成白色沉淀和气体A,请写出该反应的化学方程式
(3)④所形成的单质与水反应的化学方程式为
(4)②、③、⑦的最高价含氧酸的酸性由弱到强的顺序是
(5)表中元素⑥的最高价氧化物与少量的KOH溶液反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表是元素周期表的一部分,表中的每个编号代表一种元素。请根据要求回答问题:
(1)元素①③④组成的化合物的电子式是___________ ,其属于___________ (填“离子化合物”或“共价化合物”)。
(2)元素⑤的离子结构示意图是___________ ;元素⑩的单质常温下为___________ 的液体(填颜色)。
(3)元素③⑥⑨的非金属性比较:___________ (填化学式,下同);元素②③⑦的原子半径比较:___________ 。元素⑥⑨的氢化物稳定性比较:___________ 。
(4)元素①③⑦可组成酸性强于硫酸的强酸,其化学式为___________ 。
(5)元素⑧的单质与水反应的化学方程式为___________ 。
| 族 周期 | IA | ⅡA | ⅢB~ⅡB | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ||||||||
| 2 | ② | ③ | |||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | |||||
| 4 | ⑧ | ⑨Se | ⑩Br |
(2)元素⑤的离子结构示意图是
(3)元素③⑥⑨的非金属性比较:
(4)元素①③⑦可组成酸性强于硫酸的强酸,其化学式为
(5)元素⑧的单质与水反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】元素周期表揭示了元素之间的内在联系,使元素构成了一个较为系统的体系.请回答下列问题:
Ⅰ.元素周期表的建立与完善是一个渐进的过程.直至20世纪初,原子结构奥秘被揭示后,元素周期表中元素的排序由依据相对原子质量改为依据原子的_______ 。按照元素在周期表中的顺序给元素编号,得到原子序数。人们发现原子序数与元素的原子结构之间存在如下关系:原子序数=_______ =核外电子数
Ⅱ.图为元素周期表的一部分,序号①~⑥分别代表周期表中相应位置的种元素。
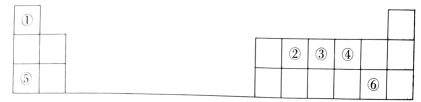
(1)②、③、④三种元素中,原子半径由大到小的顺序为_______ (用元素符号表示)。
(2)①、④、⑤三种元素形成的化合物的电子式为_______ ,该化合物中化学键的类型有_______ 。
(3)元素Q位于第四周期,且与元素⑥均为同一主族元素。请用离子方程说明⑥和Q两种元素单质氧化性的强弱:_______ 。根据元素周期律推测,下列性质中Q不可能具有的是_______ (填选项字母)。
A.最高正化合价为 B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
Ⅰ.元素周期表的建立与完善是一个渐进的过程.直至20世纪初,原子结构奥秘被揭示后,元素周期表中元素的排序由依据相对原子质量改为依据原子的
Ⅱ.图为元素周期表的一部分,序号①~⑥分别代表周期表中相应位置的种元素。

(1)②、③、④三种元素中,原子半径由大到小的顺序为
(2)①、④、⑤三种元素形成的化合物的电子式为
(3)元素Q位于第四周期,且与元素⑥均为同一主族元素。请用离子方程说明⑥和Q两种元素单质氧化性的强弱:
A.最高正化合价为
 B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检查)。
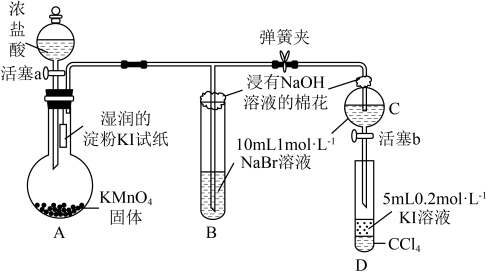
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)验证氯气的氧化性强于碘的实验现象是_____________________________________ 。
(2)B中溶液发生反应的离子方程式是_________________________________________ 。
(3)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是___________________ 。
(4)过程Ⅲ实验的目的是___________________________________________________ 。
(5)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下____________________ ,得电子能力逐渐减弱。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)验证氯气的氧化性强于碘的实验现象是
(2)B中溶液发生反应的离子方程式是
(3)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是
(4)过程Ⅲ实验的目的是
(5)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】已知非金属单质硫 是淡黄色固体粉末,难溶于水。为了验证氯元素与硫元素的非金属性强弱,某化学实验小组设计了如图实验。回答下列问题:
是淡黄色固体粉末,难溶于水。为了验证氯元素与硫元素的非金属性强弱,某化学实验小组设计了如图实验。回答下列问题:___________ 。
(2)装置A用于制取___________ (填“ ”或“
”或“ ”)。
”)。
(3)装置B中的实验现象为___________ 。
(4)装置C用于尾气处理,盛放的 溶液的溶质为
溶液的溶质为___________ (填“ ”或“
”或“ ”)。
”)。
(5)实验验证了非金属性:氯元素___________ (填“强于”或“弱于”)硫元素。
 是淡黄色固体粉末,难溶于水。为了验证氯元素与硫元素的非金属性强弱,某化学实验小组设计了如图实验。回答下列问题:
是淡黄色固体粉末,难溶于水。为了验证氯元素与硫元素的非金属性强弱,某化学实验小组设计了如图实验。回答下列问题:
(2)装置A用于制取
 ”或“
”或“ ”)。
”)。(3)装置B中的实验现象为
(4)装置C用于尾气处理,盛放的
 溶液的溶质为
溶液的溶质为 ”或“
”或“ ”)。
”)。(5)实验验证了非金属性:氯元素
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】在复习元素周期律过程中,某研究性学习小组的几位同学拟通过具体的实验来探讨某些金属元素的性质差异,下面是他们设计的探究性实验方案,请填写下列空白:
(1)实验目的:比较钠、镁、铝金属性强弱。
(2)实验用品:酒精灯、______ 、试管、试管夹、砂纸、滤纸;
钠、镁条、铝片、酚酞、蒸馏水、6 mol·L-1的盐酸
(3)实验过程与现象记录
Ⅰ.甲同学的方案如下:
①你认为a、b两步实验中出现异常现象的可能原因是:
a_______________________________________ ;
b___________________________________________ 。
②上面的实验表明:钠、镁、铝三种元素的金属性由强到弱的顺序为____________________ 。
Ⅱ乙同学的方案:他认为只需要一种试剂就可以确定钠、镁、铝的金属性强弱,预计他的主要实验操作是____________________ 。
(1)实验目的:比较钠、镁、铝金属性强弱。
(2)实验用品:酒精灯、
钠、镁条、铝片、酚酞、蒸馏水、6 mol·L-1的盐酸
(3)实验过程与现象记录
Ⅰ.甲同学的方案如下:
| 实验过程 | 预期现象 | 实际观察到的现象 |
| a取已切去表皮的一小块金属钠,放入盛有水的某容器中 | 立即剧烈反应 | 开始时钠块浮在水面上不反应,稍后才开始与水剧烈反应 |
| b向盛有适量水(内含2滴 酚酞的试管中加入一小段镁条 | 有气泡产生,溶液变红色 | 没有相应现象,加热后仍无明显变化 |
| c向两支盛有3mL6mol·L-1盐酸的试管中加入大小相同的镁片和铝片 | 镁、铝与盐酸反应产生气泡剧烈程度不同 | 镁与盐酸反应产生气泡速率较快 |
①你认为a、b两步实验中出现异常现象的可能原因是:
a
b
②上面的实验表明:钠、镁、铝三种元素的金属性由强到弱的顺序为
Ⅱ乙同学的方案:他认为只需要一种试剂就可以确定钠、镁、铝的金属性强弱,预计他的主要实验操作是
您最近一年使用:0次



