为了探究某固体化合物M(仅含两种元素)的组成和性质,设计并完成如图实验(假设各步反应均完全,反应中气体完全逸出):
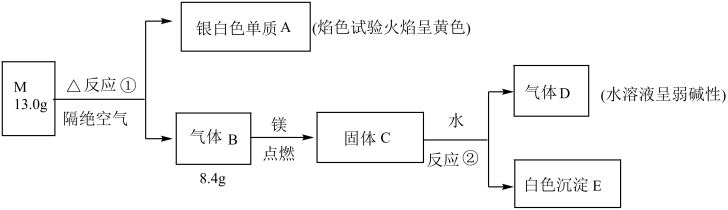
请回答:
(1)组成固体M的元素是___________ (填元素符号);
(2)白色沉淀E中所含化学键类型为___________ ;
(3)反应①的化学反应方程式为___________ 。

请回答:
(1)组成固体M的元素是
(2)白色沉淀E中所含化学键类型为
(3)反应①的化学反应方程式为
更新时间:2023-04-21 09:44:46
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】物质间有下列转代关系:
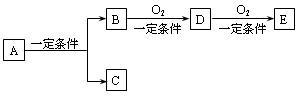
(1)若C是可用于自来水消毒的气体,D、E是氧化物,D转化为E时增加氧的质量是D的质量的25.8%,则A是____________ (写化学式)并写出A在一定条件下生成的C的化学方程式_______________________________ 。
(2)若E是酸酐,且为无色易挥发的晶体,A为气态氢化物,则A与D反应生成B的化学方程式为_______________________ 。
(3)若C是水,B是无氧化合物,B在同系物中是相对分子质量最小的化合物;工业上用B与C在催化剂条件下制取A,A为常见的一种燃料。E能使紫色石蕊试液显红色,则由D生成E的反应类型为_________________ 。A、B、D、E中能与水形成氢键而易溶于水的是_____________________ (写结构简式)

(1)若C是可用于自来水消毒的气体,D、E是氧化物,D转化为E时增加氧的质量是D的质量的25.8%,则A是
(2)若E是酸酐,且为无色易挥发的晶体,A为气态氢化物,则A与D反应生成B的化学方程式为
(3)若C是水,B是无氧化合物,B在同系物中是相对分子质量最小的化合物;工业上用B与C在催化剂条件下制取A,A为常见的一种燃料。E能使紫色石蕊试液显红色,则由D生成E的反应类型为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】将晶体X加热分解,可得A、B、D、E、F和H2O六种产物,其中A、B、D都是中学化学中常见的氧化物,气体E是单质F所含元素的氢化物。
(1) A能溶于强酸、强碱,写出A与强碱溶液反应的离子方程式:________________________ 。
(2)B、D都是酸性氧化物且组成元素相同,D溶于水得强酸,则B、D分子中除氧元素外所含另一种元素在元素周期表中的位置是____________________ 。
(3)E能使湿润的红色石蕊试纸变蓝,E的结构式为__________________ ,工业制取E气体的化学方程式为___________________________ 。
(4)由各分解产物的物质的量之比推测X的组成类似于明矾,若向X的浓溶液中滴加浓NaOH溶液至过量,现象依次为____________________ 、____________________ 、__________________ 。
(5)取一定量的X晶体分解,若生成0.1mol F,则必同时生成____________ (填化学式)________ mol。
(1) A能溶于强酸、强碱,写出A与强碱溶液反应的离子方程式:
(2)B、D都是酸性氧化物且组成元素相同,D溶于水得强酸,则B、D分子中除氧元素外所含另一种元素在元素周期表中的位置是
(3)E能使湿润的红色石蕊试纸变蓝,E的结构式为
(4)由各分解产物的物质的量之比推测X的组成类似于明矾,若向X的浓溶液中滴加浓NaOH溶液至过量,现象依次为
(5)取一定量的X晶体分解,若生成0.1mol F,则必同时生成
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】化合物A为一种常见金属元素与一种常见非金属元素组成的化合物,阳离子与阴离子的个数比为2:3。K为常见固态非金属单质,J为常见气态单质。其余为化合物,其中I、F在常温下为液态,C、D为刺激性气体,H无色无味气体,B为白色胶状沉淀,L为氯碱工业中的常见产品。F的浓溶液与K加热可生成D和H。(部分生成物未标出)
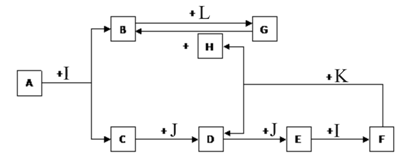
(1)写出下列物质的化学式:E_____________ J_____________
(2)写出D通入足量稀Ba(NO3)2溶液反应的化学方程式:_______________________
(3)银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故,根据电化学原理可进行如下处理,在Al制容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去,写出该反应的离子方程式_____________
(4)A电池性能优越,A-AgO电池可用作水下动力电源,其原理如图所示.该电池反应的化学方程式为:2A+3AgO+2NaOH=2NaAO2+3Ag+H2O,下列说法正确的是_____
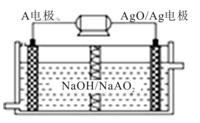
A.该隔膜是阳离子交换膜
B.当电极上析出1.08 g Ag时,电路中转移的电子为0.01 mol
C.A电极的反应式为:A-3e-+4OH-=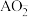 +2H2O
+2H2O
D.正极的电极反应式为:O2+2H2O+4e-=4OH-

(1)写出下列物质的化学式:E
(2)写出D通入足量稀Ba(NO3)2溶液反应的化学方程式:
(3)银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故,根据电化学原理可进行如下处理,在Al制容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去,写出该反应的离子方程式
(4)A电池性能优越,A-AgO电池可用作水下动力电源,其原理如图所示.该电池反应的化学方程式为:2A+3AgO+2NaOH=2NaAO2+3Ag+H2O,下列说法正确的是

A.该隔膜是阳离子交换膜
B.当电极上析出1.08 g Ag时,电路中转移的电子为0.01 mol
C.A电极的反应式为:A-3e-+4OH-=
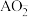 +2H2O
+2H2OD.正极的电极反应式为:O2+2H2O+4e-=4OH-
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。已知实验中可能会发生下列反应:①2Mg+O2 2MgO;②3Mg+N2
2MgO;②3Mg+N2 Mg3N2;
Mg3N2;
③2Mg+CO2 2MgO+C ④Mg+H2O
2MgO+C ④Mg+H2O MgO+H2↑ ⑤Mg3N2+6H2O =3Mg(OH)2+2NH3↑
MgO+H2↑ ⑤Mg3N2+6H2O =3Mg(OH)2+2NH3↑
可供选择的装置和药品如下页图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。
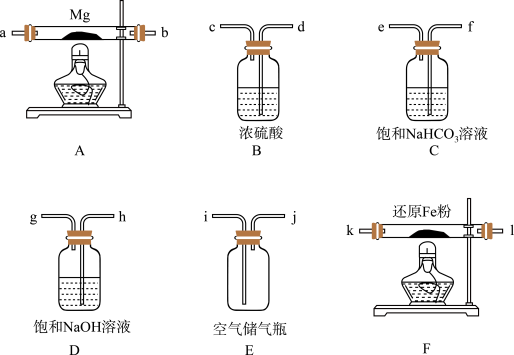
回答下列问题;
(1)在设计实验方案时,除装置A、E外,还应选择的装置(填字母代号)及其目的分别为(可不填满)
(2)连接并检查实验装置的气密性。实验开始时,打开自来水的开关,将空气从5升的储气瓶压入反应装置,则气流流经导管的顺序是(填字母代号)_______________________ ;
(3)通气后,应先点燃_______ 处的酒精灯,再点燃_______ 处的酒精灯;如果同时点燃A、F装置的酒精灯,对实验结果有何影响?_________________________ ;
(4)请设计一个实验,验证产物是Mg3N2,写出操作步骤、现象和结论:_____________ 。
 2MgO;②3Mg+N2
2MgO;②3Mg+N2 Mg3N2;
Mg3N2;③2Mg+CO2
 2MgO+C ④Mg+H2O
2MgO+C ④Mg+H2O MgO+H2↑ ⑤Mg3N2+6H2O =3Mg(OH)2+2NH3↑
MgO+H2↑ ⑤Mg3N2+6H2O =3Mg(OH)2+2NH3↑可供选择的装置和药品如下页图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。

回答下列问题;
(1)在设计实验方案时,除装置A、E外,还应选择的装置(填字母代号)及其目的分别为(可不填满)
| 装置 | 目的 |
(3)通气后,应先点燃
(4)请设计一个实验,验证产物是Mg3N2,写出操作步骤、现象和结论:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】制备氮化镁的装置示意图如下:
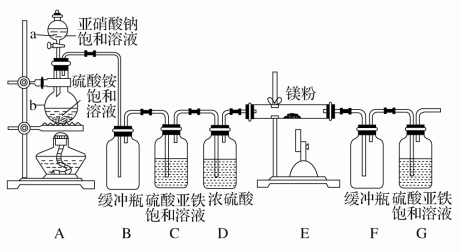
回答下列问题:
(1)检查装置气密性的方法是__________________________ ,
a的名称是________ ,b的名称是________ 。
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式_______________ 。
(3)C的作用是______________ ,D的作用是__________________ ,是否可以把C与D的位置对调并说明理由________________ 。
(4)写出E中发生反应的化学方程式________________________ 。

回答下列问题:
(1)检查装置气密性的方法是
a的名称是
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式
(3)C的作用是
(4)写出E中发生反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】Ⅰ.为探究无水盐X(仅含5种元素)的组成和性质,设计并完成如下实验:

请回答:
(1)组成X的5种元素符号是H、N___________ ;X的化学式是___________ 。
(2)写出向X溶液中加入足量的浓Ba(OH)2溶液并微热的离子方程式__________________________ 。
(3)写出检验X中金属阳离子的实验操作和现象:_________ 。
Ⅱ.钠、镁、铁是重要的金属元素。
(1)隔绝空气条件下,金属Na和Fe2O3粉末高温发生置换反应的化学方程式为:________
(2)化合物Mg (OH)2可作环保型阻燃材料,受热时按如下化学方程式分解:Mg (OH) 2 H2O↑+MgO,该化合物作阻燃剂的可能原因是
H2O↑+MgO,该化合物作阻燃剂的可能原因是____________ (填序号)
A.氢氧化镁易升华,降低温度
B.MgO固体覆盖在可燃物表面,隔绝空气
C.水蒸气稀释空气
D.生成的水高温分解吸热,降低温度

请回答:
(1)组成X的5种元素符号是H、N
(2)写出向X溶液中加入足量的浓Ba(OH)2溶液并微热的离子方程式
(3)写出检验X中金属阳离子的实验操作和现象:
Ⅱ.钠、镁、铁是重要的金属元素。
(1)隔绝空气条件下,金属Na和Fe2O3粉末高温发生置换反应的化学方程式为:
(2)化合物Mg (OH)2可作环保型阻燃材料,受热时按如下化学方程式分解:Mg (OH) 2
 H2O↑+MgO,该化合物作阻燃剂的可能原因是
H2O↑+MgO,该化合物作阻燃剂的可能原因是A.氢氧化镁易升华,降低温度
B.MgO固体覆盖在可燃物表面,隔绝空气
C.水蒸气稀释空气
D.生成的水高温分解吸热,降低温度
您最近一年使用:0次
【推荐2】I.物质X是由4种短周期元素组成的化合物,某兴趣小组对其开展探究实验。
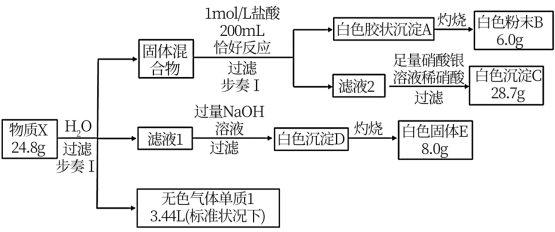
已知:①气体F在燃烧时产生淡蓝色火焰;
②滤液1与滤液2成分相同,且只含单一溶质。
请回答:
(1)组成X的非金属元素是__ (填元素符号),X的化学式是___ 。
(2)步骤I,发生的化学方程式是__ 。
(3)写出白色粉末B与NaOH溶液发生的离子方程式是__ 。
II.某同学用NaOH溶液同时吸收Cl2和SO2。经分析吸收液(强碱性)中存在Cl-和SO 。该同学认为溶液中还可能存在SO
。该同学认为溶液中还可能存在SO 、ClO-,请设计实验方案证明该同学的猜想:
、ClO-,请设计实验方案证明该同学的猜想:___ 。

已知:①气体F在燃烧时产生淡蓝色火焰;
②滤液1与滤液2成分相同,且只含单一溶质。
请回答:
(1)组成X的非金属元素是
(2)步骤I,发生的化学方程式是
(3)写出白色粉末B与NaOH溶液发生的离子方程式是
II.某同学用NaOH溶液同时吸收Cl2和SO2。经分析吸收液(强碱性)中存在Cl-和SO
 。该同学认为溶液中还可能存在SO
。该同学认为溶液中还可能存在SO 、ClO-,请设计实验方案证明该同学的猜想:
、ClO-,请设计实验方案证明该同学的猜想:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】已知A~O分别代表一种物质,它们之间的转化关系如下图所示(反应条件略去)。A、B、H分别是由短周期元素组成的单质。B元素为第三周期第IIA族。J常温下为液体。D是一种离子化合物,其阴阳离子的个数比为2:3,且能与水反应得到两种碱。C为淡黄色固体化合物,O能与G的水溶液反应生成蓝色沉淀。
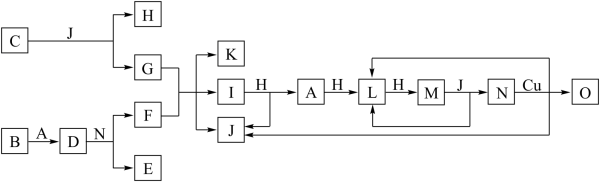
请回答下列问题:
(1)D为_______ 。(填化学式)
(2)I的沸点比PH3的沸点高,其原因是_______ 。
(3)写出I与H在点燃条件下反应生成A和J的化学方程式:_______ 。
(4)写出N与FeO反应的离子方程式:_______ 。
(5)F中阳离子的检验步骤是_______ 。

请回答下列问题:
(1)D为
(2)I的沸点比PH3的沸点高,其原因是
(3)写出I与H在点燃条件下反应生成A和J的化学方程式:
(4)写出N与FeO反应的离子方程式:
(5)F中阳离子的检验步骤是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】请根据以下信息答题:
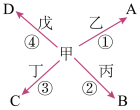
已知:I.图中,①②③④四个反应均为单质与单质在一定条件下的化合反应。
II.图中涉及的物质中除乙和A外均由短周期元素组成。
II. 丙与A在高温下反应能放出大量的热,生成B和乙,该反应能用于焊接钢轨。
IV.乙在甲中燃烧生成A,戊能在C中燃烧生成D和丁,C是一种常见的温室气体。且D中甲元素的质量分数为40%。
(1)请写出III对应的化学方程式:______ 。
(2)23.2gA溶于足量盐酸,得到的溶液与铜粉完全反应,至少需铜粉的质量为_____ 。
(3)丙与少量的NaOH溶液反应的离子方程式为______ 。
(4)C的电子式为___ ,它的空间结构是_____ 。

已知:I.图中,①②③④四个反应均为单质与单质在一定条件下的化合反应。
II.图中涉及的物质中除乙和A外均由短周期元素组成。
II. 丙与A在高温下反应能放出大量的热,生成B和乙,该反应能用于焊接钢轨。
IV.乙在甲中燃烧生成A,戊能在C中燃烧生成D和丁,C是一种常见的温室气体。且D中甲元素的质量分数为40%。
(1)请写出III对应的化学方程式:
(2)23.2gA溶于足量盐酸,得到的溶液与铜粉完全反应,至少需铜粉的质量为
(3)丙与少量的NaOH溶液反应的离子方程式为
(4)C的电子式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】短周期元素X、Y、Z、W、R原子序数依次增大,W原子次外层电子数比最外层电子数多2个,X与R同主族,其中部分元素的原子半径和主要化合价如下表所示:
请回答下列问题:
(1)W元素在元素周期表中的位置为___________ 。
(2)Y元素最高价氧化物水化物的溶液与Z的氧化物反应的离子方程式为___________ 。
(3)W、R元素最高价氧化物水化物的酸性较强的为___________ (用化学式表示),从原子结构角度解释原因___________ 。
(4)化合物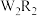 、
、 (所有原子均满足8电子结构)在工业生产中有广泛用途,
(所有原子均满足8电子结构)在工业生产中有广泛用途,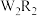 的电子式为
的电子式为___________ ;在一定条件下, 与
与 反应生成
反应生成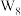 、
、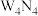 和一种仅由非金属元素组成的离子化合物,该离子化合物为
和一种仅由非金属元素组成的离子化合物,该离子化合物为___________ (填化学式)。
(5)化合物 可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等。
可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等。 与
与 反应生成两种单质(其中一种为黄绿色气体)和一种氢化物,则该反应的化学方程式为
反应生成两种单质(其中一种为黄绿色气体)和一种氢化物,则该反应的化学方程式为___________ 。
| N | X | Y | Z | |
| 原子半径/pm | 75 | 71 | 186 | 143 |
| 主要化合价 | / | —1 | +1 | +3 |
(1)W元素在元素周期表中的位置为
(2)Y元素最高价氧化物水化物的溶液与Z的氧化物反应的离子方程式为
(3)W、R元素最高价氧化物水化物的酸性较强的为
(4)化合物
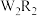 、
、 (所有原子均满足8电子结构)在工业生产中有广泛用途,
(所有原子均满足8电子结构)在工业生产中有广泛用途,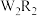 的电子式为
的电子式为 与
与 反应生成
反应生成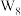 、
、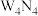 和一种仅由非金属元素组成的离子化合物,该离子化合物为
和一种仅由非金属元素组成的离子化合物,该离子化合物为(5)化合物
 可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等。
可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等。 与
与 反应生成两种单质(其中一种为黄绿色气体)和一种氢化物,则该反应的化学方程式为
反应生成两种单质(其中一种为黄绿色气体)和一种氢化物,则该反应的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如图转化关系,请完成下列问题:
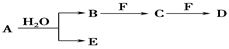
(1)若常温下A为有色气体。
①当F是一种金属单质时,请写出一定浓度的B溶液和适量F反应生成C与气体E的离子方程式:_________________ 。
②当C为直线形分子时,E具有漂白性,物质F焰色反应呈黄色,则C的电子式为________________ ;D中所含化学键的类型为____________________ 。
(2)若A为淡黄色固体,D为白色难溶于水的物质,且A和D的相对分子质量相等,请用离子方程式表示F的水溶液呈酸性的原因:_________________ 。
(3)若A中一种元素原子的最外层电子数为内层电子总数的 ,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:
,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:____________ ;B转化为C的化学方程式为______________ 。

(1)若常温下A为有色气体。
①当F是一种金属单质时,请写出一定浓度的B溶液和适量F反应生成C与气体E的离子方程式:
②当C为直线形分子时,E具有漂白性,物质F焰色反应呈黄色,则C的电子式为
(2)若A为淡黄色固体,D为白色难溶于水的物质,且A和D的相对分子质量相等,请用离子方程式表示F的水溶液呈酸性的原因:
(3)若A中一种元素原子的最外层电子数为内层电子总数的
 ,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:
,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:
您最近一年使用:0次




