下列有关分子结构与性质的叙述,正确的是
| A.BF3与PCl3的VSEPR模型均为正四面体形 |
| B.SO2与BeCl2分子均呈V形 |
| C.乙炔分子中碳原子采取sp杂化,分子中σ键与π键的数目之比为3:2 |
D.邻羟基苯甲醛( )的沸点比对羟基苯甲醛( )的沸点比对羟基苯甲醛( )的高 )的高 |
更新时间:2023-04-24 09:20:46
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】 晶体溶于水的过程中,破坏了
晶体溶于水的过程中,破坏了 晶体中的
晶体中的
 晶体溶于水的过程中,破坏了
晶体溶于水的过程中,破坏了 晶体中的
晶体中的| A.离子键 | B.共价键 | C.离子键和共价键 | D.范德华力 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知N-N、N=N、N≡N键能之比为1.00∶2.17∶4.90,而C-C,C=C,C≡C键能之比为1.00∶1.17∶2.34。下列有关叙述,不正确的是
| A.乙烯分子中σ键、π键的电子云形状对称性不同 |
| B.乙炔分子中π键重叠程度比σ键小,易发生加成反应 |
| C.氮分子中的N≡N键非常牢固,不易发生加成反应 |
| D.氮气和乙炔都易在空气中点燃燃烧 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】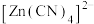 在水溶液中与HCHO发生如下反应:
在水溶液中与HCHO发生如下反应: 。下列说法正确的是
。下列说法正确的是
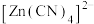 在水溶液中与HCHO发生如下反应:
在水溶液中与HCHO发生如下反应: 。下列说法正确的是
。下列说法正确的是| A.HCHO的分子构型是是三角锥形 |
B.基态 的电子排布式为 的电子排布式为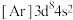 |
C.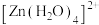 中与 中与 形成配位键的原子是H 形成配位键的原子是H |
D.1mol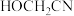 中所含 中所含 键的数目是6mol 键的数目是6mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏加德罗常数的值,下列说法正确的是
| A.1molNH4F晶体中含有共价键数目为3NA |
| B.0.5molXeF4中氙的价层电子对数为3NA |
| C.标况下,11.2LNO和11.2LO2混合后的分子数目为NA |
| D.46g乙醇中sp3杂化的原子数目为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】四氯化锗( )是光导纤维的常用掺杂剂,锗与硅同族。下列说法不正确的是
)是光导纤维的常用掺杂剂,锗与硅同族。下列说法不正确的是
 )是光导纤维的常用掺杂剂,锗与硅同族。下列说法不正确的是
)是光导纤维的常用掺杂剂,锗与硅同族。下列说法不正确的是A.基态 原子价层电子排布式为 原子价层电子排布式为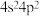 | B. 的熔点比 的熔点比 低 低 |
C. 的空间构型为正四面体 的空间构型为正四面体 | D.第一电离能大小: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】四种短周期元素X、Y、Z、W的原子序数依次增大,X的最外层电子数是次外层电子数的2倍,Y、W同主族且能形成两种常见的化合物,X、W质子数之和是Z质子数的2倍。则下列说法中正确 的是
| A.原子半径比较:X<Y<Z<W |
| B.X的氢化物沸点一定低于Y的氢化物 |
| C.Y的氢化物稳定性一定弱于W的氢化物 |
| D.短周期所有元素中,Z的最高价氧化物的水化物碱性最强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列各项比较中前者大于后者的是
| A.Na和Mg的熔点 |
B. 和 和 中心原子的价层电子对数 中心原子的价层电子对数 |
C. 和 和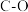 的键能 的键能 |
D.对羟基苯甲醛(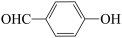 )和邻羟基苯甲醛( )和邻羟基苯甲醛(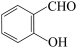 )的沸点 )的沸点 |
您最近一年使用:0次

 互为等电子体 ,且它们中心原子都是 sp3 杂化
互为等电子体 ,且它们中心原子都是 sp3 杂化

