氧化铈(CeO2)是一种重要的光催化材料,光催化过程中立方晶胞的组成变化如图所示。下列说法错误的是
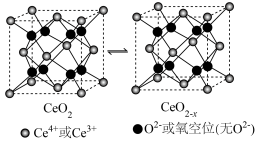

| A.氧元素位于元素周期表中的p区 |
| B.CeO2晶体中与Ce4+相邻且最近的Ce4+有12个 |
| C.O2-占据所有四面体空隙 |
| D.每个CeO2-x晶胞中Ce4+个数为1-2x |
更新时间:2023-04-24 08:38:51
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其 内层电子数的2倍,Y是地壳中含量最高的元素,W2+与Y2-具有相同的电子层结构,W与 X同主族。下列说法正确的是
| A.Y的气态简单氢化物的热稳定性比W的强 |
| B.Y分别与Z、W形成的化合物中化学键类型相同 |
| C.X的最高价氧化物对应的水化物的酸性比W的弱 |
| D.原子半径的大小顺序:K(W) > r(Z) > r(Y) > r(X) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】几种短周期元素的原子半径及主要化合价如下表:
下列说法正确的是
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径(×10-10 m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
| 主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | -- |
| 最低负价 | -- | -1 | -- | -- | -3 | -2 | |
| A.离子半径r(R3-)﹥r(X+)﹥r(Z3+) | B.元素X和Q形成的化合物中不可能含有共价键 |
| C.Q2-比R3-更容易失去电子 | D.Y的含氧酸的酸性一定比R的含氧酸的酸性强 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】某晶体由镁、铝、氧三种元素组成,若将其晶胞按图1方式切成8个体积相同的小立方体,Mg2+、Al3+和O2-在小立方体中的分布如图2、图3所示。已知Mg2+之间的最小间距为apm。下列说法错误的是
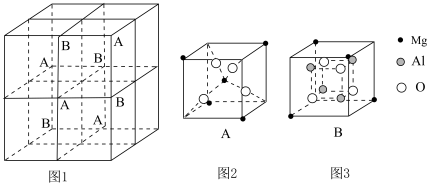
A.晶胞的体积为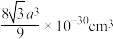 |
| B.晶体中Mg2+的配位数为4 |
| C.第一电离能:Al<Mg |
| D.晶胞中镁、铝离子个数比为1:2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】高压不仅会引发物质的相变,还会导致新类型化学键的形成。如图所示,M、N、P为Na与 在50~300GPa的高压下反应生成的不同晶体晶胞,下列说法错误的是
在50~300GPa的高压下反应生成的不同晶体晶胞,下列说法错误的是
 在50~300GPa的高压下反应生成的不同晶体晶胞,下列说法错误的是
在50~300GPa的高压下反应生成的不同晶体晶胞,下列说法错误的是
A.M、N、P晶体的化学式分别为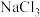 、 、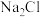 、 、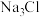 |
B.晶胞M、N、P中所含Cl原子的个数之比为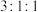 |
| C.晶胞M中与Na原子距离最近且等距的Cl原子有12个 |
D.1号的原子坐标为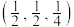 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】将钾离子嵌入石墨层可制得一种新型负极材料,图1为该负极材料的六方晶胞示意图。由于钾离子半径较大,在充放电过程中,会使石墨体积变化大而引起结构坍塌,导致容量快速衰减。
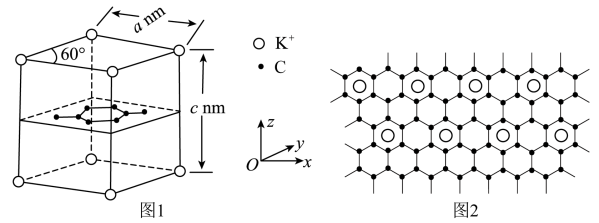
下列说法错误的是

下列说法错误的是
| A.与石墨相比,中空碳纳米管结构能提供更多的自由空间来适应充放电过程中的体积变化 |
| B.石墨晶体既存在共价键又存在范德华力,同时还存在类似金属键的作用力 |
C.该材料的密度为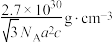 ( ( 表示阿伏加德罗常数的值) 表示阿伏加德罗常数的值) |
| D.图2可表示该材料沿z轴的局部投影图 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】根据如图所示,下列说法错误的是


| A.第三周期某元素的前5个电子的电离能如图1所示,则该元素是Mg |
| B.图2表示石墨晶体结构,石墨晶体既存在共价键又存在范德华力,属于混合型晶体 |
| C.图3所示是[Zn(NH3)6]2+的部分结构以及其中H-N-H键的键角,键角比NH3大的原因与NH3中N原子的孤电子对转化为成键电子对有关 |
D.立方BN晶体晶胞结构如图4所示,设晶胞中最近的B、N原子之间的距离为anm,阿伏加德罗常数的值为NA,则晶体的密度为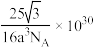 g·cm-3 g·cm-3 |
您最近一年使用:0次


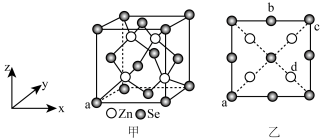
 的晶体结构呈立方体形,其晶胞侧视图及晶胞结构如图,下列说法错误的是
的晶体结构呈立方体形,其晶胞侧视图及晶胞结构如图,下列说法错误的是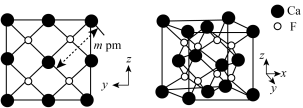

 最邻近的
最邻近的 数为4
数为4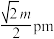

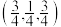
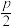 nm
nm

