我国磷资源储量丰富。回答下列问题:
(1)已知亚磷酸(H3PO3)为二元弱酸,写出亚磷酸与过量 反应的化学方程式
反应的化学方程式___________ ;
(2)磷酸为磷的最高价含氧酸,其空间结构如图1所示:
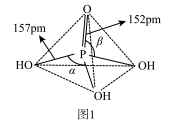
①键能大小比较:磷氧双键___________ (填“大于”“等于”或“小于”)磷氧单键。
②键角大小比较:
___________  (填“大于”“等于”或“小于”)。
(填“大于”“等于”或“小于”)。
③纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是___________ 。
(3)磷化硼(BP)是一种超硬耐磨涂层材料,其立方晶胞如图2所示
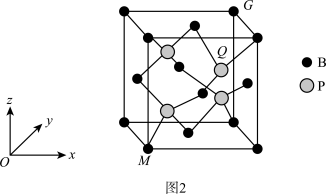
①固态磷化硼属于___________ (填“分子”“离子”或“共价”)晶体。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。已知原子分数坐标:M点为(0,0,0)、G点为(1,1,1),则Q点的原子分数坐标为___________ 。
③若晶胞参数为acm,则B与P之间的最短距离为___________ cm(用含a的代数式表示)。
(1)已知亚磷酸(H3PO3)为二元弱酸,写出亚磷酸与过量
 反应的化学方程式
反应的化学方程式(2)磷酸为磷的最高价含氧酸,其空间结构如图1所示:

①键能大小比较:磷氧双键
②键角大小比较:

 (填“大于”“等于”或“小于”)。
(填“大于”“等于”或“小于”)。③纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是
(3)磷化硼(BP)是一种超硬耐磨涂层材料,其立方晶胞如图2所示

①固态磷化硼属于
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。已知原子分数坐标:M点为(0,0,0)、G点为(1,1,1),则Q点的原子分数坐标为
③若晶胞参数为acm,则B与P之间的最短距离为
更新时间:2023-04-26 20:26:10
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】高氯酸三碳酰肼合镍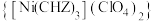 是一种新型的起爆药。设
是一种新型的起爆药。设 为阿伏加德罗常数的值。回答下列问题:
为阿伏加德罗常数的值。回答下列问题:
(1)基态 的电子排布式为
的电子排布式为___________ 。
(2)基态碳原子核外电子有___________ 种不同运动状态。
(3) 的中心原子的价层电子对数为
的中心原子的价层电子对数为________ , 的VSEPR模型是
的VSEPR模型是_________ 。
(4)上述化学式中的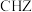 为碳酰肼,其结构为
为碳酰肼,其结构为 ,是一种新型的环保锅炉水除氧剂。
,是一种新型的环保锅炉水除氧剂。
①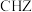 中氮原子的杂化轨道类型为
中氮原子的杂化轨道类型为___________ 。
②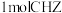 中含有的
中含有的 键数目为
键数目为___________  (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
③键角:
___________ (填“>”“<”或“=”) 。
。
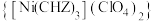 是一种新型的起爆药。设
是一种新型的起爆药。设 为阿伏加德罗常数的值。回答下列问题:
为阿伏加德罗常数的值。回答下列问题:(1)基态
 的电子排布式为
的电子排布式为(2)基态碳原子核外电子有
(3)
 的中心原子的价层电子对数为
的中心原子的价层电子对数为 的VSEPR模型是
的VSEPR模型是(4)上述化学式中的
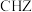 为碳酰肼,其结构为
为碳酰肼,其结构为 ,是一种新型的环保锅炉水除氧剂。
,是一种新型的环保锅炉水除氧剂。①
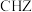 中氮原子的杂化轨道类型为
中氮原子的杂化轨道类型为②
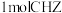 中含有的
中含有的 键数目为
键数目为 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。③键角:

 。
。
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】按要求填空。
(1)比较大小或强弱
①A.乙酸(CH3COOH)、B.三氟乙酸(CF3COOH)、C.三氯乙酸(CCl3COOH),它们的酸性由强到弱的顺序为_______ (用ABC字母作答,填汉字不给分,下同)。
②A.一氯乙烷(CH2ClCH3)、B.乙烷(CH3CH3)、C.乙醇(CH3CH2OH),它们的沸点由高到低的顺序为_______ 。
③A.丙三醇(CH2OHCHOHCH2OH)、B.丙醇(CH3CH2CH2OH)、C.丙烷(CH3CH2CH3),它们的水溶性由好到差的顺序为_______ 。
④A.SCl2、B.CS2、C.SO2,它们的键角由大到小的顺序为_______ 。
(2) 的空间结构为
的空间结构为_______ ,中心原子Cl的杂化类型为_______ 。
(3)有机物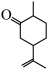 中,有
中,有_______ 个手性碳,1mol该有机物含π键的个数为_______ 。
(4)H2O的热稳定性比H2S好,沸点也比H2S高,原因是_______ 。
(1)比较大小或强弱
①A.乙酸(CH3COOH)、B.三氟乙酸(CF3COOH)、C.三氯乙酸(CCl3COOH),它们的酸性由强到弱的顺序为
②A.一氯乙烷(CH2ClCH3)、B.乙烷(CH3CH3)、C.乙醇(CH3CH2OH),它们的沸点由高到低的顺序为
③A.丙三醇(CH2OHCHOHCH2OH)、B.丙醇(CH3CH2CH2OH)、C.丙烷(CH3CH2CH3),它们的水溶性由好到差的顺序为
④A.SCl2、B.CS2、C.SO2,它们的键角由大到小的顺序为
(2)
 的空间结构为
的空间结构为(3)有机物
 中,有
中,有(4)H2O的热稳定性比H2S好,沸点也比H2S高,原因是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】硫和锌及其化合物用途广泛。回答下列问题:
(1)基态硫原子的价电子排布图为__________________ 。
(2)已知基态锌、铜的电离能如表所示:
由表格数据知,I2(Cu)>I2(Zn)的原因是____________________________________ 。
(3)H2O分子中的键长比H2S中的键长__________ (填“长”或“短”)。H2O分子的键角比H2S的键角大,其原因是____________________________________ 。
(4)S8与热的浓NaOH溶液反应的产物之一为Na2S3,S32-的空间构型为__________________ 。
(5)噻吩(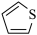 )广泛应用于合成医药、农药、染料工业。
)广泛应用于合成医药、农药、染料工业。
①噻吩分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ,则噻吩分子中的大π键应表示为
,则噻吩分子中的大π键应表示为______________ 。
②噻吩的沸点为84 ℃,吡咯(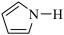 )的沸点在129~131 ℃之间,后者沸点较高,其原因是
)的沸点在129~131 ℃之间,后者沸点较高,其原因是____________________________ 。1 mol吡咯含__________ mol σ键。
(6)硫化锌是一种半导体材料,其晶胞结构如图所示。
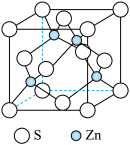
已知:硫化锌晶体密度为d g·cm-3,NA代表阿伏加 德罗常数的值,则Zn2+和S2-之间的最短核间距(x)为__________ nm(用代数式表示)。
(1)基态硫原子的价电子排布图为
(2)已知基态锌、铜的电离能如表所示:
| 电离能/kJ·mol1 | I1 | I2 |
| Cu | 746 | 1958 |
| Zn | 906 | 1733 |
(3)H2O分子中的键长比H2S中的键长
(4)S8与热的浓NaOH溶液反应的产物之一为Na2S3,S32-的空间构型为
(5)噻吩(
 )广泛应用于合成医药、农药、染料工业。
)广泛应用于合成医药、农药、染料工业。①噻吩分子中的大π键可用符号
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ,则噻吩分子中的大π键应表示为
,则噻吩分子中的大π键应表示为②噻吩的沸点为84 ℃,吡咯(
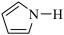 )的沸点在129~131 ℃之间,后者沸点较高,其原因是
)的沸点在129~131 ℃之间,后者沸点较高,其原因是(6)硫化锌是一种半导体材料,其晶胞结构如图所示。

已知:硫化锌晶体密度为d g·cm-3,NA代表阿伏加 德罗常数的值,则Zn2+和S2-之间的最短核间距(x)为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】短周期元素在自然界中比较常见,它们的化合物及其合金在社会生活中有着很重要的作用。请回答下列问题:
(1)硫代硫酸盐可用作浸金试剂。硫代硫酸根( )可看作是
)可看作是 中的一个O原子被S原子取代的产物。
中的一个O原子被S原子取代的产物。
①基态O原子的核外电子中,两种自旋状态的电子数之比为________ 。 的空间结构是
的空间结构是________ 。
②浸金时, 作为配体可提供孤电子对与
作为配体可提供孤电子对与 形成
形成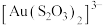 。分别判断
。分别判断 中的中心S原子和端基S原子能否做配位原子并说明理由:
中的中心S原子和端基S原子能否做配位原子并说明理由:_______ 。
(2)一定条件下,将F插入石墨层间可得到具有润滑性的层状结构化合物 ,其单层局部结构如图所示:
,其单层局部结构如图所示: 中C原子的杂化方式为
中C原子的杂化方式为________ ,与石墨相比, 的导电性将
的导电性将________ ,原因是________ 。

(3)①呋喃(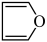 )和吡咯(
)和吡咯(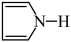 )均是重要化工原料,请解释呋喃沸点低于吡咯沸点的原因
)均是重要化工原料,请解释呋喃沸点低于吡咯沸点的原因_____ 。
②卤代乙酸可增强乙酸的酸性,则酸性:三氯乙酸( )
)___ 三氟乙酸( )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。
(4)Mg-Fe合金是当前储氢密度最高的储氢材料之一,其晶胞结构如图所示。
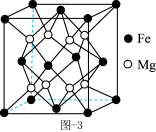
①距离Fe原子最近的Mg原子个数是_______ 。
②若该晶胞的棱长为a pm,阿伏加德罗常数的值为 ,则该合金的密度为
,则该合金的密度为______  。
。
(1)硫代硫酸盐可用作浸金试剂。硫代硫酸根(
 )可看作是
)可看作是 中的一个O原子被S原子取代的产物。
中的一个O原子被S原子取代的产物。①基态O原子的核外电子中,两种自旋状态的电子数之比为
 的空间结构是
的空间结构是②浸金时,
 作为配体可提供孤电子对与
作为配体可提供孤电子对与 形成
形成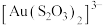 。分别判断
。分别判断 中的中心S原子和端基S原子能否做配位原子并说明理由:
中的中心S原子和端基S原子能否做配位原子并说明理由:(2)一定条件下,将F插入石墨层间可得到具有润滑性的层状结构化合物
 ,其单层局部结构如图所示:
,其单层局部结构如图所示: 中C原子的杂化方式为
中C原子的杂化方式为 的导电性将
的导电性将
(3)①呋喃(
 )和吡咯(
)和吡咯( )均是重要化工原料,请解释呋喃沸点低于吡咯沸点的原因
)均是重要化工原料,请解释呋喃沸点低于吡咯沸点的原因②卤代乙酸可增强乙酸的酸性,则酸性:三氯乙酸(
 )
) )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。(4)Mg-Fe合金是当前储氢密度最高的储氢材料之一,其晶胞结构如图所示。

①距离Fe原子最近的Mg原子个数是
②若该晶胞的棱长为a pm,阿伏加德罗常数的值为
 ,则该合金的密度为
,则该合金的密度为 。
。
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)A、B、C、D的第一电离能由小到大的顺序为____________________________________ 。
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是________________________ ;
(3)A的最高价含氧酸根离子中,其中心原子采取____________ 杂化,D的低价氧化物分子的空间构型是___________________________ 。
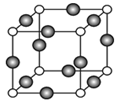
(4)A、E形成某种化合物的晶胞结构如图所示,则其化学式为________________ ;(每个球均表示1个原子) 若相邻A原子和E原子间的距离为a nm,阿伏伽德罗常数为NA,则该晶体的密度为_____________ g/cm3(用含a、NA的符号表示)。
(1)A、B、C、D的第一电离能由小到大的顺序为
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是
(3)A的最高价含氧酸根离子中,其中心原子采取
(4)A、E形成某种化合物的晶胞结构如图所示,则其化学式为

您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】[化学——选修3:物质结构与性质]
由H、C、O、N、S、Cu等元素能形成多种物质。这些物质有许多用途。请回答下列问题:
(1)基态Cu原子的价电子有____ 种运动状态,未成对电子占据原子轨道的形状为______ 。
(2)碳和氢形成的最简单碳正离子CH3+,其中心原子碳原子的杂化类型为___________ ,该阳离子的空间构型为___________ 。
(3)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是_________________________________ 。
(4)向盛有CuSO4溶液的试管中滴加少量氨水,现象是_____ ,离子反应方程式为____ ;继续滴加氨水至过量得到深蓝色溶液。经测定深蓝色是由于存在[Cu(NH3)4]SO4。其阳离子的结构式为___________ ,中心原子的配位数为___________ 。
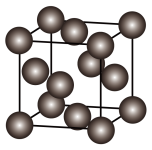
(5)金属晶体铜的晶胞如图所示。其堆积模型是___________ ,铜原子间的最短距离为apm,密度为ρg·cm-3,NA为阿伏伽德罗常数。铜的相对原子质量为___________ (用a、ρ、NA表示,写出计算式即可)。
由H、C、O、N、S、Cu等元素能形成多种物质。这些物质有许多用途。请回答下列问题:
(1)基态Cu原子的价电子有
(2)碳和氢形成的最简单碳正离子CH3+,其中心原子碳原子的杂化类型为
(3)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是
(4)向盛有CuSO4溶液的试管中滴加少量氨水,现象是
(5)金属晶体铜的晶胞如图所示。其堆积模型是

您最近一年使用:0次




