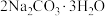 (过碳酸钠)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂。某兴趣小组制备过碳酸钠的实验方案如下:
(过碳酸钠)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂。某兴趣小组制备过碳酸钠的实验方案如下: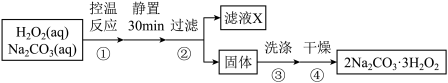
已知:
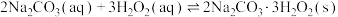 ,该反应速率大且放热多,50℃时,
,该反应速率大且放热多,50℃时,
 (s)开始分解。反应装置如图所示,下列说法错误的是
(s)开始分解。反应装置如图所示,下列说法错误的是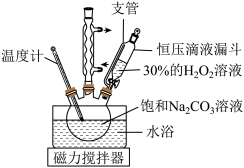
| A.制备过碳酸钠的关键是控制反应温度,该反应使用热水浴 |
| B.在滤液X中滴加无水乙醇可以提高产物的产率 |
C.球形冷凝管的作用是可以使 冷凝回流 冷凝回流 |
| D.使用过碳酸钠处理含有铁离子的污水时,其去污能力和杀菌作用会减弱 |
2023·河北沧州·二模 查看更多[3]
更新时间:2023-04-28 15:03:19
|
相似题推荐
单选题
|
适中
(0.65)
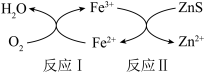
【推荐1】生物浸出是用细菌等微生物从固体中浸出金属离子,有速率快、浸出率高等特点。氧化亚铁硫杆菌是一类在酸性环境中加速 氧化的细菌,其浸出
氧化的细菌,其浸出 矿机理如图所示。下列说法错误的是
矿机理如图所示。下列说法错误的是
 氧化的细菌,其浸出
氧化的细菌,其浸出 矿机理如图所示。下列说法错误的是
矿机理如图所示。下列说法错误的是
A.温度过高或酸性过强时, 的浸出率均偏低 的浸出率均偏低 |
| B.反应Ⅱ可能有硫单质生成 |
C.反应Ⅰ的离子方程式为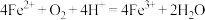 |
D.理论上浸出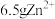 ,需要消耗 ,需要消耗 的体积为1.12L 的体积为1.12L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】Fe2(SO4)3可用作H2O2溶液分解的催化剂,其反应原理如图所示。常温下,向H2O2溶液中滴加少量Fe2(SO4)3溶液,反应原理如图所示。关于该反应过程的说法正确的是
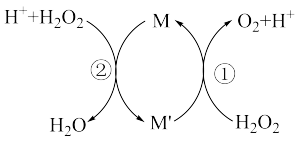

| A.该反应过程中,M是Fe3+,M′是Fe2+ | B.当有1molO2生成时,转移2mol电子 |
| C.在H2O2分解过程中,溶液的c(H+)不变 | D.H2O2的氧化性比Fe3+强,还原性比Fe2+弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】有关化学反应过程或实验现象的叙述中,正确的是
| A.氨气的水溶液可以导电,说明氨气是电解质 |
| B.漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 |
| C.氯气可以使湿润的有色布条褪色,说明氯气具有漂白作用 |
| D.在滴有酚酞的Na2CO3溶液中慢慢滴入BaCl2溶液,溶液的红色逐渐褪去 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】浓度相同的NaOH溶液各100 mL倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量的CO2,充分反应后,再向三份所得溶液中逐滴加入0.2 mol·L-1的盐酸,产生CO2的体积与所加盐酸体积之间的关系如图所示。下列判断不正确的是
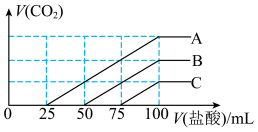

| A.原NaOH溶液的浓度为0.2 mol·L-1 |
| B.B烧杯中通入的CO2体积为448 mL(标准状况) |
| C.通入CO2后,A烧杯中的溶质为Na2CO3和NaHCO3 |
| D.通入CO2后,C烧杯中溶质成分的物质的量之比为n(NaOH)∶n(Na2CO3)=2∶1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】以二氧化钛表面覆盖Cu2Al2O4为催化剂,可将CO2和CH4直接转化成乙酸,如图为反应过程中催化剂的催化效率(实线)与乙酸的生成速率(虚线)随温度的变化情况。下列说法不正确的是
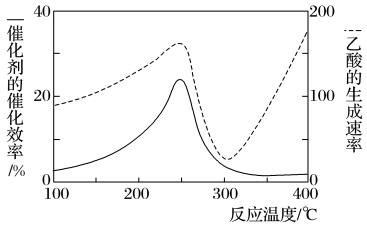

| A.该制备乙酸的反应中,原子利用率为100% |
| B.Cu2Al2O4写成氧化物的形式是Cu2O·Al2O3 |
| C.由图可知,工业上制备乙酸最适宜的温度应为250℃或者400℃ |
| D.250~300℃时,温度升高而乙酸的生成速率降低的主要原因是催化剂的催化效率降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在有关试剂的作用下,乙酸可通过两步反应得乙烷,反应原理如下:
①CH3COOH+2H2 CH3CH2OH+H2O
CH3CH2OH+H2O
②CH3CH2OH+H2 CH3CH3+H2O
CH3CH3+H2O
分别考查Mo16Ni6作用效果,某文献记载的数据如下:
下列叙述不正确的是
①CH3COOH+2H2
 CH3CH2OH+H2O
CH3CH2OH+H2O②CH3CH2OH+H2
 CH3CH3+H2O
CH3CH3+H2O分别考查Mo16Ni6作用效果,某文献记载的数据如下:
乙酸转化率 | 未反应的含氧化合物含量 | |||||
乙酸 | 乙醇 | |||||
温度/℃ | Mo16Ni6 | Ni6 | Mo16Ni6 | Ni6 | Mo16Ni6 | Ni6 |
240 | 87.2 | 21.8 | 0.53 | 3.24 | 1.03 | 0.14 |
260 | 89.1 | 27.2 | 0.45 | 3.02 | 0.99 | 0.19 |
| A.上述①②两反应均属于加成反应 |
| B.上述①②两反应中有机物均发生还原反应 |
| C.反应260℃比240℃进行更有利 |
| D.Mo16Ni6作用效果比Ni6好 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列从混合物中分离出其中的某一成分,所采取的分离方法正确的是
| A.根据CaO和BaSO4在水中溶解性不同,可以用溶于水再过滤的方法除去CaO中的BaSO4杂质 |
| B.除去KNO3溶液中的AgNO3杂质,可加入适量的NaCl溶液,再过滤即可 |
| C.利用氯化钾与碳酸钙的溶解性差异,可用溶解、过滤的方法除去碳酸钙 |
| D.氯化钠的溶解度随温度的下降而减小,所以可用冷却法从热的含有少量氯化钾的氯化钠浓溶液中得到纯净的氯化钠晶体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】制备氮化镁的装置如图所示。实验时在不锈钢舟内加入镁粉,通氮气15min,升温至1073K,加热半小时,冷却至室温,停止通氮气。下列说法正确的是( )
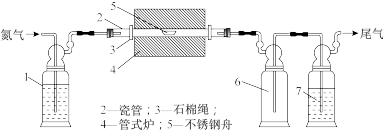

| A.1中的试剂是饱和食盐水,便于观察气泡,调节气流速度 |
| B.6的作用是缓冲加热后未反应的氮气,7的作用是防止空气中的水分进入装置 |
| C.氮化镁是共价化合物,露置于空气中有刺激性气味的气体产生 |
| D.实验中氮气是反应物,仅起到氧化镁粉的作用 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列有关实验的操作、原理和现象,正确的是( )
| A.吸滤操作可加快过滤速度,若吸滤完毕,则应先关闭水龙头,然后拆下连接抽气泵和吸滤液的橡皮管 |
| B.某无色溶液中滴加硝酸银溶液,有白色沉淀生成, 加稀硝酸后沉淀溶解;若另取该溶液加稀硫酸后,微热后有气泡产生;可确定该溶液中一定含NO2- |
| C.在纸层析法分离Fe3+和Cu2+的实验中,层析后,经氨熏,滤纸中无色带出现,一定是误将试样点浸没在展开试中造成的 |
| D.结晶时,若沉淀的结晶颗粒较大,静置后容易沉降到容器底部,此时,进行分离的操作方法是倾析 |
您最近一年使用:0次


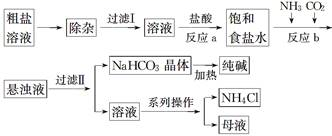
 、
、 的投料比采用1∶2.8(物质的量比)而不是1∶3,是为了提高
的投料比采用1∶2.8(物质的量比)而不是1∶3,是为了提高

