I.化学反应中伴随着能量变化,探究各种能量变化是一永恒的主题。
(1)下列变化属于放热反应的是_______ (填序号)。
a.生石灰溶于水 b.氢氧化钠固体溶于水 c.氢气与氯气化合
d氯化铵固体与氢氧化钡晶体混合搅拌 e.盐酸和镁的反应
(2)下列图像分别表示有关反应的反应过程与能量变化的关系。
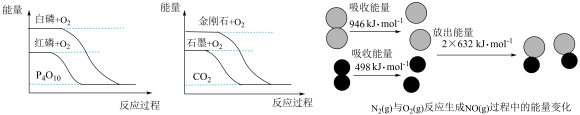
据此判断下列说法中正确的是_______ (填序号)。
a.等质量的石墨和金刚石完全燃烧释放的热量相同
b.白磷和红磷互为同素异形体,相同条件下白磷比红磷稳定
c.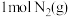 和
和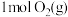 具有的总能量小于
具有的总能量小于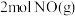 具有的总能量
具有的总能量
Ⅱ.如下图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。
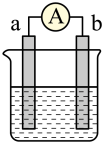
请回答下列问题:
(3)当电极a为 ,电极b为
,电极b为 ,电解质溶液为
,电解质溶液为 溶液时,正极的电极反应式为
溶液时,正极的电极反应式为_______ 。若初始时两电极质量相等,当电路中有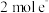 通过时,两极的质量差为
通过时,两极的质量差为_______ g。
(4)当电极a为 ,电极b为
,电极b为 ,电解质溶液为
,电解质溶液为 溶液时,该电池的负极反应式为
溶液时,该电池的负极反应式为_______ 。当反应中收集到标准状况下 气体时,消耗负极的物质的量为
气体时,消耗负极的物质的量为_______  。
。
(1)下列变化属于放热反应的是
a.生石灰溶于水 b.氢氧化钠固体溶于水 c.氢气与氯气化合
d氯化铵固体与氢氧化钡晶体混合搅拌 e.盐酸和镁的反应
(2)下列图像分别表示有关反应的反应过程与能量变化的关系。

据此判断下列说法中正确的是
a.等质量的石墨和金刚石完全燃烧释放的热量相同
b.白磷和红磷互为同素异形体,相同条件下白磷比红磷稳定
c.
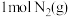 和
和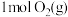 具有的总能量小于
具有的总能量小于 具有的总能量
具有的总能量Ⅱ.如下图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。

请回答下列问题:
(3)当电极a为
 ,电极b为
,电极b为 ,电解质溶液为
,电解质溶液为 溶液时,正极的电极反应式为
溶液时,正极的电极反应式为 通过时,两极的质量差为
通过时,两极的质量差为(4)当电极a为
 ,电极b为
,电极b为 ,电解质溶液为
,电解质溶液为 溶液时,该电池的负极反应式为
溶液时,该电池的负极反应式为 气体时,消耗负极的物质的量为
气体时,消耗负极的物质的量为 。
。
更新时间:2023-04-30 22:00:39
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.完成下列问题
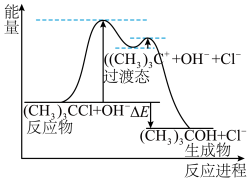
(1)叔丁基氯与碱溶液经两步反应得到叔丁基醇,反应(CH3)3CCl+OH-→(CH3)3COH+Cl-的能量与反应进程如图所示。下列说法正确的是______
(2)下列有关热化学方程式的叙述正确的是_______
(3)已知反应:2NO(g)+2CO(g)=N₂(g)+2CO₂(g),在298K、100kPa的条件下,其中ΔH=-113.0kJ·mol-1,ΔS=-145.3J·mol-1·K-1,该反应___________ (填“能”或“不能”)用于消除汽车尾气中的NO,理由为___________ 。实际上,如果不采取一定措施,汽车尾气并不会自动消除,原因是___________ ;
Ⅱ.CH4和CO2在催化剂作用下可以转化为合成气(主要含H2、CO和少量H2O的混合气体)。
主反应为:I.CH4(g)+CO2(g) 2CO(g)+2H2(g),ΔH1=+247kJ·mol-1
2CO(g)+2H2(g),ΔH1=+247kJ·mol-1
主要副反应有:Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g),ΔH2=+41.2kJ·mol-1
CO(g)+H2O(g),ΔH2=+41.2kJ·mol-1
Ⅲ.CH4(g) C(s)+2H2(g),ΔH3=+74.8kJ·mol-1
C(s)+2H2(g),ΔH3=+74.8kJ·mol-1
Ⅳ.CO(g)+H2(g) C(s)+H2O(g),ΔH4=-131kJ·mol-1
C(s)+H2O(g),ΔH4=-131kJ·mol-1
完成下列填空:
(4)写出CH4和水蒸气反应生成CO和H2的热化学方程式___________ 。
(5)对于反应Ⅰ,有利于提高CH4平衡转化率的措施是___________ 、___________ (任写两条)。
(6)反应Ⅰ温度控制在550~750℃之间,从反应速率角度分析,选择该温度范围的可能原因:___________ 。
(7)某温度下,反应Ⅰ的平衡常数K=0.16,该温度下,测得容器中CH4、CO2、CO和H2的浓度分别为0.5mol/L、0.5mol/L、0.25mol/L、0.25mol/L,此时,反应Ⅰ是否处于平衡状态?若不是,预测反应的方向。___________ 。
(8)CH4和CO2各1mol充入密闭容器中,发生反应I。
①300℃,100kPa,反应达到平衡时CO2体积分数与温度的关系如图中曲线所示。则n(平衡时气体):n(初始气体)=___________ 。
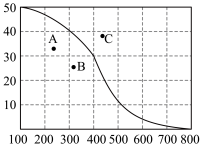
②若A、B、C三点表示不同温度和压强下已达平衡时CO2体积分数___________ 点对应的平衡常数最小,理由是:___________ ;___________ 点对应压强最大,理由是:___________ 。
(1)叔丁基氯与碱溶液经两步反应得到叔丁基醇,反应(CH3)3CCl+OH-→(CH3)3COH+Cl-的能量与反应进程如图所示。下列说法正确的是______

| A.该反应为吸热反应 |
| B.(CH3)3C+比(CH3)3CCl稳定 |
| C.第一步反应一定比第二步反应快 |
| D.增大碱的浓度和升高温度均可加快反应速率 |
(2)下列有关热化学方程式的叙述正确的是_______
A.已知C(石墨,s) C(金刚石,s)ΔH>0,则金刚石比石墨稳定 C(金刚石,s)ΔH>0,则金刚石比石墨稳定 |
| B.含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则该反应的热化学方程式为NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);ΔH=-57.4kJ·mol-1 |
| C.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
D.N2(g)+3H2(g) 2NH3(g);ΔH=-akJ·mol-1,则将14gN2(g)和足量H2置于一密闭容器中,充分反应后放出0.5akJ的热量 2NH3(g);ΔH=-akJ·mol-1,则将14gN2(g)和足量H2置于一密闭容器中,充分反应后放出0.5akJ的热量 |
(3)已知反应:2NO(g)+2CO(g)=N₂(g)+2CO₂(g),在298K、100kPa的条件下,其中ΔH=-113.0kJ·mol-1,ΔS=-145.3J·mol-1·K-1,该反应
Ⅱ.CH4和CO2在催化剂作用下可以转化为合成气(主要含H2、CO和少量H2O的混合气体)。
主反应为:I.CH4(g)+CO2(g)
 2CO(g)+2H2(g),ΔH1=+247kJ·mol-1
2CO(g)+2H2(g),ΔH1=+247kJ·mol-1主要副反应有:Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g),ΔH2=+41.2kJ·mol-1
CO(g)+H2O(g),ΔH2=+41.2kJ·mol-1Ⅲ.CH4(g)
 C(s)+2H2(g),ΔH3=+74.8kJ·mol-1
C(s)+2H2(g),ΔH3=+74.8kJ·mol-1Ⅳ.CO(g)+H2(g)
 C(s)+H2O(g),ΔH4=-131kJ·mol-1
C(s)+H2O(g),ΔH4=-131kJ·mol-1完成下列填空:
(4)写出CH4和水蒸气反应生成CO和H2的热化学方程式
(5)对于反应Ⅰ,有利于提高CH4平衡转化率的措施是
(6)反应Ⅰ温度控制在550~750℃之间,从反应速率角度分析,选择该温度范围的可能原因:
(7)某温度下,反应Ⅰ的平衡常数K=0.16,该温度下,测得容器中CH4、CO2、CO和H2的浓度分别为0.5mol/L、0.5mol/L、0.25mol/L、0.25mol/L,此时,反应Ⅰ是否处于平衡状态?若不是,预测反应的方向。
(8)CH4和CO2各1mol充入密闭容器中,发生反应I。
①300℃,100kPa,反应达到平衡时CO2体积分数与温度的关系如图中曲线所示。则n(平衡时气体):n(初始气体)=

②若A、B、C三点表示不同温度和压强下已达平衡时CO2体积分数
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】异丁烯[CH2=C(CH3)2]是一种重要的化工原料,常用于制备丁基橡胶、甲基丙烯氰等。工业上常利用异丁烷[CH3-CH(CH3)-CH3]为原料制备异丁烯,涉及的主要反应有:
反应I:CH3-CH(CH3)-CH3(g) CH2=C(CH3)2(g)+H2(g) ΔH1=+122kJ·mol-1
CH2=C(CH3)2(g)+H2(g) ΔH1=+122kJ·mol-1
反应II:CH3-CH(CH3)-CH3(g) CH3-CH2-CH2-CH3(g) ΔH2=+9kJ·mol-1
CH3-CH2-CH2-CH3(g) ΔH2=+9kJ·mol-1
请回答下列问题:
(1)已知生成1molH-H键放出能量436kJ,1molC=C键断键生成1molC-C键吸收能量274kJ,则断裂1molC-H键吸收能量为_______ kJ。
(2)异丁烷和正丁烷中稳定性更好的是_______ (填物质名称),反应II的正活化能与逆活化能之差为_______ 。
(3)T℃时,向压强恒定为p0kPa的密闭容器中通入一定量的异丁烷,达到平衡时,测得容器中H2的分压为akPa,正丁烷的分压为bkPa。
①T℃时,反应I的化学平衡常数Kp=_______ kPa(Kp是用气体分压表示的平衡常数)。
②平衡后,若其他条件不变,向容器中再通入少量N2(不参与反应),则异丁烯的平衡产率将_______ (填“增大”“减小”或“不变”),原因为_______ 。
(4)资料表明,在固体杂多酸盐(用S表示)作催化剂时反应I的反应机理如下:
i.CH3-CH(CH3)-CH3(g)+S→CH3-CH(CH3)-CH3…S;
ii.CH3-CH(CH3)-CH3…S+S→CH2=C(CH3)2…S+H2…S;
iii._______。
iv.H2…S→H2(g)+S。
表征CH3-CH(CH3)-CH3(g)在固体催化剂表面吸附过程的是_______ (填反应序号),反应iii的化学方程式为_______ 。
反应I:CH3-CH(CH3)-CH3(g)
 CH2=C(CH3)2(g)+H2(g) ΔH1=+122kJ·mol-1
CH2=C(CH3)2(g)+H2(g) ΔH1=+122kJ·mol-1反应II:CH3-CH(CH3)-CH3(g)
 CH3-CH2-CH2-CH3(g) ΔH2=+9kJ·mol-1
CH3-CH2-CH2-CH3(g) ΔH2=+9kJ·mol-1请回答下列问题:
(1)已知生成1molH-H键放出能量436kJ,1molC=C键断键生成1molC-C键吸收能量274kJ,则断裂1molC-H键吸收能量为
(2)异丁烷和正丁烷中稳定性更好的是
(3)T℃时,向压强恒定为p0kPa的密闭容器中通入一定量的异丁烷,达到平衡时,测得容器中H2的分压为akPa,正丁烷的分压为bkPa。
①T℃时,反应I的化学平衡常数Kp=
②平衡后,若其他条件不变,向容器中再通入少量N2(不参与反应),则异丁烯的平衡产率将
(4)资料表明,在固体杂多酸盐(用S表示)作催化剂时反应I的反应机理如下:
i.CH3-CH(CH3)-CH3(g)+S→CH3-CH(CH3)-CH3…S;
ii.CH3-CH(CH3)-CH3…S+S→CH2=C(CH3)2…S+H2…S;
iii._______。
iv.H2…S→H2(g)+S。
表征CH3-CH(CH3)-CH3(g)在固体催化剂表面吸附过程的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】回答或解释下列问题:
(1)已知:P4(白磷,s) =4P(红磷,s) ΔH=-a kJ·mol-1(a>0),则稳定性:白磷_______ 红磷(填“大于”或“小于”)。
(2)在常温常压下,1 g 氢气在足量氯气中完全燃烧生成氯化氢气体,放出91.5 kJ 的热量。写出相应的热化学方程式为____________ ;
(3)将浓氨水滴入到固体氢氧化钠中,可以快速制备氨气,用平衡移动原理解释原因:____________ ;
(4)常温下,用0.1mol·L-1 NaOH溶液分别滴定20.00 mL 0.1mol/L HCl溶液和20.00 mL0.1 mol/L CH3COOH溶液,得到2条滴定曲线如图所示:
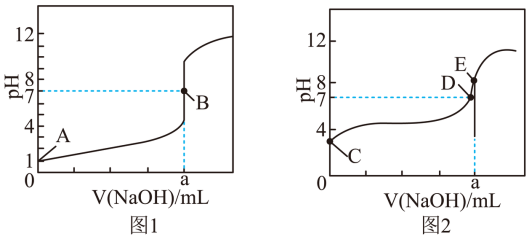
①由A、C点判断,滴定HCl溶液的曲线是__________ (填“图1”或“图2”)。
②a=________ mL。
③D点对应离子浓度由大到小的顺序为____________ 。
(1)已知:P4(白磷,s) =4P(红磷,s) ΔH=-a kJ·mol-1(a>0),则稳定性:白磷
(2)在常温常压下,1 g 氢气在足量氯气中完全燃烧生成氯化氢气体,放出91.5 kJ 的热量。写出相应的热化学方程式为
(3)将浓氨水滴入到固体氢氧化钠中,可以快速制备氨气,用平衡移动原理解释原因:
(4)常温下,用0.1mol·L-1 NaOH溶液分别滴定20.00 mL 0.1mol/L HCl溶液和20.00 mL0.1 mol/L CH3COOH溶液,得到2条滴定曲线如图所示:

①由A、C点判断,滴定HCl溶液的曲线是
②a=
③D点对应离子浓度由大到小的顺序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g) CH3OH(g)。图1表示反应进行过程中能量的变化;图2表示一定温度下,在体积为2 L的密闭容器中加入4molH2(g)和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化情况。
CH3OH(g)。图1表示反应进行过程中能量的变化;图2表示一定温度下,在体积为2 L的密闭容器中加入4molH2(g)和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化情况。
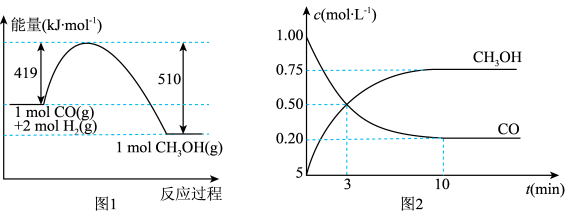
(1)由图1可知,该反应是____ (填“吸热”或“放热”)反应。
(2)当反应生成1 mol CH3OH(g)时,能量变化值是____ kJ。若要加快反应速率,可采取的措施有____ (写一条)。
(3)根据图2判断,下列说法错误的是____ (填字母)。
A.反应进行到3 min时达到化学平衡状态
B.若反应生成液态甲醇,能量变化值会更大
C.平衡时氢气的浓度为1 mol/L
(4)推测反应CH3OH(g) CO(g)+2H2(g)是
CO(g)+2H2(g)是____ (填“吸热”或“放热”)反应。
(5)若断开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要吸收能量为436 kJ、391 kJ、946 kJ,则3 mol H2(g)与足量N2(g)反应生成NH3(g)需放出能量____ kJ。事实上,反应的热量总小于理论值,理由是____ 。
 CH3OH(g)。图1表示反应进行过程中能量的变化;图2表示一定温度下,在体积为2 L的密闭容器中加入4molH2(g)和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化情况。
CH3OH(g)。图1表示反应进行过程中能量的变化;图2表示一定温度下,在体积为2 L的密闭容器中加入4molH2(g)和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化情况。
(1)由图1可知,该反应是
(2)当反应生成1 mol CH3OH(g)时,能量变化值是
(3)根据图2判断,下列说法错误的是
A.反应进行到3 min时达到化学平衡状态
B.若反应生成液态甲醇,能量变化值会更大
C.平衡时氢气的浓度为1 mol/L
(4)推测反应CH3OH(g)
 CO(g)+2H2(g)是
CO(g)+2H2(g)是(5)若断开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要吸收能量为436 kJ、391 kJ、946 kJ,则3 mol H2(g)与足量N2(g)反应生成NH3(g)需放出能量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)中和热测定的实验中,用到的玻璃仪器有烧杯、量筒、温度计、_______ 。
(2)向 的NaOH溶液中分别加入稀醋酸、浓硫酸、稀盐酸,则恰好完全反应时的热效应
的NaOH溶液中分别加入稀醋酸、浓硫酸、稀盐酸,则恰好完全反应时的热效应 、
、 、
、 从大到小的排序是
从大到小的排序是_______ 。
(3)为了研究化学反应 的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到现象为
的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到现象为_______ ,则说明该反应是放热反应。

(1)中和热测定的实验中,用到的玻璃仪器有烧杯、量筒、温度计、
(2)向
 的NaOH溶液中分别加入稀醋酸、浓硫酸、稀盐酸,则恰好完全反应时的热效应
的NaOH溶液中分别加入稀醋酸、浓硫酸、稀盐酸,则恰好完全反应时的热效应 、
、 、
、 从大到小的排序是
从大到小的排序是(3)为了研究化学反应
 的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到现象为
的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到现象为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于放热反应的是_____(填字母)。
(2)获取能量变化的途径
①已知:
则:SiCl4(g)+2H2(g)= Si(s)+4HCl(g)的反应热
_____  (已知1molSi中含有2molSi-Si)
(已知1molSi中含有2molSi-Si)
②已知在常温常压下:
i、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)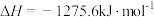
ii、H2O(l)=H2O(g)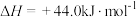
写出表示甲醇燃烧热的热化学方程式_____ 。
③利用实验装置测量利用下图图装置测定中和热的实验步骤如下:
回答下列问题:
I.仪器a的名称为_____
Ⅱ.做了四次实验,并将实验数据记录如下:
近似认为0.55mol/LNaOH溶液和0.25mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g·℃),通过以上数据计算中和热ΔH=_____ (结果保留小数点后一位)。上述结果与-57.3kJ/mol有偏差的原因可能是_____ 。
A.量取硫酸溶液的体积时仰视读数
B.量取NaOH溶液的体积时仰视读数
C.温度计测出NaOH溶液起始温度后直接测定硫酸的温度
D.搅拌不充分
(1)下列反应中,属于放热反应的是_____(填字母)。
| A.碳与水蒸气反应 |
| B.铝和氧化铁反应 |
| C.CaCO3受热分解 |
| D.氢气还原三氧化钨制取钨E.锌与盐酸反应 |
①已知:
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能(kJ·mol-1) | a | b | c | d | e | f |

 (已知1molSi中含有2molSi-Si)
(已知1molSi中含有2molSi-Si)②已知在常温常压下:
i、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)
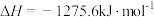
ii、H2O(l)=H2O(g)
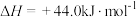
写出表示甲醇燃烧热的热化学方程式
③利用实验装置测量利用下图图装置测定中和热的实验步骤如下:
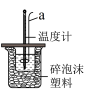 | ①用量筒量取0.25mol/L的硫酸50mL倒入小烧杯中,测出硫酸溶液温度; ②用另一量筒量取50mL0.55mol/LNaOH溶液,并用同一温度计测出其温度; ③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液的最高温度。 |
I.仪器a的名称为
Ⅱ.做了四次实验,并将实验数据记录如下:
温度实验次数 | 起始温度t1℃ | 终止温度t2/℃ | ||
| H2SO4 | NaOH | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 |
A.量取硫酸溶液的体积时仰视读数
B.量取NaOH溶液的体积时仰视读数
C.温度计测出NaOH溶液起始温度后直接测定硫酸的温度
D.搅拌不充分
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】将CO2应用于生产清洁燃料甲醇,既能缓解温室效应的影响,又能为能源的制备开辟新的渠道,其合成反应为CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。回答下列问题:
(1)利用二氧化碳制得的甲醇还可以制取甲胺,其反应原理为CH3OH(g)+NH3(g)⇌CH3NH2(g)+H2O(g) ∆H,已知该反应中相关化学键的键能数据如下:
则该反应的∆H=_______ kJ•mol-1。
(2)汽油燃油车上安装三元催化转化器,可有效降低汽车尾气污染。已知:
①CO(g)+NO2(g)⇌CO2(g)+NO(g) ∆H1=-226kJ•rnol-1
②N2(g)+2O2(g)⇌2NO2(g) ∆H2=+68kJ•mol-1
③N2(g)+O2(g)⇌2NO(g) ∆H3=+183kJ•mol-1
则:CO和NO两种尾气在催化剂作用下生成N2的热化学方程式是_______ 。
(3)CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:
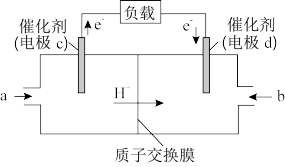
电池总反应为2CH3OH+3O2=2CO2+4H2O。则d电极是_______ (填“正极”或“负极”),c电极的电极反应式为______ 。若线路中转移2mol电子,则上述CH3OH燃料电池消耗的O2在标准状况下的体积为_____ L。
(1)利用二氧化碳制得的甲醇还可以制取甲胺,其反应原理为CH3OH(g)+NH3(g)⇌CH3NH2(g)+H2O(g) ∆H,已知该反应中相关化学键的键能数据如下:
| 共价键 | C-O | H-O | N-H | C-N |
| 键能/kJ•mol-1 | 351 | 463 | 393 | 293 |
则该反应的∆H=
(2)汽油燃油车上安装三元催化转化器,可有效降低汽车尾气污染。已知:
①CO(g)+NO2(g)⇌CO2(g)+NO(g) ∆H1=-226kJ•rnol-1
②N2(g)+2O2(g)⇌2NO2(g) ∆H2=+68kJ•mol-1
③N2(g)+O2(g)⇌2NO(g) ∆H3=+183kJ•mol-1
则:CO和NO两种尾气在催化剂作用下生成N2的热化学方程式是
(3)CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:

电池总反应为2CH3OH+3O2=2CO2+4H2O。则d电极是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】利用化学反应将储存在物质内部的化学能转化为电能,科学家设计出了原电池,从而为人类生产、生活提供能量。
(1)甲同学认为,所有的氧化还原反应都可以设计成原电池,你是否同意?________ (填“是”或“否”)。
(2)乙同学依据氧化还原反应:2Ag++Cu===Cu2++2Ag设计的原电池如图所示:
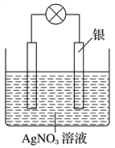
①负极材料是_______ ,发生的电极反应为____________________________ ;
②外电路中的电子是从________ 电极流向________ 电极。(写出电极材料的名称)
③当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4 g,则该原电池反应共转移的电子数目是________ 。
Ⅱ.水是生命之源,也是化学反应中的主角。请回答下列问题:
(1)已知:2 mol H2完全燃烧生成液态水时放出572 kJ的热量。
①生成物的能量总和________ (填“>”“<”或“=”)反应物的能量总和。
②若2 mol氢气完全燃烧生成水蒸气,则放出的热量________ (填“>”“<”或“=”)572 kJ。
③每克氢气燃烧生成液态水时放出的热量为________ 。
(2)天然气(主要成分CH4)和氧气反应生成二氧化碳和水,该反应为放热的氧化还原反应,可将其设计成燃料电池,构造如图所示,a、b两个电极均由多孔的碳块组成。
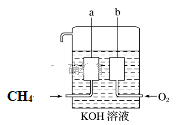
a电极的电极反应式是_______________________________________________ 。
(1)甲同学认为,所有的氧化还原反应都可以设计成原电池,你是否同意?
(2)乙同学依据氧化还原反应:2Ag++Cu===Cu2++2Ag设计的原电池如图所示:

①负极材料是
②外电路中的电子是从
③当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4 g,则该原电池反应共转移的电子数目是
Ⅱ.水是生命之源,也是化学反应中的主角。请回答下列问题:
(1)已知:2 mol H2完全燃烧生成液态水时放出572 kJ的热量。
①生成物的能量总和
②若2 mol氢气完全燃烧生成水蒸气,则放出的热量
③每克氢气燃烧生成液态水时放出的热量为
(2)天然气(主要成分CH4)和氧气反应生成二氧化碳和水,该反应为放热的氧化还原反应,可将其设计成燃料电池,构造如图所示,a、b两个电极均由多孔的碳块组成。

a电极的电极反应式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】I.利用化学反应将储存在物质内部的化学能转化为电能,科学家设计出了原电池,从而为人类生产、生活提供能量。
(1)甲同学认为,所有的氧化还原反应都可以设计成原电池,你是否同意?____ (填“是”或“否”)。
(2)乙同学依据氧化还原反应:2Ag++Cu=Cu2++2Ag设计的原电池如图所示:
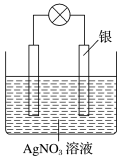
①负极材料是_______ ,发生的电极反应为____________________________ 。
②当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4 g,则该原电池反应共转移的电子数目是________ 。
II.水是生命之源,也是化学反应中的主角。请回答下列问题:
(1)已知:2 mol H2完全燃烧生成液态水时放出572 kJ的热量。
①若2 mol氢气完全燃烧生成水蒸气,则放出的热量________ (填“>”“<”或“=”)572 kJ。
②每克氢气燃烧生成液态水时放出的热量为________ 。
(2)天然气(主要成分CH4)和氧气反应生成二氧化碳和水,该反应为放热的氧化还原反应,可将其设计成燃料电池,构造如图所示,a、b两个电极均由多孔的碳块组成。a电极的电极反应式是____________________________ 。当a极转移0.3mol电子时,b极消耗标准状况下O2的体积为_________________ mL。b极附近pH____ (填“增大”、“减小”或“不变”)。

(1)甲同学认为,所有的氧化还原反应都可以设计成原电池,你是否同意?
(2)乙同学依据氧化还原反应:2Ag++Cu=Cu2++2Ag设计的原电池如图所示:

①负极材料是
②当反应进行到一段时间后取出电极材料,测得某一电极增重了5.4 g,则该原电池反应共转移的电子数目是
II.水是生命之源,也是化学反应中的主角。请回答下列问题:
(1)已知:2 mol H2完全燃烧生成液态水时放出572 kJ的热量。
①若2 mol氢气完全燃烧生成水蒸气,则放出的热量
②每克氢气燃烧生成液态水时放出的热量为
(2)天然气(主要成分CH4)和氧气反应生成二氧化碳和水,该反应为放热的氧化还原反应,可将其设计成燃料电池,构造如图所示,a、b两个电极均由多孔的碳块组成。a电极的电极反应式是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】电池在我们的生活中有着重要的应用,请回答下列问题:
(1)为了验证与 和
和 的氧化性强弱,下列装置能达到实验目的的是
的氧化性强弱,下列装置能达到实验目的的是____________________ (填序号),写出正极的电极反应式___________________ 。若构建原电池时两个电极的质量相等,当导线中通过 电子时,两个电极的质量差为
电子时,两个电极的质量差为____________________ 。

(2)将 设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
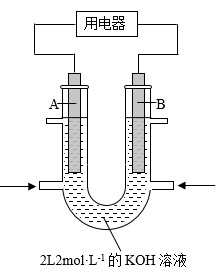
实验测得电池工作时 向B电极定向移动,则
向B电极定向移动,则____________________ (填“A”或“B”)处电极入口通甲烷,其电极反应式为_____________ 。
(3)以氨作为燃料的燃料电池,具有能量效率高的特点,另外氨气含氢量高,易液化,方便运输和贮存,是很好的氢源载体。燃料电池的结构如图所示:

①a极是电池的____________________ (填“正”或“负”)极,电极反应式为_______________________ 。
②当生成 时,电路中通过的电子的物质的量为
时,电路中通过的电子的物质的量为____________________ 。
(1)为了验证与
 和
和 的氧化性强弱,下列装置能达到实验目的的是
的氧化性强弱,下列装置能达到实验目的的是 电子时,两个电极的质量差为
电子时,两个电极的质量差为
(2)将
 设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
实验测得电池工作时
 向B电极定向移动,则
向B电极定向移动,则(3)以氨作为燃料的燃料电池,具有能量效率高的特点,另外氨气含氢量高,易液化,方便运输和贮存,是很好的氢源载体。燃料电池的结构如图所示:

①a极是电池的
②当生成
 时,电路中通过的电子的物质的量为
时,电路中通过的电子的物质的量为
您最近一年使用:0次
【推荐2】(1)习近平总书记提出“绿水青山就是金山银山”,因此研究NOx、SO2等大气污染物的妥善处理具有重要意义。SO2的排放主要来自煤的燃烧,工业上常用氨水作为吸收液吸收工业废气中的SO2。
已知吸收过程中相关反应的热化学方程式如下:
①
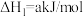 ;
;
②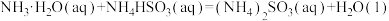
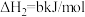 ;
;
③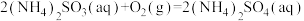
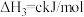 ;
;
则反应 的
的
_______ kJ/mol。
(2)甲醇在工业上利用水煤气合成,反应为
 。在一定条件下,将2molCO和4molH2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,反应达到平衡时CH3OH的体积分数φ(CH3OH)变化趋势如图1所示。
。在一定条件下,将2molCO和4molH2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,反应达到平衡时CH3OH的体积分数φ(CH3OH)变化趋势如图1所示。

①M点CO的转化率为_______ 。
②X轴上a点的数值比b点_______ (填“大”或“小”)。某同学认为上图中Y轴表示温度,你认为他判断的理由是_______ 。
(3)已知CO2催化加氢合成乙醇的反应原理为
 。m代表起始时的投料比,即
。m代表起始时的投料比,即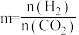 。m=3时,该反应达到平衡状态后
。m=3时,该反应达到平衡状态后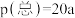 MPa,恒压条件下各物质的物质的量分数与温度的关系如图2所示。
MPa,恒压条件下各物质的物质的量分数与温度的关系如图2所示。 温度时,反应达到平衡时的Kp=
温度时,反应达到平衡时的Kp=_______ 。(保留两位有效数字)

(4)科学家利用图3所示装置可以将CO2转化为气体燃料CO(电解质溶液为稀硫酸),该装置工作时,导线中通过2mol电子后,假定体积不变,M极电解质溶液的pH____ (填“增大”“减小”或“不变”),M、N两极电解质溶液变化的质量差|Δ(M)|-|Δ(N)|=___ g。
已知吸收过程中相关反应的热化学方程式如下:
①

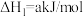 ;
;②
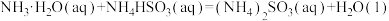
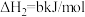 ;
;③
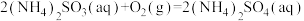
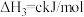 ;
;则反应
 的
的
(2)甲醇在工业上利用水煤气合成,反应为

 。在一定条件下,将2molCO和4molH2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,反应达到平衡时CH3OH的体积分数φ(CH3OH)变化趋势如图1所示。
。在一定条件下,将2molCO和4molH2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,反应达到平衡时CH3OH的体积分数φ(CH3OH)变化趋势如图1所示。
①M点CO的转化率为
②X轴上a点的数值比b点
(3)已知CO2催化加氢合成乙醇的反应原理为

 。m代表起始时的投料比,即
。m代表起始时的投料比,即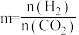 。m=3时,该反应达到平衡状态后
。m=3时,该反应达到平衡状态后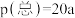 MPa,恒压条件下各物质的物质的量分数与温度的关系如图2所示。
MPa,恒压条件下各物质的物质的量分数与温度的关系如图2所示。 温度时,反应达到平衡时的Kp=
温度时,反应达到平衡时的Kp=
(4)科学家利用图3所示装置可以将CO2转化为气体燃料CO(电解质溶液为稀硫酸),该装置工作时,导线中通过2mol电子后,假定体积不变,M极电解质溶液的pH
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氢气是非常重要的化学能源,利用氢气可以实现化学能向热能、电能的直接转化。
(1)已知断开 、
、 、
、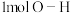 需要的能量依次是
需要的能量依次是 、
、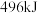 、.
、. .,则
.,则 是
是___________ (填“吸热”或“放热”)反应,能正确表示反应 中能量变化的是图
中能量变化的是图___________ (填“甲”或“乙”)。 和
和 组合形成的质子交换膜燃料电池的结构如下图:
组合形成的质子交换膜燃料电池的结构如下图:___________ (填“正极”或“负极”),电极c的电极反应式为___________ 。
②若电路中转移 电子,则该燃料电池理论上消耗的
电子,则该燃料电池理论上消耗的 在标况下的体积为
在标况下的体积为___________ L。
(3)将纯锌片和纯铜片按图中方式插入100mL浓度为2mol/L的稀硫酸中一段时间,回答下列问题:___________ 。
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
②当图中构成原电池的电路中转移0.1mol的电子时,负极的质量___________ (填“增加”或“减少”)___________ g。
③请写出图中构成原电池的负极电极反应式:___________ 。
(1)已知断开
 、
、 、
、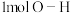 需要的能量依次是
需要的能量依次是 、
、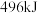 、.
、. .,则
.,则 是
是 中能量变化的是图
中能量变化的是图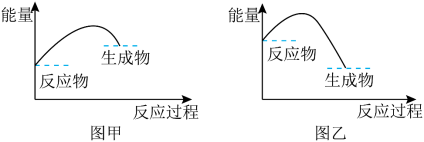
 和
和 组合形成的质子交换膜燃料电池的结构如下图:
组合形成的质子交换膜燃料电池的结构如下图: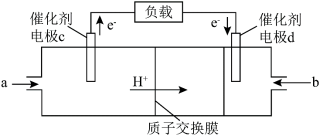
②若电路中转移
 电子,则该燃料电池理论上消耗的
电子,则该燃料电池理论上消耗的 在标况下的体积为
在标况下的体积为(3)将纯锌片和纯铜片按图中方式插入100mL浓度为2mol/L的稀硫酸中一段时间,回答下列问题:

A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
②当图中构成原电池的电路中转移0.1mol的电子时,负极的质量
③请写出图中构成原电池的负极电极反应式:
您最近一年使用:0次



