Ⅰ.完成下列问题
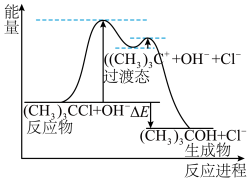
(1)叔丁基氯与碱溶液经两步反应得到叔丁基醇,反应(CH3)3CCl+OH-→(CH3)3COH+Cl-的能量与反应进程如图所示。下列说法正确的是______
(2)下列有关热化学方程式的叙述正确的是_______
(3)已知反应:2NO(g)+2CO(g)=N₂(g)+2CO₂(g),在298K、100kPa的条件下,其中ΔH=-113.0kJ·mol-1,ΔS=-145.3J·mol-1·K-1,该反应___________ (填“能”或“不能”)用于消除汽车尾气中的NO,理由为___________ 。实际上,如果不采取一定措施,汽车尾气并不会自动消除,原因是___________ ;
Ⅱ.CH4和CO2在催化剂作用下可以转化为合成气(主要含H2、CO和少量H2O的混合气体)。
主反应为:I.CH4(g)+CO2(g) 2CO(g)+2H2(g),ΔH1=+247kJ·mol-1
2CO(g)+2H2(g),ΔH1=+247kJ·mol-1
主要副反应有:Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g),ΔH2=+41.2kJ·mol-1
CO(g)+H2O(g),ΔH2=+41.2kJ·mol-1
Ⅲ.CH4(g) C(s)+2H2(g),ΔH3=+74.8kJ·mol-1
C(s)+2H2(g),ΔH3=+74.8kJ·mol-1
Ⅳ.CO(g)+H2(g) C(s)+H2O(g),ΔH4=-131kJ·mol-1
C(s)+H2O(g),ΔH4=-131kJ·mol-1
完成下列填空:
(4)写出CH4和水蒸气反应生成CO和H2的热化学方程式___________ 。
(5)对于反应Ⅰ,有利于提高CH4平衡转化率的措施是___________ 、___________ (任写两条)。
(6)反应Ⅰ温度控制在550~750℃之间,从反应速率角度分析,选择该温度范围的可能原因:___________ 。
(7)某温度下,反应Ⅰ的平衡常数K=0.16,该温度下,测得容器中CH4、CO2、CO和H2的浓度分别为0.5mol/L、0.5mol/L、0.25mol/L、0.25mol/L,此时,反应Ⅰ是否处于平衡状态?若不是,预测反应的方向。___________ 。
(8)CH4和CO2各1mol充入密闭容器中,发生反应I。
①300℃,100kPa,反应达到平衡时CO2体积分数与温度的关系如图中曲线所示。则n(平衡时气体):n(初始气体)=___________ 。
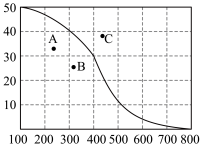
②若A、B、C三点表示不同温度和压强下已达平衡时CO2体积分数___________ 点对应的平衡常数最小,理由是:___________ ;___________ 点对应压强最大,理由是:___________ 。
(1)叔丁基氯与碱溶液经两步反应得到叔丁基醇,反应(CH3)3CCl+OH-→(CH3)3COH+Cl-的能量与反应进程如图所示。下列说法正确的是______

| A.该反应为吸热反应 |
| B.(CH3)3C+比(CH3)3CCl稳定 |
| C.第一步反应一定比第二步反应快 |
| D.增大碱的浓度和升高温度均可加快反应速率 |
(2)下列有关热化学方程式的叙述正确的是_______
A.已知C(石墨,s) C(金刚石,s)ΔH>0,则金刚石比石墨稳定 C(金刚石,s)ΔH>0,则金刚石比石墨稳定 |
| B.含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则该反应的热化学方程式为NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);ΔH=-57.4kJ·mol-1 |
| C.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
D.N2(g)+3H2(g) 2NH3(g);ΔH=-akJ·mol-1,则将14gN2(g)和足量H2置于一密闭容器中,充分反应后放出0.5akJ的热量 2NH3(g);ΔH=-akJ·mol-1,则将14gN2(g)和足量H2置于一密闭容器中,充分反应后放出0.5akJ的热量 |
(3)已知反应:2NO(g)+2CO(g)=N₂(g)+2CO₂(g),在298K、100kPa的条件下,其中ΔH=-113.0kJ·mol-1,ΔS=-145.3J·mol-1·K-1,该反应
Ⅱ.CH4和CO2在催化剂作用下可以转化为合成气(主要含H2、CO和少量H2O的混合气体)。
主反应为:I.CH4(g)+CO2(g)
 2CO(g)+2H2(g),ΔH1=+247kJ·mol-1
2CO(g)+2H2(g),ΔH1=+247kJ·mol-1主要副反应有:Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g),ΔH2=+41.2kJ·mol-1
CO(g)+H2O(g),ΔH2=+41.2kJ·mol-1Ⅲ.CH4(g)
 C(s)+2H2(g),ΔH3=+74.8kJ·mol-1
C(s)+2H2(g),ΔH3=+74.8kJ·mol-1Ⅳ.CO(g)+H2(g)
 C(s)+H2O(g),ΔH4=-131kJ·mol-1
C(s)+H2O(g),ΔH4=-131kJ·mol-1完成下列填空:
(4)写出CH4和水蒸气反应生成CO和H2的热化学方程式
(5)对于反应Ⅰ,有利于提高CH4平衡转化率的措施是
(6)反应Ⅰ温度控制在550~750℃之间,从反应速率角度分析,选择该温度范围的可能原因:
(7)某温度下,反应Ⅰ的平衡常数K=0.16,该温度下,测得容器中CH4、CO2、CO和H2的浓度分别为0.5mol/L、0.5mol/L、0.25mol/L、0.25mol/L,此时,反应Ⅰ是否处于平衡状态?若不是,预测反应的方向。
(8)CH4和CO2各1mol充入密闭容器中,发生反应I。
①300℃,100kPa,反应达到平衡时CO2体积分数与温度的关系如图中曲线所示。则n(平衡时气体):n(初始气体)=

②若A、B、C三点表示不同温度和压强下已达平衡时CO2体积分数
更新时间:2024-02-16 21:33:04
|
相似题推荐
【推荐1】卤素的单质和化合物在生产和生活中应用广泛。
(1)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。
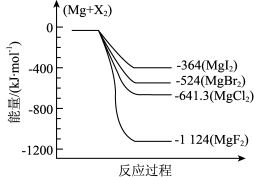
①图中四种MgX2的热稳定由小到大的顺序是:_______ 。
②MgBr2(s)+Cl2(g) MgCl2(s)+Br2(g) △H=
MgCl2(s)+Br2(g) △H=_______ kJ∙mol-1。
某温度下,在密闭恒容容器中放入一定量MgBr2(s)和Cl2(g)进行该反应,一定时间后不能说明该反应已经达到平衡的是_______ 。(选填序号)。
A.容器内的压强不再改变 B.混合气体的密度不再改变
C.混合气体的颜色不再改变 D.混合气体的平均相对分子质量不再改变
E.容器内的固体的质量不再改变
③工业上用金属Mg与I2反应制取MgI2时,常加入少量水,水的作用是_______ 。
④AgBr常用作感光剂和镇静剂,工业制得的AgBr固体常含有AgCl固体。现有含AgCl质量分数为14.35%的AgBr固体100.00g,可用饱和KBr溶液一次性浸泡,恰好溶解除去AgCl固体,需要5.015 mol∙L-1的饱和KBr溶液的体积至少为_______ mL。(保留4位有效数字)(已知常温下Ksp(ABr)=5.418×10-13,Ksp(AgCl)=1.806×10-10)
(2)将一定量的PCl5(g)在T℃、Po压强下发生反应:PCl5(g) PCl3(g)+Cl2(g),测得平衡时PCl5的分解率为a,求该温度下此反应的平衡常数Kp=
PCl3(g)+Cl2(g),测得平衡时PCl5的分解率为a,求该温度下此反应的平衡常数Kp=_______ 。(用含a的式子表示。其中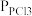 、
、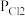 、
、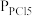 为各组分的平衡分压,如
为各组分的平衡分压,如 ,p为平衡总压,
,p为平衡总压, 为平衡系统中PCl5的物质的量分数)
为平衡系统中PCl5的物质的量分数)
(3)向11mL0.40mol∙L-1H2O2溶液中加入适量FeCl3溶液,16分钟时测得生成O2的体积(已折算为标准状况)为44.8mL。资料显示,反应分两步进行:①2Fe3++H2O2=2Fe2++O2↑+2H+,②2Fe2++H2O2+2H+=2Fe3++2H2O。反应过程中能量变化如图1所示,在图2中画出在0~16分钟内产生O2的物质的量随时间的变化示意图_______ 。

(1)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。

①图中四种MgX2的热稳定由小到大的顺序是:
②MgBr2(s)+Cl2(g)
 MgCl2(s)+Br2(g) △H=
MgCl2(s)+Br2(g) △H=某温度下,在密闭恒容容器中放入一定量MgBr2(s)和Cl2(g)进行该反应,一定时间后不能说明该反应已经达到平衡的是
A.容器内的压强不再改变 B.混合气体的密度不再改变
C.混合气体的颜色不再改变 D.混合气体的平均相对分子质量不再改变
E.容器内的固体的质量不再改变
③工业上用金属Mg与I2反应制取MgI2时,常加入少量水,水的作用是
④AgBr常用作感光剂和镇静剂,工业制得的AgBr固体常含有AgCl固体。现有含AgCl质量分数为14.35%的AgBr固体100.00g,可用饱和KBr溶液一次性浸泡,恰好溶解除去AgCl固体,需要5.015 mol∙L-1的饱和KBr溶液的体积至少为
(2)将一定量的PCl5(g)在T℃、Po压强下发生反应:PCl5(g)
 PCl3(g)+Cl2(g),测得平衡时PCl5的分解率为a,求该温度下此反应的平衡常数Kp=
PCl3(g)+Cl2(g),测得平衡时PCl5的分解率为a,求该温度下此反应的平衡常数Kp=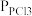 、
、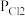 、
、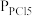 为各组分的平衡分压,如
为各组分的平衡分压,如 ,p为平衡总压,
,p为平衡总压, 为平衡系统中PCl5的物质的量分数)
为平衡系统中PCl5的物质的量分数)(3)向11mL0.40mol∙L-1H2O2溶液中加入适量FeCl3溶液,16分钟时测得生成O2的体积(已折算为标准状况)为44.8mL。资料显示,反应分两步进行:①2Fe3++H2O2=2Fe2++O2↑+2H+,②2Fe2++H2O2+2H+=2Fe3++2H2O。反应过程中能量变化如图1所示,在图2中画出在0~16分钟内产生O2的物质的量随时间的变化示意图

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】化学反应与能量变化是化学研究的重要问题,根据相关材料分析回答:
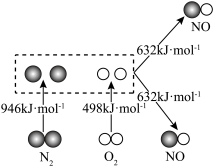
(1)汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气,其中生成NO的能量变化如图所示,则图中三种分子最稳定的是_________ 。
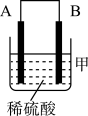
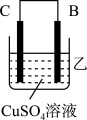
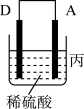
(3)把A、B、C、D四种金属按表中装置进行实验。
根据表中信息判断四种金属活动性由大到小的顺序是_______ ;写出装置乙中正极的电极反应式:_______ 。
(4)一种熔融碳酸盐燃料电池原理示意如图所示。电池工作时,外电路上电流的方向应从电极___________ (填A或B)流向用电器。内电路中, 向电极
向电极___________ (填A或B)移动,电极A上CO参与的电极反应为___________ 。
(1)汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气,其中生成NO的能量变化如图所示,则图中三种分子最稳定的是
| A.CH4+2O2=CO2+2H2O | B.Fe+CuSO4=FeSO4+Cu |
| C.2NaOH+H2SO4=Na2SO4+2H2O | D.Pb+PbO2+2H2SO4=2PbSO4+2H2O |
| 装置 |
|
|
|
| 电子从A到B | C电极的质量增加 | 二价金属D不断溶解 |
(4)一种熔融碳酸盐燃料电池原理示意如图所示。电池工作时,外电路上电流的方向应从电极
 向电极
向电极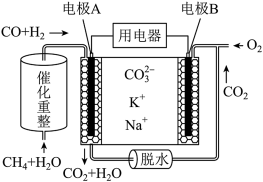
您最近一年使用:0次
【推荐3】回答下列问题:
(1)已知两种同素异形体A、B的燃烧热的热化学方程式为:
A(s)+O2(g) =CO2(g) △H= - 393.51 kJ/mol
B(s)+O2(g)=CO2(g) △H= - 395.41 kJ/mol
则两种同素异形体中较稳定的是(填"A"或"B")___________________ 。
(2)工业上用H2和Cl2反应制HCl,各键能数据为:H – H:436 kJ/mol;Cl-Cl:243 kJ/mol;H-Cl:431 kJ/mol,该反应的热化学方程式是_____________________ 。
(3)合成气(CO和H2为主的混合气体)不但是重要的燃料也是重要的化工原料,制备合成气的方法有多种,已知l gCH4气体与O2气体反应生成CO气体和H2气体放2.25 kJ热量。
①写出相应热化学方程式______________ 。
②用甲烷制备合成气还可以发生反应:CH4(g)+H2O(g)=CO(g)+3H2(g);△H2= +216kJ/mol。现有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。若x=0.2时,反应①放出的能量为____ kJ;若x=____ 时, 反应①与②放出(或吸收)的总能量为0。
(4)一定温度下,将3 mol A气体和l mol B气体通入一容积固定为2 L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g), 反应1 min时测得剩余1.8 mol A,C的浓度为0.4 mol/L,则1 min内,B的平均反应速率为
xC(g), 反应1 min时测得剩余1.8 mol A,C的浓度为0.4 mol/L,则1 min内,B的平均反应速率为_________ ; x为___________ 。可以作为达到平衡状态的标志是______________ 。
A.单位时间内生成n mol B的同时生成3n molA
B.混合气体的压强不变
C.混合气体的颜色不再改变(C为有色气体)
D.混合气体的密度不变
(1)已知两种同素异形体A、B的燃烧热的热化学方程式为:
A(s)+O2(g) =CO2(g) △H= - 393.51 kJ/mol
B(s)+O2(g)=CO2(g) △H= - 395.41 kJ/mol
则两种同素异形体中较稳定的是(填"A"或"B")
(2)工业上用H2和Cl2反应制HCl,各键能数据为:H – H:436 kJ/mol;Cl-Cl:243 kJ/mol;H-Cl:431 kJ/mol,该反应的热化学方程式是
(3)合成气(CO和H2为主的混合气体)不但是重要的燃料也是重要的化工原料,制备合成气的方法有多种,已知l gCH4气体与O2气体反应生成CO气体和H2气体放2.25 kJ热量。
①写出相应热化学方程式
②用甲烷制备合成气还可以发生反应:CH4(g)+H2O(g)=CO(g)+3H2(g);△H2= +216kJ/mol。现有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。若x=0.2时,反应①放出的能量为
(4)一定温度下,将3 mol A气体和l mol B气体通入一容积固定为2 L的密闭容器中,发生如下反应:3A(g)+B(g)
 xC(g), 反应1 min时测得剩余1.8 mol A,C的浓度为0.4 mol/L,则1 min内,B的平均反应速率为
xC(g), 反应1 min时测得剩余1.8 mol A,C的浓度为0.4 mol/L,则1 min内,B的平均反应速率为A.单位时间内生成n mol B的同时生成3n molA
B.混合气体的压强不变
C.混合气体的颜色不再改变(C为有色气体)
D.混合气体的密度不变
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】硫的氧化物的排放是形成硫酸型酸雨的主要原因,含硫烟气(主要成分为SO2)的处理备受关注,主要有以下两种方法。请回答下列问题:
I.碱液吸收法
步骤1:用足量氨水吸收SO2。
步骤2:再加入熟石灰,发生反应2NH +Ca2++2OH-+SO
+Ca2++2OH-+SO ⇌CaSO3↓+2NH3•H2O。
⇌CaSO3↓+2NH3•H2O。
(1)已知:25℃时,Kb(NH3•H2O)=a;Ksp(CaSO3)=b。该温度下,步骤2中反应的平衡常数K=________ (用含a、b的代数式表示)。
Ⅱ.水煤气还原法
已知:
i.2CO(g)+SO2(g)⇌S(l)+2CO2(g)ΔH1═-37.0kJ•mol-1
ii.2H2(g)+SO2(g)⇌S(l)+2H2O(g)ΔH2=+45.4kJ•mol-1
(2)CO(g)与H2O(g)反应生成CO2(g)、H2(g)的热化学方程式为________ 。
(3)在一定压强下,发生反应ii。平衡时,SO2的转化率α(SO2)与原料气投料比[ ]和温度(T)的关系如图所示。
]和温度(T)的关系如图所示。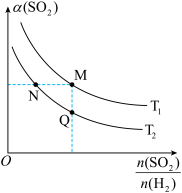 ①H2的转化率α(H2):M
①H2的转化率α(H2):M______ N(填“>”“<”或“=”)。
②逆反应速率:Q______ M(填“>”“<”或“=”)。
(4)T℃,向2L恒容密闭容器中充入2molCO(g)、2molSO2(g)和2molH2(g),发生反应i和反应ii。5min达到平衡时,CO2(g)和H2O(g)的物质的量分别为1.6mol、1.8mol。
①其他条件不变,6min时缩小容器容积,α(H2)________ (填“增大”“减小”或“不变)。
②该温度下,反应ii的平衡常数K=________ 。
I.碱液吸收法
步骤1:用足量氨水吸收SO2。
步骤2:再加入熟石灰,发生反应2NH
 +Ca2++2OH-+SO
+Ca2++2OH-+SO ⇌CaSO3↓+2NH3•H2O。
⇌CaSO3↓+2NH3•H2O。(1)已知:25℃时,Kb(NH3•H2O)=a;Ksp(CaSO3)=b。该温度下,步骤2中反应的平衡常数K=
Ⅱ.水煤气还原法
已知:
i.2CO(g)+SO2(g)⇌S(l)+2CO2(g)ΔH1═-37.0kJ•mol-1
ii.2H2(g)+SO2(g)⇌S(l)+2H2O(g)ΔH2=+45.4kJ•mol-1
(2)CO(g)与H2O(g)反应生成CO2(g)、H2(g)的热化学方程式为
(3)在一定压强下,发生反应ii。平衡时,SO2的转化率α(SO2)与原料气投料比[
 ]和温度(T)的关系如图所示。
]和温度(T)的关系如图所示。 ①H2的转化率α(H2):M
①H2的转化率α(H2):M②逆反应速率:Q
(4)T℃,向2L恒容密闭容器中充入2molCO(g)、2molSO2(g)和2molH2(g),发生反应i和反应ii。5min达到平衡时,CO2(g)和H2O(g)的物质的量分别为1.6mol、1.8mol。
①其他条件不变,6min时缩小容器容积,α(H2)
②该温度下,反应ii的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】汽车尾气中的 、
、 是大气污染物。我国科研工作者经过研究,可以用不同方法处理氮的氧化物,防止空气污染。回答下列问题:
是大气污染物。我国科研工作者经过研究,可以用不同方法处理氮的氧化物,防止空气污染。回答下列问题:
(1)已知,298K时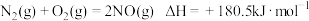
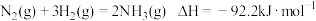
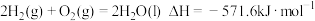
298K时, 将
将 转化成无毒物质的热化学方程式为
转化成无毒物质的热化学方程式为___________ 。
(2)利用某分子筛作催化剂,可脱除工厂废气中的 、
、 ,反应机理如图所示。
,反应机理如图所示。
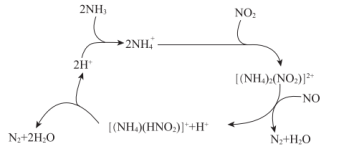
请写出整个反应过程的化学方程式:___________ 。
(3)一定条件下, 还原
还原 的反应
的反应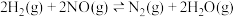 的速率方程为
的速率方程为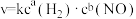 ,
, 下,该反应在不同浓度下的反应速率如表:
下,该反应在不同浓度下的反应速率如表:
则表中空白处表示的反应速率为___________ 。
(4)活性炭处理汽车尾气中 的原理:
的原理: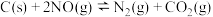 。
。 下,向某恒压密闭容器中加入足量的活性炭和一定量的
下,向某恒压密闭容器中加入足量的活性炭和一定量的 气体,以下各项能说明该反应一定达到平衡状态的是___________(填标号)。
气体,以下各项能说明该反应一定达到平衡状态的是___________(填标号)。
(5)科研人员进一步研究了催化剂对反应: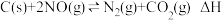 的影响,在三个完全相同的恒容密闭反应器中分别加入C、
的影响,在三个完全相同的恒容密闭反应器中分别加入C、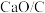 、
、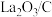 ,通入相同量的
,通入相同量的 。不同温度下,测得2h时
。不同温度下,测得2h时 的去除率如图所示:
的去除率如图所示:
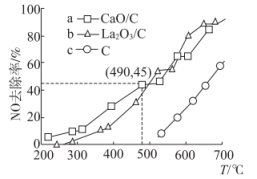
已知:490℃时,盛放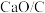 的容器内该反应已经达到平衡状态。
的容器内该反应已经达到平衡状态。
①
___________ 0(填“>”或“<”),判断的理由是___________ 。
②据图分析,490℃以下反应活性最好的是___________ (用a、b、c表示)
③490℃时,该反应的平衡常数为___________ (列式即可)。
 、
、 是大气污染物。我国科研工作者经过研究,可以用不同方法处理氮的氧化物,防止空气污染。回答下列问题:
是大气污染物。我国科研工作者经过研究,可以用不同方法处理氮的氧化物,防止空气污染。回答下列问题:(1)已知,298K时
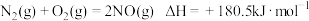
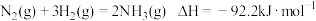
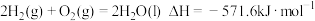
298K时,
 将
将 转化成无毒物质的热化学方程式为
转化成无毒物质的热化学方程式为(2)利用某分子筛作催化剂,可脱除工厂废气中的
 、
、 ,反应机理如图所示。
,反应机理如图所示。
请写出整个反应过程的化学方程式:
(3)一定条件下,
 还原
还原 的反应
的反应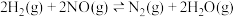 的速率方程为
的速率方程为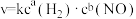 ,
, 下,该反应在不同浓度下的反应速率如表:
下,该反应在不同浓度下的反应速率如表: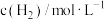 | 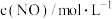 | 反应速率 |
| 0.1 | 0.1 |  |
| 0.3 | 0.1 | 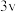 |
| 0.2 | 0.2 | 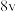 |
| 0.2 | 0.3 |
则表中空白处表示的反应速率为
(4)活性炭处理汽车尾气中
 的原理:
的原理: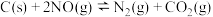 。
。 下,向某恒压密闭容器中加入足量的活性炭和一定量的
下,向某恒压密闭容器中加入足量的活性炭和一定量的 气体,以下各项能说明该反应一定达到平衡状态的是___________(填标号)。
气体,以下各项能说明该反应一定达到平衡状态的是___________(填标号)。A. | B.混合气体的总质量不变 |
| C.容器内气体的平均摩尔质量不变 | D.容器内气体的密度不变 |
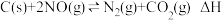 的影响,在三个完全相同的恒容密闭反应器中分别加入C、
的影响,在三个完全相同的恒容密闭反应器中分别加入C、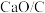 、
、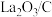 ,通入相同量的
,通入相同量的 。不同温度下,测得2h时
。不同温度下,测得2h时 的去除率如图所示:
的去除率如图所示:
已知:490℃时,盛放
 的容器内该反应已经达到平衡状态。
的容器内该反应已经达到平衡状态。①

②据图分析,490℃以下反应活性最好的是
③490℃时,该反应的平衡常数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】大气环境中NOx的减量化排放受到国内外广泛关注。利用碳还原NO的反应为:2NO(g)+C(s) N2(g)+CO2(g)。回答下列问题:
N2(g)+CO2(g)。回答下列问题:
(1)该反应在常温下可以自发进行,则反应的△H________ 0(填“>”“=”或“<”)'有利于提高NO平衡转化率的条件是____________ (任写一条)。
(2)以上反应可分为如下四步反应方程,写出其中第三步的反应:
第一步:2NO=(NO)2
第二步:(NO)2+C=N2O+C(O)
第三步:_________________
第四步:2C(O)=C+CO2
(3)对比研究活性炭负载钙、镧氧化物的反应活性。在三个反应器中分别加入C、CaO/C、La2O3/C,通入NO使其浓度达到0.1 mol/L。不同温度下,测得第2小时NO去除率如图所示:
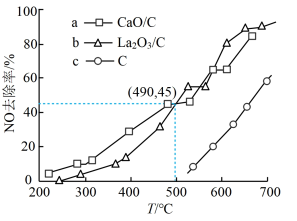
①据图分析,温度490°C以下,三种情况下反应的活化能最小的是________ 用a、b、c表示);CaO/C、La2O3/C去除NO效果比C更好,其依据是________ (写一条)。
②上述实验中,490°C时,若测得CaO/C对NO的去除率为60%,则可能采取的措施是________ 。
A.及时分离出CO2 B.压缩体积
C.恒容下,向体系中通入氦气 D.改良优化了催化剂
③在CaO/C、490°C条件下0~2 h内的平均反应速率v(NO)=_______ mol•L-1•h-1,该温度下此反应的平衡常数为121,则反应达平衡时NO的去除率为________ (保留二位有效数字)。
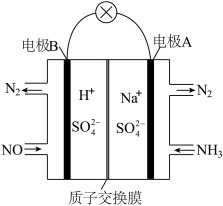
(4)利用电化学原理处理NOx也是重要的研究方向,如下装置图中正极的电极反应式为:_________ 。
 N2(g)+CO2(g)。回答下列问题:
N2(g)+CO2(g)。回答下列问题:(1)该反应在常温下可以自发进行,则反应的△H
(2)以上反应可分为如下四步反应方程,写出其中第三步的反应:
第一步:2NO=(NO)2
第二步:(NO)2+C=N2O+C(O)
第三步:
第四步:2C(O)=C+CO2
(3)对比研究活性炭负载钙、镧氧化物的反应活性。在三个反应器中分别加入C、CaO/C、La2O3/C,通入NO使其浓度达到0.1 mol/L。不同温度下,测得第2小时NO去除率如图所示:

①据图分析,温度490°C以下,三种情况下反应的活化能最小的是
②上述实验中,490°C时,若测得CaO/C对NO的去除率为60%,则可能采取的措施是
A.及时分离出CO2 B.压缩体积
C.恒容下,向体系中通入氦气 D.改良优化了催化剂
③在CaO/C、490°C条件下0~2 h内的平均反应速率v(NO)=
(4)利用电化学原理处理NOx也是重要的研究方向,如下装置图中正极的电极反应式为:

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】合成氨工业对国民经济和社会发展具有重要意义,对于密闭容器中的反应: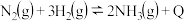
(1)写出该反应的逆反应的化学平衡常数表达式______ ,升高温度,该反应化学反应速率______ ,氢气的转化率______  以上均填“增大”、“减小”或“不变”
以上均填“增大”、“减小”或“不变” 。实际生产中温度一般控制在
。实际生产中温度一般控制在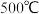 ,原因是
,原因是______ 。
(2)能表示该反应在恒温恒容密闭容器中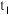 时刻后已经达到平衡状态的图示是
时刻后已经达到平衡状态的图示是______ 。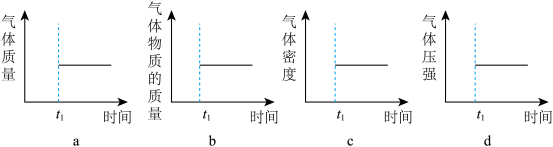
(3)浓度 的氨水,pH为
的氨水,pH为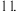 当用蒸馏水稀释100倍时,则
当用蒸馏水稀释100倍时,则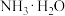 的电离平衡将向
的电离平衡将向______ 方向移动 填“正”或“逆”
填“正”或“逆” ,溶液的pH将为
,溶液的pH将为______ 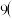 “大于”“小于”“等于”
“大于”“小于”“等于” 。
。
设计一个简单实验,证明一水合氨是弱碱:______ 。
某化学兴趣小组进行了下列关于氯化铵的课外实验:
【实验操作】
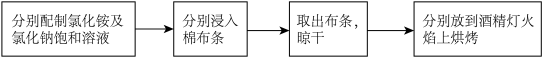
浸过氯化钠溶液的布条很快烧光,浸过氯化铵溶液的布条不燃烧,冒出白烟。
(4)氯化铵饱和溶液中离子浓度由大到小的顺序是______ 。白烟的成分是______ 。
(5)请推测浸过氯化铵溶液的布条不燃烧、不易着火的主要原因 写出一条即可
写出一条即可
______
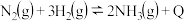
(1)写出该反应的逆反应的化学平衡常数表达式
 以上均填“增大”、“减小”或“不变”
以上均填“增大”、“减小”或“不变” 。实际生产中温度一般控制在
。实际生产中温度一般控制在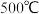 ,原因是
,原因是(2)能表示该反应在恒温恒容密闭容器中
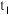 时刻后已经达到平衡状态的图示是
时刻后已经达到平衡状态的图示是
(3)浓度
 的氨水,pH为
的氨水,pH为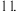 当用蒸馏水稀释100倍时,则
当用蒸馏水稀释100倍时,则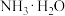 的电离平衡将向
的电离平衡将向 填“正”或“逆”
填“正”或“逆” ,溶液的pH将为
,溶液的pH将为 “大于”“小于”“等于”
“大于”“小于”“等于” 。
。设计一个简单实验,证明一水合氨是弱碱:
某化学兴趣小组进行了下列关于氯化铵的课外实验:
【实验操作】

浸过氯化钠溶液的布条很快烧光,浸过氯化铵溶液的布条不燃烧,冒出白烟。
(4)氯化铵饱和溶液中离子浓度由大到小的顺序是
(5)请推测浸过氯化铵溶液的布条不燃烧、不易着火的主要原因
 写出一条即可
写出一条即可
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.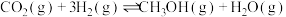

Ⅱ.

Ⅲ.

回答下列问题:
(1)
___________ kJ⋅mol-1。
(2)一定条件下,向体积为VL的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平衡时,容器中 为a mol,CO为b mol,此时
为a mol,CO为b mol,此时 的浓度为
的浓度为___________ mol/L(用含a、b、V的代数式表示,下同),反应Ⅲ的平衡常数为___________ 。
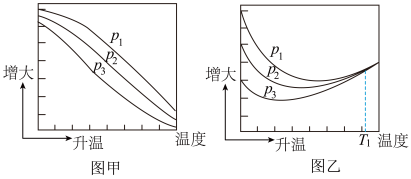
(3)不同压强下,按照 投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
已知: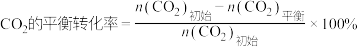
CH3OH的平衡产率=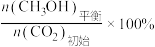
其中纵坐标表示CO2平衡转化率的是图___________ (填“甲”或“乙”);压强p1、p2、p3由大到小的顺序为___________ ;图乙中T1温度时,三条曲线几乎交于一点的原因是___________ 。
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为___________(填标号)。
(5)甲醇燃料电池中甲醇在___________ (填“正”或“负”)极发生反应,酸性条件下其正极的电极反应式为___________ 。
(6)在允许O2-自由迁移的固体电解质燃料电池中,CnH2n+2放电的电极反应式为___________ 。
Ⅰ.
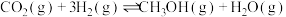

Ⅱ.


Ⅲ.


回答下列问题:
(1)

(2)一定条件下,向体积为VL的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平衡时,容器中
 为a mol,CO为b mol,此时
为a mol,CO为b mol,此时 的浓度为
的浓度为(3)不同压强下,按照
 投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
已知:
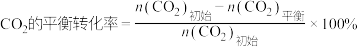
CH3OH的平衡产率=
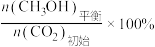
其中纵坐标表示CO2平衡转化率的是图
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为___________(填标号)。
| A.低温、高压 | B.高温、低压 | C.低温、低压 | D.高温、高压 |
(5)甲醇燃料电池中甲醇在
(6)在允许O2-自由迁移的固体电解质燃料电池中,CnH2n+2放电的电极反应式为
您最近一年使用:0次
【推荐3】一定量的 在恒压密闭容器中发生反应:
在恒压密闭容器中发生反应: 。平衡时,体系中各气体体积分数与温度的关系如图所示:
。平衡时,体系中各气体体积分数与温度的关系如图所示:
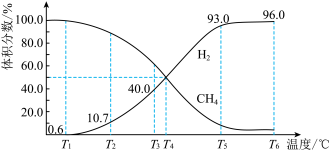
(1).已知甲烷、碳、氢气的燃烧热分别为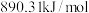 、
、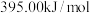 、
、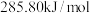 ,则该反应的反应热
,则该反应的反应热
__________ 。
(2).下列能说明反应一定达到平衡状态的是_______ 。
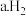 和
和 的体积分数相等
的体积分数相等
 混合气体的平均相对分子质量不变
混合气体的平均相对分子质量不变
 混合气体的密度不变
混合气体的密度不变
 气体总压强不再变化
气体总压强不再变化
 碳的质量不再改变
碳的质量不再改变
(3). 时,若在平衡体系中充入惰性气体,此时反应速率
时,若在平衡体系中充入惰性气体,此时反应速率____  填“变大”、“变小”或“不变”
填“变大”、“变小”或“不变” ,且
,且
_____ 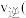 填“
填“ ”、“
”、“ ”或“
”或“ ”
” 。
。
(4).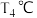 时,若在平衡体系中充入等体积的
时,若在平衡体系中充入等体积的 和
和 ,则平衡
,则平衡_____ 移动,其理由是_______ 。
(5).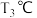 时,反应达平衡后
时,反应达平衡后 的转化率为
的转化率为____________ 。
 在恒压密闭容器中发生反应:
在恒压密闭容器中发生反应: 。平衡时,体系中各气体体积分数与温度的关系如图所示:
。平衡时,体系中各气体体积分数与温度的关系如图所示:
(1).已知甲烷、碳、氢气的燃烧热分别为
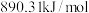 、
、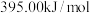 、
、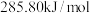 ,则该反应的反应热
,则该反应的反应热
(2).下列能说明反应一定达到平衡状态的是
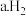 和
和 的体积分数相等
的体积分数相等  混合气体的平均相对分子质量不变
混合气体的平均相对分子质量不变 混合气体的密度不变
混合气体的密度不变  气体总压强不再变化
气体总压强不再变化  碳的质量不再改变
碳的质量不再改变(3).
 时,若在平衡体系中充入惰性气体,此时反应速率
时,若在平衡体系中充入惰性气体,此时反应速率 填“变大”、“变小”或“不变”
填“变大”、“变小”或“不变” ,且
,且
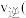 填“
填“ ”、“
”、“ ”或“
”或“ ”
” 。
。(4).
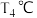 时,若在平衡体系中充入等体积的
时,若在平衡体系中充入等体积的 和
和 ,则平衡
,则平衡(5).
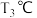 时,反应达平衡后
时,反应达平衡后 的转化率为
的转化率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题。
I.已知2C3H6(g)+2NH3(g)+3O2(g) 2C3H3N(g)+6H2O(g)
2C3H3N(g)+6H2O(g)  =-1030kJ/mol。
=-1030kJ/mol。
(1)上述为丙烯(C3H6)合成丙烯腈(C3H3N)的反应,则该反应___________。
(2)该反应
___________ 0(填>、<或=)。
(3)恒容时该反应生成丙烯腈的速率与时间的关系如图。
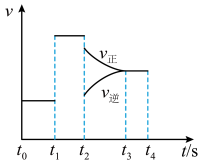
t1改变的条件为___________ ,t2改变的条件为___________ ;反应速率最大的时间段为___________ ,丙烯(C3H6)转化率最大的时间段为___________ 。
II.向1L密闭容器投入2molC3H6、2molNH3和3molO2反应5min,α(丙烯)与T的关系如图。
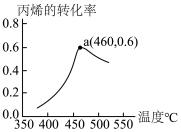
(4)460℃时平衡常数=___________ ,用O2表示反应速率v(O2)=___________ 。
(5)当温度低于460℃时,丙烯的转化率___________ (“是”或“不是”)所对应温度下的平衡转化率,理由是___________ 。
I.已知2C3H6(g)+2NH3(g)+3O2(g)
 2C3H3N(g)+6H2O(g)
2C3H3N(g)+6H2O(g)  =-1030kJ/mol。
=-1030kJ/mol。(1)上述为丙烯(C3H6)合成丙烯腈(C3H3N)的反应,则该反应___________。
| A.较高温度下自发进行 | B.较低温度下自发进行 |
| C.任何温度下都可自发进行 | D.任何温度下都不能自发进行 |
(2)该反应

(3)恒容时该反应生成丙烯腈的速率与时间的关系如图。

t1改变的条件为
II.向1L密闭容器投入2molC3H6、2molNH3和3molO2反应5min,α(丙烯)与T的关系如图。

(4)460℃时平衡常数=
(5)当温度低于460℃时,丙烯的转化率
您最近一年使用:0次
【推荐2】天然气经催化重整转化成合成气(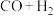 )后再合成其他化工产品,既可减少能源浪费,又能生产高附加值产品。以甲烷、二氧化碳为原料催化重整制合成气,体系中可发生如下两个反应:
)后再合成其他化工产品,既可减少能源浪费,又能生产高附加值产品。以甲烷、二氧化碳为原料催化重整制合成气,体系中可发生如下两个反应:
反应Ⅰ:

反应Ⅱ:

(1)反应Ⅰ可分为如下两步:
 裂解:
裂解: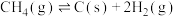
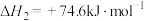
 重整:
重整: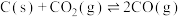
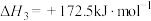
则 =
=______ 。反应Ⅰ能够自发进行的条件是______ ,判断依据是______ 。
(2) ℃时,向4L容器中通入7mol
℃时,向4L容器中通入7mol 、6mol
、6mol ,发生反应Ⅰ、Ⅱ.
,发生反应Ⅰ、Ⅱ. min后达到平衡,体系中
min后达到平衡,体系中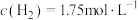 ,
,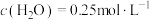 ,压强为
,压强为 。①此温度下,反应Ⅰ的平衡常数
。①此温度下,反应Ⅰ的平衡常数 =
=______ (写出计算式即可,不必化简)[对于气相反应,用某组分B的平衡压强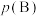 代替物质的量浓度
代替物质的量浓度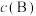 表示的平衡常数,记作
表示的平衡常数,记作 ,如
,如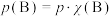 ,
, 为平衡总压强,
为平衡总压强,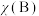 为平衡系统中B的物质的量分数]。
为平衡系统中B的物质的量分数]。
②请在图中画出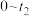 时段
时段 随时间变化曲线并标出
随时间变化曲线并标出 的平衡浓度
的平衡浓度______ 。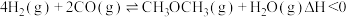
①在恒温恒压条件进行此反应,下列能说明反应已达到平衡的是______ (填标号)。
A. 、
、 、
、 、
、 的反应速率之比为4:2:1:1
的反应速率之比为4:2:1:1
B. 、
、 、
、 、
、 的物质的量之比为4:2:1:1
的物质的量之比为4:2:1:1
C.混合气体的平均摩尔质量保持不变
D.容器中气体的密度保持不变
②某温度下,将2.0mol 和4.0mol
和4.0mol 充入容积为2L的密闭容器中,反应达到平衡时,改变压强和温度,平衡体系中
充入容积为2L的密闭容器中,反应达到平衡时,改变压强和温度,平衡体系中 的物质的量分数变化情况如图所示,关于温度和压强的关系判断正确的是
的物质的量分数变化情况如图所示,关于温度和压强的关系判断正确的是______ (填标号)。 ,
,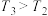 B.
B. ,
,
C. ,
, D.
D. ,
,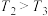
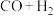 )后再合成其他化工产品,既可减少能源浪费,又能生产高附加值产品。以甲烷、二氧化碳为原料催化重整制合成气,体系中可发生如下两个反应:
)后再合成其他化工产品,既可减少能源浪费,又能生产高附加值产品。以甲烷、二氧化碳为原料催化重整制合成气,体系中可发生如下两个反应:反应Ⅰ:


反应Ⅱ:


(1)反应Ⅰ可分为如下两步:
 裂解:
裂解: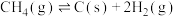
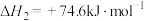
 重整:
重整: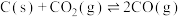
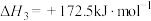
则
 =
=(2)
 ℃时,向4L容器中通入7mol
℃时,向4L容器中通入7mol 、6mol
、6mol ,发生反应Ⅰ、Ⅱ.
,发生反应Ⅰ、Ⅱ. min后达到平衡,体系中
min后达到平衡,体系中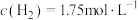 ,
,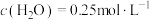 ,压强为
,压强为 。①此温度下,反应Ⅰ的平衡常数
。①此温度下,反应Ⅰ的平衡常数 =
=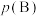 代替物质的量浓度
代替物质的量浓度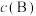 表示的平衡常数,记作
表示的平衡常数,记作 ,如
,如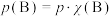 ,
, 为平衡总压强,
为平衡总压强,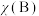 为平衡系统中B的物质的量分数]。
为平衡系统中B的物质的量分数]。②请在图中画出
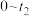 时段
时段 随时间变化曲线并标出
随时间变化曲线并标出 的平衡浓度
的平衡浓度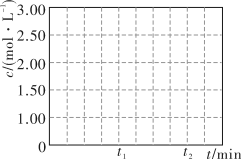
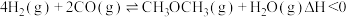
①在恒温恒压条件进行此反应,下列能说明反应已达到平衡的是
A.
 、
、 、
、 、
、 的反应速率之比为4:2:1:1
的反应速率之比为4:2:1:1B.
 、
、 、
、 、
、 的物质的量之比为4:2:1:1
的物质的量之比为4:2:1:1C.混合气体的平均摩尔质量保持不变
D.容器中气体的密度保持不变
②某温度下,将2.0mol
 和4.0mol
和4.0mol 充入容积为2L的密闭容器中,反应达到平衡时,改变压强和温度,平衡体系中
充入容积为2L的密闭容器中,反应达到平衡时,改变压强和温度,平衡体系中 的物质的量分数变化情况如图所示,关于温度和压强的关系判断正确的是
的物质的量分数变化情况如图所示,关于温度和压强的关系判断正确的是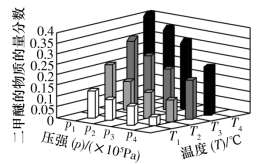
 ,
,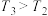 B.
B. ,
,
C.
 ,
, D.
D. ,
,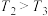
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题。
(1)工业上用 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:
Ⅰ.

Ⅱ.
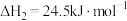
①反应I在___________ (填“高温”、“低温”或“任何温度”)下自发。
②写出 和
和 转化为
转化为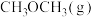 和
和 的热化学方程式
的热化学方程式___________ 。
(2)亚硝酸氨(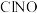 )是有机合成中的重要试剂,可由反应
)是有机合成中的重要试剂,可由反应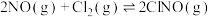 制备。在
制备。在 的密闭容器中充入
的密闭容器中充入 和
和 发生上述反应,在不同温度下测得
发生上述反应,在不同温度下测得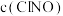 与时间的关系如图。
与时间的关系如图。
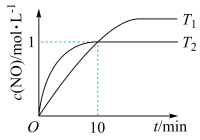
①反应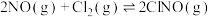 的化学平衡常数表达式为
的化学平衡常数表达式为
___________ 。
②
___________  (填“>““<”或“=”,下同),该反应的
(填“>““<”或“=”,下同),该反应的
___________ 0。
③ 时,反应从开始到
时,反应从开始到 时
时 的平均反应速率
的平均反应速率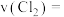
___________ 。
④写出两条能提高 平衡转化率的措施
平衡转化率的措施___________ 。
(1)工业上用
 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:Ⅰ.


Ⅱ.

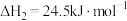
①反应I在
②写出
 和
和 转化为
转化为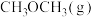 和
和 的热化学方程式
的热化学方程式(2)亚硝酸氨(
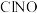 )是有机合成中的重要试剂,可由反应
)是有机合成中的重要试剂,可由反应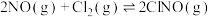 制备。在
制备。在 的密闭容器中充入
的密闭容器中充入 和
和 发生上述反应,在不同温度下测得
发生上述反应,在不同温度下测得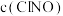 与时间的关系如图。
与时间的关系如图。
①反应
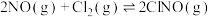 的化学平衡常数表达式为
的化学平衡常数表达式为
②

 (填“>““<”或“=”,下同),该反应的
(填“>““<”或“=”,下同),该反应的
③
 时,反应从开始到
时,反应从开始到 时
时 的平均反应速率
的平均反应速率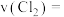
④写出两条能提高
 平衡转化率的措施
平衡转化率的措施
您最近一年使用:0次